СКАНДИЙ
Элемент с атомным номером 21 "экабор" и его свойства предсказал в 1871 г. Д. И.Менделеев. Открыл элемент шведский химик Нильсон в 1879 г., работая над изилечением редкоземельного элемента иттербия из минерала гадо - линита. Металлический скандий 94 - 98 %-ной чистоты получен в 1937 г. Фишером электролизом расплаиленного хлорида скандия.
Свойства скандия
Скандий - элемент ША подгруппы Периодической системы химических элементов. В природе известен один стабильный изотоп 45Sc; известно 12 искусственных радиоактивных изотопов.
Ниже приведены некоторые физические свойства скандия:
Атомная масса 44,9559
TOC \o "1-3" \h \z Плотность, г/см3 2,989
Тип и параметры решетки, нм: гексагональная, а = 0,33085,
С = 0,5268; ОЦК (выше 1337 °С)
Температура, °С:
Плаиления 1541
Кипения 2836
Удельная теплоемкость, Дж/(моль • К), при t, °С:
25 25,52
1500 39,80
Теплопопроводность, В/(см'К) .0,157
Твердость по Бринеллю, МПа 390
Удельное электросопротивление поликристаллического
Образца р 0 , мкОм • см 41-51
23 С
Компактный скандий - серебристо-белый металл. Непосредственно реагирует с кислородом, галогенами, серой, углеродом. На воздухе образующаяся на поверхности металла пленка предотвращает дальнейшее окисление. С азотом реагирует выше 500 °С с образованием нитрида ScN. При нагревании вытесняет водород из воды, легко растворяется в минеральных кислотах, за НЫслючением хромовой и плавиковой кислот, медленно реагирует с концентрированным раствором гидроксида натрия. Радиус иона Sc3+ (0,083 нм по Н. В.Белову и Г. В.Бокию) меньше, чем радиус иона Yi+ (0,097 нм) - и трехзарядных ионов РЗЭ (0,088 - 0,103 нм). Поэтому в соединениях скандия выражено стремление к гидролизу сильнее, чем в аналогичных соединениях РЗЭ. Скандий склонен к образованию двойных и комплексных соединений с анионами и нейтральными лиганда - ми в большей мере, чем РЗЭ.
С металлами I, II, VII, VIII побочных подгрупп и II, III, IV, V главных подгрупп Периодической системы элементов скандий образует интерметаллические соединения типа ScMe, Sc2Me, ScMe2, ScMe3 и другие.
Элементы III, IV, V и VI побочных подгрупп образуют со скандием эвтектики или области несмешиваемости в жидком состоянии, проявляется растворимость в твердом состоянии.
Свойства соединений скандия
Скандий образует соединения, отвечающие степени окисления элемента +3. Другие степени окисления нехарактерны для скандия.
Оксид и гидроксид скандия. Оксид Sc203 - белое вещество, образующееся при окислении скандия кислородом, термическом разложении гидроксида, карбоната, оксалата, сульфата, нитрата скандия. гпл = 2480 °С, плотность 3,86 г/см3. В воде малорастворим. Хорошо растворяется в концентрированных минеральных кислотах.
Гидроксид скандия Sc(OH)3 - аморфное соединение. Осаждается действием на растворы солей скандия растворами аммиака или щелочей,- рН начала выделения 4,9. Растворим и растворах щелочей, карбонатов аммония, щелочных металлов; растворимость резко снижается в присутствии малорастворимых гидроксидов железа, марганца и др.
Карбонат скандия. Для скандия характерно образование основных карбонатов [Sc(0H)m]2(C03)3_m • ЗН20, растворимых в растворах (NH4)2C03 и Na2C03 лучше, чем аналогичные соединения РЗЭ.
Нитрат скандия Sc(NOj)3 • 4Н20 - хорошо растворимая соль; растворимость в воде: 61,27% (при 15 °С), 67,60% (при 50 °С).
Сульфат скандия Sc2(S04)3 образует гидраты с 2; 4; 5 и 6 молекулами воды. Растворимость в воде 28,53% (при 254;). С сульфатами щелочных металлов образует соединения MefSd^SOjJ или Afe^SctSO^J. KjCS^SOJJ в 20 раз менее растворим в растворе K2S04, чем аналогичные соединения элементов иттриевой подгруппы РЗЭ.
Фосфат скандия ScP04 • 2Н20 - малорастворим, получается действием на водный раствор солей скандия фосфорной кислоты.
Оксалат скандия Sc2(C204)3 • лН20(л = 3; 4; 5; 6; 18) образуется при действии щавелевой кислоты на нейтральные или слабокислые растворы солей скандия. Малорастворим, ПРсс (с 0 ■>= Ю-27.
2 4^3
Яодат скандия Sc(IOj)3 • 1,5Н20 - хорошо растворим в отличие от аналогичных соединений тория и циркония.
Фторид скандия ScF3 - белое кристаллическое вещество, t = 1552 °С, *кип= = 1607 °С. Малорастворим, ПР^/г = 3 • Ю-20. При обработке концентрированной H2S04 превращается в сульфат, при нагревании в растворе NaOH - в гидроксид. Растворим в HF, растворах фторидов щелочных металлов и аммония; л растворе образуются комплексы [ScFj-, [ScFg]3-.
Хлорид скандия ScCl3 - белое кристаллическое вещество, гигроскопичен, 'пл = 'кип = 975 °С. Температурная зависимость давления пара (МПа):
LgP = -14200/Г + 10,49 (1066 - 1229 К).
Кристаллогидрат ScCl3 * 6Н20 при нагревании на воздухе превращается сначала в оксохлорид ScOCl, плохо растворимый в воде, кислотах и щелочах, затем - в Sc203.
Карбид скандия ScC изучен больше, чем другие карбиды скандия. Получается синтезом из элементарных веществ или восстановлением Sc203 углем. Температура плавления 1800 °С, микротвердость 26,7 ГПа.
Области применения
Скандий и его соединения в настоящее время применяют в производстве легких сплавов, электронной технике, светотехнике, производстве специальной керамики. Возможности применения скандия ограничены высокой ценой. В 1988 г. оксид скандия (lr) стоил 2,8 долл., дистиллированный металл (чистота 99,99%) - 15 долл. Высокая цена связана с малыми объемами производства (около 100 кг в год в пересчете на металл). Основные производители скандиевой продукции - КНР, Франция.
Легкие сплавы. Скандий представляет интерес как конструкционный материал для ракето - и самолетостроения, астронавтики, поскольку, обладая значительно более высокой температурой плавления, чем алюминий, имеет ту же плотность. Особый интерес представляют сплавы Al — Sc, Mg - Sc, Mg - Sc - Li, Mg - Y - Sc. Так как добавка десятых долей процента скандия к алюминию и его сплавам обусловливает повышение прочностных, в определенных случаях пластических свойств, рост сопротивления против коррозионного растрескивания, улучшение свариваемости деформированных полуфабрикатов. При кристаллизации расплава в процессе образования слитков большая часть скандия входит в пересыщенный раствор, а оставшаяся часть выделяется в виде частиц Al3Sc (рис. 89), которые обусловливают измельчение литого зерна.
Легирование 0,4% скандия сплавов Al - Mg (2 - 8,5 Mg)
T,°C
\
\
![]()
![]()
ВЦй
620
A*scAi3
AaaJLSOO
Al
Ршс.89. Диаграмма состояния системы Al-Sc в области, богатой алюминием
Увеличивает временное сопротивление на 20 - 35 %, а предел текучести на 60 - 80%. При этом относительное удлинение остается достаточно высоким (15 - 20%).
Электронная техника. Влажная область применения оксида скандия - производство ферритов для ЭВМ с индукцией 0,08 - 0,1 Тл, что в 3 раза меньше, чем у ферритов из оксидов железа, магния, марганца. Такие ферриты меньше перегреваются при перемагничивании, что увеличивает быстродействие магнитной памяти ЭВМ.
Светотехника. Мателлогалогенидные (иодидные) ртутные лампы с добавками скандия используют для освещения промышленных зданий и спортивных сооружений.
Производство керамики. Разработаны различные виды керамики на основе ZrOz и Hf02 с добавками Sc203, успешно работающие при высоких температурах.
Другие области применения. Гидрид скандия используют в ядерной технике как высокотемпературный замедлитель нейтронов. Борид скандия ScB2 предложено использовать как компонент легких жаропрочных сплавов, а также в материалах катодов электронных приборов. Оксид скандия - компонент германатных оптических стекол, люминофоров.
Сырьевые источники скандия
Скандий - типичный рассеянный литофильный элемент. Содержание его в земной коре 10~3% (по массе). Собственных месторождений не образует.
Собственные минералы скандия - тортвейтит Sc2[Si207] и стереттит ScP04 • 2Н20 - большая редкость и промышленного значения не имеют. Более распространены минералы, в которых скандий присустсвует в виде изоморфной примеси в количестве 0,005 - 0,3% Sc203. Скандийсодержащие минералы (оксиды, карбонаты, силикаты, фосфаты, вольфраматы) содержат ионы, характеризующиеся близким к Sc3+ (0,083 нм) радиусом иона, нм: Fe2+ 0,080, РЗЭ 0,102 - 0,080, Mg2+ 0,074, Са2+ 0,104, Мп2+ 0,091, Zr4+ 0,082, Th4+ 0,095, U4+ 0,089. Изоморфизм обусловлен также близостью других кристаллохимических констант скандия и перечисленных элементов.
Проблема промышленного получения скандия может быть решена при использовании рассеянного скандия, извлекаемого попутно из руд цветных и редких металлов. При концентрировании скандия в отходах производства (растворах, шла - мах, шлаках и пр.) создаются условия для извлечения без нарушения основной технологии.
Титановое сырье. В титановом сырье содержится Sc203 (до 0,1 % в ильмените, до 0,3 % в сфене). При обогащении ильменитовых концентратов путем восстановительной электроплавки скандий переходит в титановый шлак.
Цирконийсодержащие руды. Цирконы и другие минералы циркония содержат 0,001 - 0,08 % Sc203. При переработке цирконового концентрата спеканием известью и хлоридом кальция скандий концентрируется в основном в маточниках после выделения основного сульфата циркония.
Руды вольфрама. Содержание Sc203 в вольфрамитах 0,005 - 1,0 %. При гидрометаллургической переработке, включающей спекание концентрата с Na2C03 и последующее выщелачивание, скандий остается в кеке от выщелачивания, и его содержание повышается в 2 - 3 раза по сравнению с содержанием в вольфрамите.
Руды урана содержат 10_3 - 10-4% Sc203. При вскрытии урановых руд серной или азотной кислотами скандий переходит вместе с ураном в раствор. При вскрытии руд растворами Na2C03 скандий в основном концентрируется в кеках от выщелачивания.
Руды алюминия. Бокситы содержат 0,001 - 0,01 % Sc203. Ввиду больших масштабов переработки бокситы могут стать важным источником скандия. При переработке бокситов по способу Байера и способу спекания скандий преимущественно остается в красном шламе.
Другие источники скандия - некоторые железные руды (содержание 0,001 - 0,005 % Sc203), руды олова (0,02 - 0,22 % Sc203), концентраты берилла (0,1 - 0,2 % Sc203), золы некоторых углей (0,01 % Sc203), фосфориты.
Z ПЕРЕРАБОТКА СКАНДИЙ СО ДЕРЖАЩЕГО СЫРЬЯ
Содержание скандия в продуктах переработки минерального сырья составляет сотые - десятые доли процента. Поэтому из исходных продуктов вначале получают концентраты, которые затем перерабатывают на соединения скандия.
Для извлечения скандия из продуктов в раствор применяют выщелачивание кислотами (например, соляной кислотой), разложение хлорированием, серной кислотой или гидроксидом натрия с последующим водным или кислотным выщелачиванием
Для выделения скандия из растворов используют следующие основные способы: осаждение в составе малорастворимых соединений, экстракция органическими растворителями, ионообменные способы.
Методы осаждения
Осаждение гидроксида используют для отделения от щелочных и щелочно-земельных металлов:
ScClj + 3NH3 • Н20 = Sc(OH)3 + 3N4HC1. (12.1)
Из данных табл.11 следует, что возможно, используя разницу рН осаждения гидроксидов, в некоторой степени очистить скандий от Zr, Ті, Th и Се (+4), так как они осаждаются при более низких рН, чем гидроксид скандия, и от ряда РЗЭ и Fe (+2), осаждающихся при более высоких значениях рН. Метод не дает возможность отделить Fe (+3), в присутствии которого Sc(OH)3 осаждается при более низком значении рН, и от алюминия, имеющего близкое значение рН осаждения. Метод прост, недостаток его - плохая фильт - руемость осадков.
Таблица 11. рН осаждена некоторых гидроксидов
|
Гидроксид |
РН |
Гидроксид |
РН |
Гидроксид |
РН |
|
Sc(OH)3 ZrOj-xHjO Тю2-*н2о Се(ОН)4 |
4,9-5,5 1,9-2,6 0,7 1,2 |
La(OH), Се(ОН)3 Fe(OH), Mg(OH)2 |
6,3 7,4 6,6-9,3 8,3-11,3 |
Th(OH)4 А1(ОН)3 Fe(OH)3 |
3,0 3,6-5,1 1,6-3,5 |
Осаждение оксалата. В результате осаждения оксалата скандия
2ScCl3 + ЗН2С204 + 6Н20 = Sc2(C204)3-6H20 + 6НС1 (12.2)
Возможно отделение скандия от алюминия и железа. При избытке щавелевой кислоты осаждение неполное вследствие образования комплексного аниона [Sc(C204)3]3_. Условия осаждения: рН = 2*3, температура 90 °С, продолжительность 4 ч.
При выделении оксалата скандия, особенно из бедных растворов, более полному осаждению способствует присутствие кальция, играющего роль носителя.
Для отделения от РЗЭ используют разницу в устойчивости комплексных соединений, образуемых оксалатами скандия и РЗЭ и ЭДТА.
При кипячении раствора, содержащего эти комплексные соединения, менее прочные соединения РЗЭ разлагаются, и РЗЭ могут быть выделены из раствора в составе оксалатов. После отделения раствора, вводя в него твердую щавелевую кислоту, скандий выделяют в осадок.
Осаждение карбоната. Карбонат скандия растворяется в отличие от соединений РЗЭ, Fe, Мп, Са в избытке раствора Na2C03 или (NH4)2C03 с образованием комплексных соединений, что рекомендовано использовать для очистки от РЗЭ, Fe, Мп, Са:
Sc3+ + 4Na2C03 = Naj[Sc(C03)4] + 3Na+; (12.3)
Sc3+ + 2(NH4)2C03 = NH4[Sc(C03)2] + 3NH4. (12.4)
Карбонатный комплекс при кипячении разрушается. В осадок выделяется плохо растворимый карбонат скандия переменного состава.
Недостаток карбонатной обработки - необходимость применения большого объема растворов соды или карбоната аммония в связи с умеренной растворимостью в них соединений скандия и плохая фильтруемость осадков.
Осаждение фторида. ScF3 - малорастворим, но растворяется (в отличие от фторидов РЗЭ и тория) в растворе NH4F с образованием фтороскандата:
ScF3 + 3NH4F = (NH4)3[ScF6]. (12.5)
Для выделения фторида скандия из бедных растворов применяют фториды и кремнефториды натрия и калия, плавиковую кислоту, кремнефтористоводородную кислоту; осадитель берут с избытком.
Недостаток метода - трудность перевода фторида скандия в растворимое состояние. Для этого необходима обработка концентрированной серной кислотой при 180 - 250 °С или 20 - 30 %-ным раствором NaOH при 60 - 80 °С в течение ' 2 - Зч.
Ионный обмен
Метод применяют: а) для выделения соединения скандия из разбавленного раствора; б) для очистки растворов соединений скандия от примесей. С целью повышения эффективности при очистке скандия от наиболее трудно отделяемых примесей (РЗЭ, Y, Th) применяют сочетание ионообменного разделения на катионитах с комплексообразованием (при десорбции). Хорошие десорбенты - лимонная кислота и этилен - диаминтетрауксусная кислота. Устойчивость комплексных соединений повышается в ряду La < Y < Yb < Sc, так что при десорбции в первую очередь вымывается скандий. Процесс включает:
Пропускание раствора с разделяемой смесью через колонку со смолой в аммонийной или водородной форме (стадия сорбции):
Sc3+ + 3NH4fl Scflj + 3NHJ; (12.6)
Десорбцию ионов раствором лимонной кислоты (или ЭДТА):
Scfl3 + 2Н3С6Н507 H3[Sc(C6H507)2] + 3HR. (12.7)
Экстракция
Один из наиболее разработанных способов - экстракция ро - данидного комплекса H[Sc(CNS)4] диэтиловым эфиром из хло - ридных или нитратных растворов. Как видно, коэффициенты распределения скандия и ряда сопуствующих элементов сильно различаются (рН = 3,5):
Элемент D Элемент D Элемент D
Ве2+ 1 Sc3+ 2,9 Zr»+ 0,00001
|
Mg2+ |
0,0002 |
РЗЭ 0,0007 |
Th4+ |
0,0006 |
|
Иттриевой |
||||
|
Са2+ |
Подгруппы (Ме3+) |
|||
|
0,0004 |
La3+ 0,00001 |
Mn2+ |
0,0014 |
|
|
А13+ |
0,59 |
Ti4+ 0,025 |
Fe3+ |
0,75 |
Перед экстракцией Fe(+3) восстанавливают до Fe(+2). Скандий реэкстрагируют, многократно обрабатывая экстракт водой. Недостаток способа - огнеопасность экстрагента, большой расход роданида аммония.
Другие экстрагенты, применяемые в технологии скандия: ТБФ, диалкильные эфиры алкилфосфорной кислоты (ДААФ), Д2ЭГФК и др. Экстракцию скандия ТБФ и ДААФ проводят в сильнокислых средах в присутствии высаливателей (хлориды или нитраты кальция и магния). Экстракция скандия ТБФ из хлоридных растворов протекает с образованием сольватов ScCl3 • дгТБФ (х меняется от 2 до 3 в зависимости от условий кислотности и наличия высаливателей). Коэффициент распределения скандия при экстракции ТБФ из 6 н. НСІ составляет 3,2, иттрия - 0,001 (т. е. коэффициент разделения равен 3200). Реэкстрагируют скандий разбавленной НС1.
Алкилфосфорные кислоты имеют меньшую селективность, чем ТБФ, и вместе со скандием экстрагируют цирконий, торий, титан, железо, уран и др. Поэтому такие экстрагенты применяют главным образом для выделения скандия из бедных (кислых или нейтральных) растворов с целью концентрирования. Из нейтрального раствора экстракция протекает по ка - тионообменному механизму за счет образования соли скандия с органической кислотой, растворимой в этой кислоте:
/iSc3+ + ЗН„Х ScnX3 +ЗлН+, (12.8)
Где Н„Х - алкилфосфорная кислота. Недостаток способа - реэкстрагировать скандий можно лишь плавиковой кислотой или раствором щелочи, в результате чего получается трудно фильтрующийся осадок ScF3 или Sc(OH)3.
Примеры переработки скандийсодержащего сырья
Переработка тортвейтита. Существуют следующие способы:
Кислотные (вскрытие HCl, H2S04, NH4HF2, плавиковой кислотой);
Щелочные (сплавление с NaOH, спекание с Na2C03);
Карбидный;
Хлорирование.
Кислотное вскрытие требует многократного повторения процесса. При высокотемпературном вскрытии щелочью или содой
Sc2Os • 2Si02 + 2Na2C03 = Sc203 + 2Na2Si03 + 2C02 (12.9)
Скандий остается после водного выщелачивания спека в остатке. Остаток растворяют в НС1; аммиаком осаждают гидроксид скандия. Растворяя гидроксид в 6 - 8 н. НС1 и экстрагируя эфиром, отделяют железо. Остальные примеси отделяют, экстрагируя эфиром роданид скандия. После отгонки эфира скандий осаждают в виде двойного тартрата с аммонием; извлечение равно 96 %.
Карбидный способ заключается в образовании карбидов в результате нагревания при 1800 - 2100 °С смеси минерала и древесного угля (соотношение 1:1,2). При обработке карбидов соляной кислотой в раствор переходят Sc, РЗЭ, Al, Fe, Ті, Zr. Карбид кремния соляная кислота почти не разлагает. Из раствора осаждают оксалат скандия, после повторного переосаждения получают богатый скандиевый концентрат, содержащий 10 % оксидов РЗЭ. Дальшейшую очистку ведут дробным осаждением гидроксидов и ионным обменом.
При переработке хлорированием тортвейтит в смеси с углем нагревают в токе хлора при 900 - 1000 °С. Различие температур кипения и конденсации хлоридов элементов, составляющих минерал, дает возможность их разделить в процессе конденсации. Хлориды Si, Zr, Al, Fe, Ті конденсируются ниже 400 °С; ScCl3 - при 600 - 900 °С; выход равен 87,5 %. В зоне хлорирования в плаве остаются хлориды РЗЭ.
Переработка уран-ториевых руд. По технологической схеме уранового завода в Солт-Лейк-Сити (США, штат Юта) получают растворы, в которых наряду с ураном содержится 0,001 г/л Sc203. При экстракции урана 0,1 М раствором до- децилфосфорной кислоты в керосине скандий переходит в эАтракт вместе с ураном, торием, титаном. Уран реэкстра - гируют Юн. НС1; скандий остается в органической фазе вместе с торием и титаном и концентрируется до 0,1 г/л Sc2Oj. Из экстрагента действием плавиковой кислоты осаждают фториды скандия и тория. Скандиево-ториевый кек, содержащий 10 % Sc203 и 20 % Th02, перерабатывают с целью 382 извлечения скандия. Фторидный кек вскрывают 15 %-ным раствором NaOH при 75 - 90 °С в течение 4 ч. Образовавшиеся гидроксиды обрабатывают соляной кислотой при 100 °С, устанавливая рН = 4; этим достигается очистка от Zr, Th, Ті, Si частично от Fe (ill), которые остаются в осадке. Из раствора щавелевой кислотой осаждают скандий. Оксалат скандия отфильтровывают, сушат, прокаливают.
Для получения Sc203 чистотой более 99,5 % дальнейшую очистку от примесей ведут экстракционным методом после растворения Sc203 в соляной кислоте. Экстрагируют диэти - ловым эфиром в присутствии NH4CNS. Из органической фазы скандий реэкстрагируют водой и аммиаком осаждают в составе гидроксида; прокаливанием при 700 °С гидроксид переводят в Sc203.
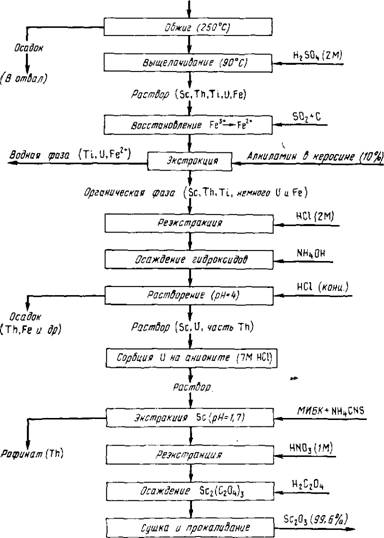
Для извлечения скандия вместе с ураном из сернокислых растворов после выщелачивания урановой руды (завод Порт - Пири, Австралия) используют Д2ЭГФК. После реэкстракции урана скандий накапливается в органической фазе. После содовой обработки экстракта получают кек, содержащий, %: Sc 0,14, Th 0,14, Ті 0,3, U3Og 24, Fe 38. Технологическая схема, приведенная на рис. 90, позволяет извлечь из кека 90 % Sc и получить оксид скандия чистотой 99,6 %.
По этой схеме кек вскрывают серной кислотой, скандий концентрируют, экстрагируя 10 %-ным раствором первичного алкиламина. При этом в экстаракт переходит 97 % Sc, 97 % Th, 55% Ті, 7 % U, 2 % Fe, предварительно Fe (III) восстанавливают S02 в присутствии активированного угля до Fe (II). После реэкстракции 2 н. НС1 соотношение скандия и примесей изменяется от 1:410 до 1:10. Дальнейшие операции предусматривают доочистку скандия. От урана скандий отделяют сорбцией на анионите, от тория - экстракцией рода - нидного комплекса скандия метилизобутилкетоном. Окончательно скандий выделяют в составе оксалата, который при прокаливании переходит в оксид.
Переработка титаномагнетитових концентратов. В титановом шлаке, получаемом в результате восстановительной плавки титаномагнетитов, содержится 0,005 -. 0,009 % скандия. При хлорировании шлаков большая часть скандия в составе хлорида концентрируется в отработанном расплаве титановых хлораторов (до 0,01 - 0,03% Sc203). Расплав обрабатывают раствором НС1 (20 - 40 г/л), выщелачивая скандий. Раствор
Ней
Ржс.90. Технологическая схема извлечения скандия из сернокислых урановых растворов отфильтровывают, корректируют содержание Fe (III), скандий экстрагируют 70 %-ным раствором ТБФ в керосине. Установлено, что FeCl3 способствует экстракции скандия ТБФ, однако повышение содержания FeCl3 в растворе приводит к загрязнению экстрагента. Кроме того, FeCl3 образует с ТБФ соединение, имеющее ограниченную растворимость в ТБФ, что приводит к загустеванию органической фазы, образованию эмульсии. Оптимальная концентрация FeCl3 в исходном растворе 7-12 г/л. Корректировка содержания FeCl3 перед экстракцией заключается в восстановлении Fe3+:
2FeCl3 + Mg = 2FeCl2 + MgCl2. (12.10)
Экстракт, обогащенный скандием, отмывают от примесей соляной кислотой (220 - 240 г/л), скандий реэкстра ги - руют с помощью 7%-ного раствора НС1. Из реэкстракта щавелевой кислотой осаждают оксалаты скандия и других элементов, пульпу фильтруют, осадок сушат и прокаливают при 700 °С, получая технический оксид скандия, содержащий 40 - 60% SCjOJ.
Технический оксид скандия растворяют в соляной кислоте, экстрагируют скандий с помощью ТБФ, из реэкстракта после многократных переосаждений иодатов [очистка от Th (IV) и Zr (IV)], гидроксидов и оксалатов получают товарный оксид скандия, содержащий более 99,9% Sc203.
Переработка отходов вольфрамового и оловянного производства. Отвальные кеки гидрометаллургической переработки вольфрамитовых концентратов состоят в основном из оксидов железа (25 - 35%) и марганца (25 - 35 %), содержат Nb, Та, Th, U, Sn РЗЭ и 0,15 - 0,50% Sc203. Для 'выделения скандия известны методы хлорирования, методы «Укрытия соляной или серной кислотой.
Более высокое извлечение скандия достигнуто в результате вскрытия кеков 98 %-ной серной кислотой при 220,°С (Т:Ж = 1:1,4) (рис.91). При водном выщелачивании в раствор вместе со Sc (0,2 - 0,3 г/л) переходят большая часть железа (15 - 25 г/л), марганца (15 - 20 г/л), Zr, Ті, Th, РЗЭ, Al и другие примеси. Железо и алюминий отделяют карбонатным методом, основанным на способности скандия образовывать комплексные карбонаты с содой и карбонатом аммония, растворимые в избытке соответствующего карбоната.
Золыррамитодый кек
Нг50ц
Сумыратизация (220°С)
Нг0
Выщелачивание
Осадок (Са, si)
(В отдал)
Роствор (Sc, Fe, Mn, Ti, Zr, Th, P33,Al, Be)
ІЧНцОН
Нейтрализация (рн=2) и кипячение
Осадак
(д отдал)
РастЗар NqjCQ, (10%-ный р-р) f і
Карбонатная очистка
1
1 ,
Осадок (Fe, Ca, Mn)
\
РастЗар (Sc)
(В отбал)
L
Падкисление (рН*-1) и кипячение
NHijOH
Осаждение Sc(0h)3
Осадок Sc (ОН),
Прокаливание (850°)
Т
Sc203 (<(0-70%~ный концентрат) Ржс.91. Технологическая схема извлечения скандия из вольфрамитовых кеков
Из раствора после подкисления НС1 до рН = 1 и кипячения осаждают Sc(OH)3, прибавляя концентрированный раствор аммиака. Прокаливая гидроксид, получают 40 - 70 %-ный Sc203. Дальнейшую очистку от примеси Ті, Zr, Th, РЗЭ проводят экстракционными методами с применением различных экстрагентов. Извлечение скандия составляет 80 - 88 %, чистота Sc203 99,99%.
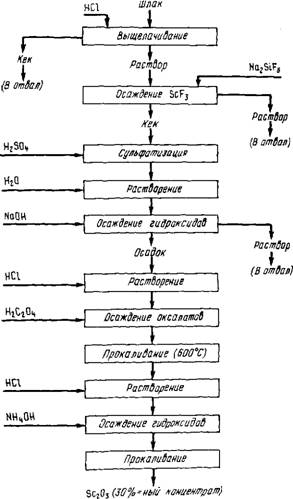
Переработка шлаков ферровольфромового и оловянного производства. Технологические схемы извлечения скандия из этих видов сырья разработаны в СССР. В результате пироме - таллургической переработки вольфрамитовых концентратов на ферровольфрам и переплавки оловосодержащих концентратов
Lnz03 (70%-ный концентрат)
Ржс.92. Технологическая схема извлечения скандия из шлаков производства ферровольфрама
Получают шлаки, в которых содержание скандия составляет 0,04 - 0,25%. Основные примеси - Fe, Si, Al, Ca, Ті, Mn, иногда Th, РЗЭ. Из обоих видов шлаков извлекать скандий предложено, обрабатывая измельченный материал 18 %-ной НС1 при 80 - 90 °С (Т:Ж = 1:1-5-5). В раствор извлекается до 96% Sc. Для отделения от основных количеств железа и марганца скандий осаждают в составе малорастворимого фторида путем введения в раствор кремнефторида натрия при рН=2. Осадок фторида скандия, содержащий Ca, Al, РЗЭ, Ті, Mn, обрабатывают серной кислотой, а затем проводят
Шлаков, S с, 0;
Водное выщелачивание. Часть кальция остается нерастворимой в составе CaS04. Для отделения алюминия и осадков кальция осаждают гидроксиды, вводя NaOH, при рН = 10. Указанные примеси остаются в растворе; в осадок вместе с Sc(OH)3 выделяются титан, марганец и другие примеси. Осадок гидроксидов растворяют в соляной кислоте и осаждают скандий щавелевой кислотой. Прокаливанием оксалаты переводят в оксиды. После растворения в НС1, осаждения гидроксидов, их прокаливания получают концентрат, содержащий 30% Sc203 и 70% (РЗЭ)203. Извлечение из шлака ~7б%. Схема процесса приведена на рис. 92.
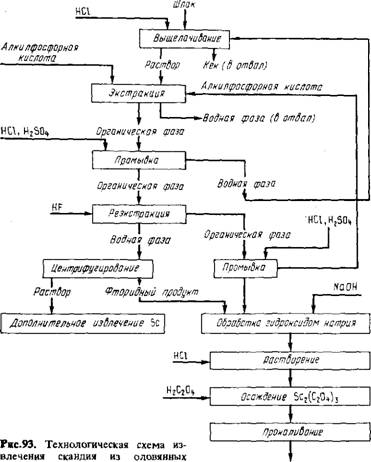
Разработан и проверен в промышленных условиях метод экстракционного концентрирования и очистки скандия, получаемого из шлаков от переплавки оловянных концентратов. Схема процесса приведена на рис. 93, После выщелачивания шлака соляной кислотой получают раствор, содержащий, г/л: Sc 0,2 - 1,0, Ті 0,8 - 3, Si 0,1 - 2, Са 11 - 30, Sn 0,1 - 1, Al 3,5, Mg 0,5 - 1,6, Zr до 2,6, Fe 0,5 - 2, W 0,03, HC1 110. Скандий экстрагируют 0,3 M Д2ЭГФК в керосине при соотношении объемов водной и органической фаз 10:1. Органическую фазу промывают 15%-нок НС1 при соотношении фаз 1:1, а затем 45%-ной H2S04 при таком же соотношении фаз. Скандий реэкстрагируют плавиковой кислотой. После отделения центрифугированием фторид обрабатывают раствором NaOH, переводя в Sc(OH)3; затем проводят оксалатную очистку. Прямое извлечение скандия - 75%.