СТРОЕНИЕ СТАЛИ
Чистое железо, 'В котором суммарное содержание различных примесей не превышает сотых долей процента, представляет собой мягкий металл (немного прочнее меди). Его получение не связано с особыми техническими трудностями. Однако для применения в котлострое - II її и и большинстве других отраслей промышленности в железо необходимо 'вводить добавки различны* веществ, улучшающих его свойства.
Железо, содержащее примерно до 2% углерода, называется сталью. В котлостроении применяют сталь с содержанием углерода около 0,1- 0,25%' (табл. 1).
Таблица I
| Марки стали | 20 | 15xm | 12хмф | 16гнм | 22к |
| Наименование | |||||
| Элементов | Содержание, % | ||||
| Углерод. . . . ■ . . | 0,17—0.25 | 0.09—0,16 | 0,08—0,15 | 0,12—0,18 | 0,19—0,26 |
| Марганец................ | 0,35—0,(55 | 0,40—0,70 | 0,4—0,7 | 0,8—1,1 | 0,75—1,00 |
| Кремний. ................... ............................ | 0.17—0.37 | 0,17—0,37 | 0,15—0,35 | 0,17—0,37 | 0,2—0,4 |
| Молибден................... | — | 0 40—0.60 | 0,25-0,35 | 0,40—0,55 | — |
| Хром.................................. | До 0,3 | 0.8—1.1 | 0,9—1,2 | До 0,3 | До 0.4 |
| Ванадий...................... | — | — | 0.15—0,3 | — | ■— |
| Никель............................ | — | До 0,3 | До 0 3 | 1.0—1,3 | До 0.3 |
| Медь................................... | До 0.25i | . 0,25 | „ 0,25 | 0,15-0,25 | > 0,3 |
| Сера.................................... | » 0,045 | , 0,04 | „ 0,04 | До 0,04 | . 0,045 |
| Фосфор.......................... | . 0.04 | . 0.04 | . 0,04 | . 0.035 | . 0,045 |
Кроме углерода, в котельных сталях обычно содержится небольшое количество марганца и кремния, а иногда и других металлов. В ничтожном количестве имеются и неудаленные остатки вредных примесей —- серы и фосфора.
При остывании расплавленной стали образуется твердый раствор примесей в железе, в котором сохраняется кристаллическая решетка железа. Кроме того, примеси, содержащиеся в стали, могут вступать в химическое взаимодействие с железом. При этом появляются новые соединения с собственной, иногда весьма сложной кристаллической решеткой.
Из различных химических соединений железа с другими веществами упомянем о его соединении с углеродом, известном под названием карбида железа или ц е - ментита. Химическая формула цементита Fe3C не отражает его сложного кристаллического строения, которое весьма трудно изобразить графически. Вокруг каждого атома углерода имеется по нескольку атомов железа. На рис. 10, чтобы не затемнять чертежа, показана только часть этих атомов. Цементит имеет высокую твердость (он царапает стекло).
Рассмотрим теперь вопрос о том, как образуется характерный для стали твердый раствор углерода в железе. Как уже упоминалось, растворение добавляемых
Веществ в основном металле происходит в период, когда металл находится в жидком состоянии. Когда металл затвердевает, атомы добавляемой примеси могут занять отдельные места (узлы) в кристаллической решетке, которые без них были бЫ1 заняты атомами самого железа. Иногда атомы добавляемой примеси размещаются в промежутках между атомами основного металла. В первом случае получается так называемый твердый раствор замещения, а во втором — твердый раствор внедрения.
Чтобы атом добавляемого вещества мог прочно занять место в «чужой» для него кристаллической решетке, необходимо несколько условий. Прежде всего требуется, чтобы диаметр этого атома соответствовал занимаемому им месту. В твердом растворе замещения диаметр «постороннего» атома должен мало отличаться от диаметра атома железа. В растворе же внедрения он должен иметь гораздо меньшие размеры.
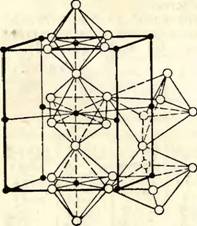
Рис. 10. Упрощенная схема кристаллической структуры цементита (светлые кружочки соответствуют атомам железа, черные — атомам углерода). |
Рассматривая твердый раствор углерода в железе, следует указать, что, не являясь металлом, углерод имеет кристаллическую решетку, которая значительно отличается от кристаллической решетки железа. Поэтому углерод не может образовать с железом твердого раетвоpa замещения. В альфа-железе затруднено образование твердого раствора. внедрения углерода. Дело в том, что в свободном состоянии атом углерода имеет диаметр 1,54 10~7 мм; диаметр же так называемой шоры, т. е. свободного пространства в кристаллической решетке альфа-железа, равен 0,62 10~7 мм. Поэтому в альфа-железе растворяется лишь ничтожное количество углерода, занимающего свободное пространство в местах, где в решетке нарушается правильное кристаллическое строение (см. рис. 3,6). Этим, вероятно, объясняется то, что максимальная растворимость углерода - по-разному оценивалась различными исследователями. Во всех случаях она измерялась сотыми долями процента.
Углерод гораздо легче растворяется в железе, нагретом до высокой температуры и имеющем гамма - структуру, так как в центре каждой ячейки кристаллической решетки гамма-железа имеется пора диаметром 1,02- 10"7 мм. При размещении в такой поре атома углерода происходит некоторое увеличение размеров соответствующих ячеек кристаллической решетки.
На рис. 4,а представлен полученный при помощи микроскопа фотоснимок поверхности котельной стали марки 20, тщательно отшлифованной и протравленной кислотой. Как видно из фотоснимка, сталь состоит из отдельных светлых зерен (кристаллитов) альфа-железа и тем- ны'х зерен. Зерна альфа-железа в стали называются ферритом (по-латыни: «феррум»—железо), а темные зерна — перлитом (от слова «перламутр», на который они похожи в чистом виде).
При очень большом увеличении можно обнаружить, что перлит имеет. вид чередующихся темных и светлых полосок Исследования подтверждают неравномерность его структуры: перлит состоит из чередующихся слоев альфа-железа и цементита, т. е. из слоев чистого железа и химического соединения железа с углеродом.
Чем больше углерода в стали, тем больше перлита образуется при ее остывании. Металловеды по фотографии микроструктуры стали могут довольно точно определить содержание в ней углерода.
Растворенные элементы могут перемещаться в твердой стали на некоторое расстояние, которое хотя и представляется ничтожным в наших обычных масштабах, все же весьма велико по сравнению с размерами самих атомов. Такое перемещение (диффузия) атомов ускоряется с повышением температуры металла. Диффузия и самодиффузия (перемещение атомов самого железа) в стали лежат в основе многих процессов, уменьшающих прочность стальных деталей, которые работают длительное время при высокой температуре.
4. ВЛИЯНИЕ ЛЕГИРОВАНИЯ
Качественные показатели котельной стали могут ощутимо измениться даже при ничтожной, исчисляемой долями процента добавке различных элементов. Это свойство добавок нельзя было бы объяснить, если бы добавляемые вещества полностью и равномерно растворялись в основном металле. Однако марганец, хром, молибден, вольфрам, ванадий, титан и другие металлы лишь частично переходят в твердый раствор. Значительный процент каждого из этих элементов образует химические соединения с углеродом или другими примесями.
Наибольшее значение имеет взаимодействие добавляемых металлов с углеродом. Эти химические соединения (карбиды) подобно карбиду самого железа (цементиту) увеличивают прочность стали. Отдельные добавки улучшают и другие свойства стали: повышают ее жаропрочность (т. е. прочность при высокой температуре), противодействуют коррозии и т. и.
В зависимости от содержания и количества этих добавок котельные стали делят на следующие две группы: углеродистые, в которых, кроме углерода, имеется определенное количество марганца и кремния, и легированные, в которых содержится еще и некоторое количество хрома, молибдена, никеля и других металлов.
Ниже коротко рассмотрено влияние на свойства стали .элементов, являющихся постоянными примесями. Кроме того, сведения о влиянии некоторых элементов приведены в табл. 2.
Влияние углерода. С увеличением содержания в стали углерода возрастает количество перлита (а следовательно, и цементита). Сталь при этом становится более прочной и менее пластичной. Высокая прочность является весьма полезным свойством металла; поэтому применение сортов стали с пониженным содержанием углерода нежелательно. Вместе с тем нежелательно и чрезмерно
Таблица 2
|
Большое содержание углерода в стали, так как слишком твердый и сравнительно мало пластичный металл хуже сопротивляется различным механическим деформациям, возникающим, например, три защемлении экранных труб при растопке котла или неравномерном нагревании барабана в период растопки. Кроме того, высокое содержание углерода в стали отрицательно сказывается на прочности сварных соединений.
Для изготовления поверхностей нагрева котла очень широко применяется углеродистая сталь марки 20, в которой содержание углерода допускается не более 0,25%. Несколько большее содержание углерода допускается в стали, из которой изготовляют каркас и обшивку котла, площадки обслуживания и другие конструкции, не подверженные нагреванию до высокой температуры.
В легированных сталях углерод обычно содержится в еще меньшем количестве, чем в стали марки 20. Например, в применяемой для изготовления пароперегревателей современных котлов стали марки 12ХМФ содержание углерода не должно превышать 0,15%'.
Влияние марганца. Вопрос о выборе оптимального содержания марганца в котельных сталях до сих пор окончательно не решен. Марганец подобно углероду повышает прочность стали и несколько уменьшает ее пластичность. Кроме того, при плавке стали в мартеновской печи марганец способствует очистке металла от серы, с которой он образует легко удаляемый шлак. Отрицательное действие марганца заключается в уменьшении
2 М. В. Меіікляр. J j
/
Теплопроводности стали, вследствие чего, например, в барабане котла более вероятно возникновение треїлин при местном нагреве или охлаждении какого-либо его участка. В экранах это может повести к увеличению разности температур между частями труб, обращенными е топку и к обмуровке.
На отдельных электростанциях работают шаровые котльи, у которых барабаны изготовлены из стали, содержащей более I %' марганца. Все же добавку марганца в сталь обычно ограничивают долями, процента. Применяемая для изготовления барабанов сталь марки 22К содержит марганца 0,75—1%. Еще меньше марганца содержит сталь марки 20. В большинстве легированных сталей также содержится лишь небольшое количество марганца.
Влияние кремния. При плавке в металлургической печи кремний, как и марганец, применяется для раскисления: соединяясь с растворенным в стали кислородом, он образует легко удаляемые шлаки, всплывающие на поверхность жидкого металла. Почти во всех котельных сталях содержится небольшое количество кремния, остающегося после раскисления, но иногда содержание его увеличивают для повышения жаростойкости ста - л и, т. е. для повышения максимальной температуры, при которой не приходится опасаться интенсивного образования окалины.
На свойства стали кремний влияет аналогично углероду и марганцу: при его добавлении увеличивается прочность и понижается пластичность.
5. АУСТЕНИТНАЯ СТАЛЬ
Особые результаты дает добавка в сталь никеля, имеющего такой же тип кристаллической решетки, как и гамма-железо. При высокой температуре, когда у обоих металлов структура кристаллической решетки одинакова, никель образует в стали устойчивый твердый раствор замещения. При охлаждении никель стремится сохранить собственное кристаллическое строение"и тормозит перестройку гамма-железа в структуру альфа - железа. Если добавить в сталь до 26% никеля, гамма - структура сохраняется при охлаждении стали до комнатной температуры. 18
| Углеродистое Стало с Кромоникелшя Сталь с 5%
Сталь хрома оустенитнав сталь никеля
При температуре 500°С |
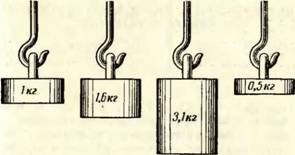
Рис. П. Сравнение нагрузки, которая может бы"ь допущена для стержней, изготовленных из разных сортов стали и нагргтых до температуры 500° С [Л. 12;. |
Присадка никеля не только не увеличивает прочности стали 'при нагреве до высокой температуры, но даже уменьшает ее по сравнению с углеродистой сталью (рис. 11). Поэтому целесообразно вместе с никелем в сталь вводить хром, при наличии которого уменьшается количество никеля, необходимого для сохранения гамма-структуры стали.
Сталь, сохраняющую гамма-структуру при обычной температуре, называют аустенитной в отличие от перлитной стали, у которой при охлаждении происходит описанная выше перестройка кристаллической решетки. В настоящее время аустенитную сталь широко применяют в различных отраслях техники, начиная от строительства кислотоупорных сосудов для химической промышленности до художественной отделки зданий (например, на станции «Маяковская» московского метро). В энергетике из аустенитной стали делают элементы оборудования, работающие при наиболее вы - 2* 19
сокои температуре, в частности выходную часть пароперегревателя парового котла.
У большинства котельных аустенитных сталей суммарное содержание хрома и никеля составляет 30% общего веса металла (табл. 3). Таким образом, количество легирующих добавок в аустенитной стали (во много раз больше, чем, например, в перлитной стали марки 12ХМФ, в которой суммарное содержание марганца, хрома, молибдена и ванадия не превышает 3%.
Аустенитная сталь стоит в 2—5 раз дороже хромомо- либденовой и в 5—10 раз дороже, чем обычная углеродистая сталь. Поэтому расход аустенитной стали стремятся по возможности сократить. Однако применение аустенитной стали для труб пароперегревателя позволяет повысить температуру перегретого пара, благодаря чему возрастает экономичность электростанций и снижается стоимость вырабатываемой на них электроэнергии.
В кристаллической решетке гамма-железа атомы «упакованы» более плотно, чем в решетке альфа-железа, поэтому при высокой температуре в аустенитной стали в меньшей мере, чем в перлитной, развиваются разуп - рочняющие процессы. К тому же в аустенитной стали почти весь углерод весьма прочно химически соединен с легирующими элементами. Кроме высокой жаропрочности (прочности при высокой температуре), аустенитная сталь должна иметь и значительную жаростойкость (сопротивление окислению при высокой температуре) аустенитной стали. 20
Начальная стадия процесса окисления заключается в химическом соединении кислорода с поверхностным слоем металла. В дальнейшем на поверхности стали образуется пленка окислов и процесс окисления может продолжаться только в случае систематического разрушения этой пленки или при прохождении кислорода через нее. Весьма прочную и в то же время непроницаемую для кислорода пленку образуют окислы хрома; поэтому добавка в сталь большого количества хрома не только позволяет увеличить ее прочность при высокой температуре, но и обеспечить высокую жаростойкость.
Кроме никеля и хрома, в аустенитную сталь вводят небольшое количество других легирующих добавок, еще более улучшающих ее характеристики. К таким добавкам обычно относятся титан, вольфрам и ниобий.
6. СПОСОБЫ ПОВЫШЕНИЯ ЖАРОПРОЧНОСТИ КОТЕЛЬНЫХ СТАЛЕЙ
В настоящее время имеется тенденция дальнейшего повышения температуры перегретого пара на электростанциях. Необходимое для этого увеличение жаропрочности. металла может быть достигнуто различными способами.
Жаропрочность котельной стали можно повысить некоторыми другими способами легирования (например, добавкой бора или редкоземельных элементов).
Дальнейшее значительное повышение жаропрочности элементов котла может быть достигнуто применением для их изготовления различных сплавов, в которые основным металлом является не железо, а кобальт и никель. Еще более высокой жаропрочностью обладают сплавы, в основе которых лежит тугоплавкий молибден. Внедрению этих сплавов в котлостроение препятствует прежде всего их высокая стоимость (кобальт примерно в 10 раз дороже хрома и никеля).
При проектировании современных мощных электростанций всегда определяют экономическую целесообразность повышения стоимости оборудования за счет применения отдельных сортов жаропрочной стали. Это повышение стоимости оправдывается тогда, когда оно перекрывается экономией топлива, получаемой благодаря применению высококачественных металлов.