КОТЕЛЬНЫЕ УСТАНОВКИ И ПАРОГЕНЕРАТОРЫ
Электрохимическая коррозия в водяном тракте энергетического блока
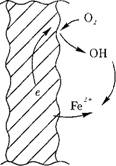
Как уже рассматривалось в предыдущем параграфе, электрохимическая коррозия связана с возникновением микрогальваничсских элементов на границе металл-рабочее тело. Анодный и катодный процессы могут протекать поочередно на одном и том же месте, или, в большинстве случаев, они разделены пространственно (рис. 12.44).
16 Котельные установки
Анодный процесс — окисление металла, в результате чего ион металла Fe2+ переходит в воду, а электроны накапливаются в металле:
Fe = Fe2+ 4- 2е~.
На катоде происходит ассимиляция (поглощение) электронов деполяризаторами, в качестве которых могут выступать Н+ или 02:
2Н+4-2е~ =Н2; 02 4-2Н20 4-4е" = 40Н~.
Соответственно данный процесс называют коррозией с водородной или кислородной деполяризацией.
Водородная деполяризация характерна для кислых растворов. В нейтральных и щелочных средах основную роль играет кислородная деполяризация. Деполяризатор уменьшает поляризацию коррозионного элемента, т. е. увеличивает ЭДС и скорость коррозии.
В результате того, что деполяризаторами могут быть не только кислород и водород, но и другие примеси воды, что ионы железа вступают в реакции с рядом веществ в растворе и удаляются от электрода, процесс коррозии может быть незатухающим. Для снижения скорости коррозии следует уменьшать концентрацию деполяризаторов и других веществ в растворе.
Одним из эффективных способов уменьшения скорости электрохимической коррозии является создание на поверхности металла защитной пленки.
Механизм образования в зоне пассивации защитной оксидной пленки зависит от температуры.
При температуре ниже 200°С ион железа, перешедший из металла в теплоноситель на анодном участке, взаимодействует с молекулами воды:
3Fe2+ + 4Н20 - Fe304 4- 2е" 4- 8Hf; 8Н+ 4- 4е~ 4- 202 = 4Н20.
Для протекания этих реакций должно быть определенное количество кислорода в воде: при рН=7 необходима концентрация кислорода порядка 400 мкг/кг, при рН> 7 - значительно меньше.
|
Рис. 12.44. Электродные процессы на границе «металл — водный теплоноситель». |
Следовательно, чтобы снизить скорость коррозии при температуре менее 200°С, в конденсатном тракте желательно иметь величину рН порядка 7 и удалять кислород.
Образовавшийся в объеме теплоносителя магнетит частично кристаллизуется и адсорбируется на поверхности металла. Оксидная пленка на поверхности при этом получается недостаточно плотной и прочной, она не защищает полностью металл от протекания коррозии.
В питательном тракте (группа ПВД), экономайзере, испарительном участке при докритичееком давлении, в топочных экранах котлов сверхкритического давления, т. е. в зонах, где температура свыше 200°С, образование защитной пленки на поверхности металла протекает одновременно по двум механизмам — химической и электрохимической коррозии.
В поверхностном слое металла происходит окисление железа по уравнению химической реакции (коррозии)
3Fe + 4Н20 - Fe304 + 4Н2.
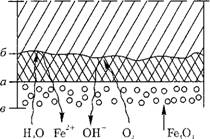
Слой магнетита растет от начальной границы металла «а» (рис. 12.45) внутрь основного металла, образуя так называемый топотактический слой (внутренний слой) «б» защитной пленки.
|
Рис. 12.45. Образование двухслойной оксидной пленки на поверхности металла. |
Образовавшиеся в результате электрохимической коррозии ионы Fe2+ диффундируют через защитную пленку и в растворе реагируют с гидрок - сильными ионами, образовавшимися на катодном участке:
Fe2+ +20Н" =Fe(OH)2.
Это соединение превращается в магнетит (по реакции Шикорра)
3Fe(OH)2 - Fe304 + Н2 + 2Н20.
Образовавшийся в растворе магнетит кристаллизуется и адсорбируется на поверхности и образует менее плотный внешний слой (эпитактический слой) «в» защитной пленки (рис. 12.45).
Таким образом, при высокой температуре защитная оксидная пленка состоит из двух слоев: внутреннего слоя, по своим характеристикам (плотность, теплопроводность) близкого к основному металлу, и внешнего слоя, состоящего из более или менее плотно упакованных кристаллов магнетита, пропитанных теплоносителем, плотность этого слоя и теплопроводность его меньше основного металла и внутреннего слоя.
* Для сохранения защитной оксидной пленки необходимо: соблюдать высокое качество питательной и котловой воды; очищать паровые котлы от накипи, отложений, шлака; во время останова парового котла и другого оборудования подвергать его консервации; при водной промывке при гидравлических испытаниях использовать деаэрированную, обессоленную и не содержащую взвешенных примесей воду.