ИЗ ЧЕГО СОСТОИТ ВСЕЛЕННАЯ (ЗАКОН МЕНДЕЛЕЕВА)
КАК БЫЛ ПОДТВЕРЖДЁН ЗАКОН МЕНДЕЛЕЕВА
ОЛсентября 1875 года на заседании Парижской Акаде - мии наук было зачитано письмо французского химика Лекок-де-Буабодрана об открытии им нового химического элемента — галлия. Галлий был обнаружен в минерале цинковая обманка при помощи спектрального анализа. Первые же испытания нового элемента показали, что по своим свойствам он очень похож на алюминий.
Это был предсказанный Д. И. Менделеевым в 1871 году экаалюминий.
5 ноября 1875 года в протокол заседания русского химического общества заносится: «Менделеев обратил внимание на то, что элемент, открытый недавно Лекок-де- Буабодраном..., совпадает с долженствующим существовать зкаалюминием, свойства которого указаны четыре года назад и выведены Менделеевым на основании периодического закона. Если галлий тождественен с зкаалюминием, то он будет иметь атомный вес 63, плотность 5,9...».
Все предсказанные Менделеевым свойства нового элемента подтвердились!
Интересно отметить, что Лекок-де-Буабодран на первых порах неверно определил удельный вес галлия. Д. И. Менделеев тут же написал в Париж письмо, указав, что Буабодран ошибся. Французский химик повторил опыт и убедился, что Менделеев прав, — удельный вес галлия оказался равным, как и предсказывал русский химик, около 6—5,94. «Я думаю, — писал он, — нет необходимости настаивать на огромном значении подтверждения теоретических выводов Менделеева относительно плотности галлия».
В 1880 году было получено новое подтверждение закона Менделеева: в Швеции был открыт экабор — скандий (Бс). Нильсон, открывший этот новый элемент, писал: «Не остаётся никакого сомнения, что в скандии открыт экабор... Так подтверждаются самым наглядным образом мысли русского химика, позволившие не только предвидеть существование названного простого тела, но и наперёд указать его важнейшие свойства».
Третий из предсказанных Д. И. Менделеевым в 1871 году элементов — экакремний — германий — был найден Винклером в 1886 году. Свойства нового элемента почти в точности совпали с предсказанными (см. таблицу).
|
Таблица совпадения некоторых свойств германия, предсказанных Д. И. Менделеевым и найденных на опыте
|
«Вряд ли может существовать более яркое доказательство справедливости учения о периодичности элементов...», — писал о своём открытии Винклер.
Так блестяще был подтверждён великий закон Менделеева.
«Писавши в 1871 году статью о приложении периодического закона к определению свойств ещё не открытых элементов, — писал Д. И. Менделеев, — я не думал, что доживу до оправдания этого следствия периодического закона, но действительность ответила иначе».
Теперь великое открытие русского химика было признано во всём мире.
Оценивая это открытие, Ф. Энгельс писал, что Менделеев совершил научный подвиг.
Закон Менделеева ещё раз подтверждает одно из основных положений диалектического материализма.
Товарищ Сталин в своей работе «Анархизм и социализм» указывает, что «...мелкие, количественные, изменения, в конце концов, приводят к большим, каче -
|
Периоды |
Ряды |
ГРУППЫ |
|||||
|
О |
О |
63 |
|||||
|
1 |
1 |
Н 1 Водород 1,0080 |
|||||
|
2 |
11 |
Ы з Литий 6,940 |
Вв 4 £>орилли$ 9,03 |
Б в Вор 10,83 |
В с Углпрод 13,010 |
7 N Азот 14,008 |
8 0 Кислород 16,000 |
|
3 |
Ш |
Ыа п Натрий аз,99? |
Мд 12 Магний 34,33 |
13 А1 Алюминий 36,97 |
14 НремниО ^8,06 |
16 р Фосфор Э0,&8 |
16 э С&ря 32,066 |
|
4 |
IV |
К 19 Налай 39,096 |
Са го Мольций 40,08 |
ЗС 2) Сниндий 40,10 |
"П 22 Титан 47,90 |
V 23 Ванадий 60,96 |
Сг 24 Хром 63,01 |
|
V |
29 Си Медь Ез, э4 |
Зо 2.п Цинн 60,38 |
Э1 ва Галлий 6 9,?2 |
32 бе Гъряаний 73,60 |
Зз Ав МышЬйк 74,91 |
34 вв Сбл&н 78,96 |
|
|
5 |
VI |
РЬ 37 Рубидий 86,48 |
Зг 38 Стронций В7твз |
У 39 Иттрий 88,93 |
Гг 40 Цирноний 91,22 |
N6 4! Ниобий 93,91 |
МО 42 Молибден 96,90 |
|
VII |
4? Ад Свр*6ро 107,88 |
48 Ос1 Кадмий 113,41 |
49 1п Индий 114,76 |
БО Зп Слава 118+70 |
51 ЭЬ Сурьми 121,76 |
52 Те Теллур 137,61 |
|
|
* |
VIII |
С8 65 Цезий 1эа>э1 |
Ва бв Варий 137,86 |
-& 67 й Лен тан 138,03 |
Ж 72 ГафноО 178,6 |
Та тз Тантал 180,08 |
Л/ 74 Вояьфрал/ 183,93 |
|
IX |
79 Аи ; Золото 197,3 |
Во Нд Ртуть 300,81 |
81 Т1 Таллий 304,3» |
82 РЬ Свинец 307,31 |
83 В1 Висмут 309,00 |
84 РО Полоний 310 |
|
|
К [7 1 |
X |
Рг 67 Франций 323 |
Ра ев Радий 336,05 |
АС 89** Аптиний 337,00 |
(ТИ) |
(Ра) |
(и) |
|
| # БВ-71 |Ланшмдь |
Се 68 ■ Церий 140,13 |
Рг 69 140,93 |
N с! во Р НооВим 144,37 |
Р^Пв) Протятий 147 |
Зт 62 Самарий 160,43 |
Ей бз Еяроаий 163,0 |
6С1 64 Г 166,9 |
ТЬ 65 Тербий 169,3 |
|
| *• 90-98 «АкТШШДЫ |
ТЬ во Торий. 932,19 | |
Ра 91 Ъротлнтт [231 |
И 92 1№ Урон 238,07 |
Ыр 93 Нъътуний 337 |
Ри 94 Алулгоний 339 |
Агп 96 Ам*риц</ь 341 |
Ст 96 Нюрий 343 |
Вк 97 Вернлий |
Рис. 8. Современная перио
![]()
|
Но а Ґ9»и0 4.003 |
![]()
ЭЛЕМЕНТО В уііу VIII
(^СПОАОМІММ
Эаоктрсмоа по орбитам
• атомах иуаааои группы: саом а перкл«» удаааииа ы ядра
|
Аг їв Лрго* 99,044 |
|
МП 75 Мср/а*9ц М, оа |
|
Со 57 Кобо* ал» ЬИ, 1*4 |
|
Кг зв Нриатс* |
|
Зб Вг Вро» 79.9*6 |
|
ІГ 77 Ир^д*» |
|
17 СІ Хж»р ».<67 |
|
Ре эв К»1Ж 66.ВЄ |
|
18 |
|
1в |
|
Хе 64 Нсгнсм 131,3 |
|
Рі 78 /7 ЙО’ПЧМЩ »®%,г 1 |
|
Р? П ей 333 |
|
1332 |
|
16 |
|
63 и Под 136,95 |
|
Ре 76 Рщмой 186.31 |
|
Оз 76 Остий <»0,2 |
|
«3,7 |
|
РЗ 46 ПшвмоЬой 106.7 |
|
РЬ 46 Рлди! 109.91 |
|
Тс 43 7а««#«<г0 |
|
Ри ♦< Рутений 101,7 |
|
|
||
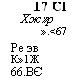 |
|||
|
|||
|
|||
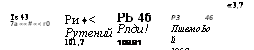 |
|||
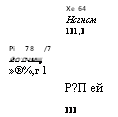 |
|||
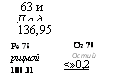 |
|||
|
|||
|
Оу 66 Ав<»р*лвы 162.46 |
Но 67 Го я ьмиИ 164,94 |
Ег ее Эрбид 167,3 |
Ти ьв Тумы» 169,4 |
ЇЬ 70 Мтторбай 173,04 |
1.и 71 /ютовий 174,99 |
|
С< ее Н*»лфг'-** |
|
Сямао* У |
|
Порадяоаый Номер |
![]()
 Дическая система элементов.
Дическая система элементов.
Ственным, изменениям... Этот закон в равной мере имеет силу в истории природы. Менделеевская „периодическая система элементов" ясно показывает, какое большое значение в истории природы имеет возникновение качественных изменений из изменений количественных».
Столь же блестяще подтвердились и все другие научные предсказания Д. И. Менделеева. Всего им было предсказано существование одиннадцати химических элементов, в том числе открытие ряда тяжёлых элементов — полония, рения, протактиния и других.
В конце прошлого века были открыты упомянутые нами ранее инертные, недеятельные газы — аргон и другие. По своим свойствам эти газы отличались от всех известных элементов. Они не давали никаких химических соединений с другими элементами (в наше время некоторые из таких газов — аргон и неон — используются в газосветных трубках — лампах «холодного света»).
Встал вопрос: куда поместить их в таблице Менделеева? Затруднение было разрешено просто. Инертные газы — всего их было открыто шесть — были помещены в отдельную, нулевую группу (см. современную периодическую систему элементов на стр. 40). Заканчивая периоды, эти газы как бы закрывают разрыв в свойствах между последним в периоде наиболее активным металлоидом и первым в следующем периоде наиболее активным металлом. Что в природе должны существовать эти элементы, об этом говорил сам Менделеев. В 1870 году он писал, что заметно отсутствие элементов между водородом и литием и между натрием и фтором. Именно на этих местах теперь и стоят инертные газы гелий и неон.
Существование в природе инертных газов предсказал и русский учёный-революционер Н. А. Морозов. В своей книге «Периодические системы строения вещества», написанной в царской тюрьме, он задолго до открытия инертных газов поместил периодическую таблицу с нулевой группой и указал атомные веса неоткрытых химических элементов этой группы.
Современная периодическая система химических элементов приведена на рисунке 8.
Как видно из этого рисунка, все элементы расположены в десяти горизонтальных рядах, составляющих семь периодов — коротких и длинных.
Периоды заключают в себе разное число элементов — в первом периоде—всего два элемента — водород и гелий; во втором и третьем—по восемь элементов; в четвёртом и пятом — по восемнадцать; в шестом, самом большом периоде таблицы, заключено тридцать два химических элемента; здесь в клетке под № 57 помещается сразу
15 элементов — от Лантана до лютеция, очень похожих по химическим свойствам друг на друга; это — так называемые «редкоземельные» элементы или лантаниды; они выделяются обычно в отдельную группу (см. внизу таблицы на рис. 8); и, наконец, последний, седьмой, неполный период включает в себя двенадцать химических элементов; сюда входят особой группой так называемые актиниды, в числе которых находятся и все элементы с атомным весом, большим атомного веса урана; начинается этот период с искусственно полученного элемента франция и обрывается также искусственно полученным калифорнием.
Всего до настоящего времени получено искусственно 10 химических элементов; это — технеций (№ 43), прометий (№ 61), астатин (№ 85), франций (№ 87) и шесть заурановых элементов (см. об них далее, стр. 59).
Каждый из первых шести периодов заканчивается инертным газом.
Расположение элементов в горизонтальных рядах таково, что сходные друг с другом химические элементы располагаются в одних и тех же вертикальных столбцах — группах. Всего групп в таблице девять.
* *
*
Великий закон Менделеева ответил на вопрос, из каких элементов состоит мир. «Кирпичами» мироздания являются не элементы-свойства учёных древнего мира, не «философские» сера и ртуть алхимиков, а вполне материальные, химические элементы, объединённые в единую систему.
Периодический закон ясно показывал, какие ещё могут быть открыты химические элементы. Слепым поискам неизвестных простых тел природы был положен конец. - Бессмысленно было искать теперь, скажем, неизвестный щелочной элемент между литием и натрием, ибо такого элемента в природе нет.
Прекрасно понимая всё исключительное значение периодического закона как объективного закона природы, Д. И. Менделеев писал: «Он (т. е. закон) рисуется ныне в виде новой, отчасти только раскрытой, глубокой тайны природы... и я, как русский, горжусь тем, что участвовал в его установлении».
Закон Менделеева явился могучим помощником человека в познании природы.
И в первую очередь он показал материальное единство Вселенной.