Теория водородного атома
Спектральные серии и уровни энергии.
Закономерности в атомных спектрах.
Бальмер проводил исследование спектров излучения атомов водорода. Экспериментально было установлено, что атомы водорода (как и атомы других элементов) излучают электромагнитные волны строго определённых частот, другими словами, спектр атома водорода состоит из спектральных линий, длины волн которых строго определены. При этом оказалось, что величину, обратную длине волны спектральной линии, можно рассчитать, как разность, некоторых двух величин, которые называются спектральными термами:
1/λ = Тn1 – Tn2 (1)
Для атома водорода терм можно записать следующим образом:
Tn= Rн/ n2 (2)
где n = 1,2,3... принимает ряд положительных значений,
Rh - постоянная Ридберга, численно равная:
Rh = (1,097373177 ± 0,000000083) 107м -1.
Тогда длину волны любой спектральной линии водорода можно рассчитать по обобщенной Формуле Бальмера: 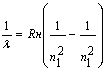 (3)
(3)
(n1 = 1,2,3...) (n2=n1, n1+1, n1+2 …)
Длины волн, рассчитанные по формуле (3), совпали с экспериментально измеренными величинами.