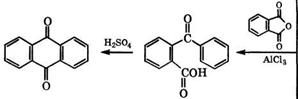
Ароматические углеводороды: Выделение, применение, рынок
ПОЛУЧЕНИЕ ЭТИЛБЕНЗОЛА
Основной способ получения этилбензола - алкилирование бензола этиленом. В качестве катализаторов процесса широко использовались А1С13, Н3Р04 на кизельгуре, BF3 на модифицированном А1203[1].
Однако в последние годы наибольший интерес исследователей привлекли процессы алкилирования с использованием цеолитов, более активных и селективных по сравнению с ранее применявшимися катализаторами. Так, установлено, что цеолит Р более активен и селективен, чем Н3Р04 и цеолит Y при получении этилбензола и кумола [2]. С увеличением соотношения Si/Al от 14 до 35, а также при модифицировании цеолита Р бором селективность образования этилбензола и кумола снижается. Степень конверсии повышается с уменьшением размеров частиц катализатора. При 170 С, давлении 3.5 МПа, мольном соотношении бензол/этилен, равном 5, при конверсии этилена 100 % селективность по этилбензолу на цеолите Р (Si/Al — 14) равна
99.1 %, в то время как на цеолите Y - лишь 92.3 %.
На использование цеолита Р в качестве катализатора процессов алкилирования аренов С6-С8 олефинами С2-С4 получен ряд патентов [3-7]. Так, при алкилировании бензола этиленом в мольном соотношении 7 : 1 на катализаторе состава 80 % (мае.) цеолита Р и 20 % (мае.) А1203 при 163 С, избыточном давлении 3.2 МПа, объемной скорости 4.6 ч 1 конверсия этилена равна 100 %, а состав продуктов алкилирования следующий, % (мае.): этилбензол - 91.1, диэтил бензолы - 7.9, триэтилбензолы - 0.3, прочие - 0.7 [3].
Для снижения выхода побочно образующегося 1,1-дифенил- этана предложено разбавлять смесь реагентов триэтилбензола - ми [8].
|
Сн=сн2 |
![]()
|
-н2 |
![]()
![]()
|
С№=СН2 |
![]()
СН2=СН2
С6н5св=сн2 - СбН5СН2СН3
-н2
Сн2=снсн3
СН3ССН3 + С6Н5ОН С6Н5СН(СНз)2 ------------------------
& V----------------------------
Н2
|
|
|
СН2СН3 |
|
СвН5СН2СНз |
Сн2=с=сн2
(СНз~С5СиГ С6Н5С(СН3)=СН2
А1С13—СиС12
|
Сн2=ст1 |
|
С6Н5СН(С^Ж |
|
Ю |
|
СН2=СНСН2С1 |
|
N00 |
|
С12 |
|
НИОз Н2304 |
|
Нмо*. |
|
C6H5N02 |
|
Н2304 N^ + 0*2 |
|
Сн2о |
|
N02 |
|
НС1, 7,пСъ СС14 |
|
С61^Н2 |
|
С6Н5СН2С№=СН2 |
|
С6Н5СН2С1 |
|
С6Н5С1 |
|
Н,0 |
 |
![]()
|
А1С13 Со |
|
НС1, А1С13 СН3С0С1 |
|
А1С1, |
|
|
 |
|
|
|
|
|
|
|
|
,нО“он |
|
О |
|
Сн2о |
|
Н2Э04 |
|
ЭОзСКОН) СеН^ОгС! Вг2 |
|
С6Н5802С1 |
|
СбНбЭОгСбНб |
|
СвНбВг |
|
|
 |
|
 |
|
|
|
|
|
|
Н2С—сн2 о |
|
А1С13 О *5° СГС1 |
|
|||
 |
|||
|
|||
|
|||
|
|||
|
|||
|
|||
|
|
||
|
|||
|
|||
|
|||
|
|||
|
|||
![]()
Рис. 6. Направления использования бензола
Для снижения скорости дезактивации и увеличения срока службы цеолита Я предложено продувать оборудование и сырье азотом для удаления примесей растворенного кислорода [7].
При алкилировании бензола этиленом на цеолите Я с отношением Si02/Al203= 70-200 при 400 С, избыточном давлении
2.1 МПа, объемной скорости 12 ч-1 и содержании этилена в смеси с азотом 30% (мол.) конверсия этилена 96.7%, бензола -
16.3 %, селективность образования этилбензола 85.8 % и ди- этилбензолов - 9.01 % [5].
Результаты сравнительного исследования эффективности широкопористого Я-цеолита и среднепористого цеолита типа H-ZSM-5 с такой же кислотностью при алкилировании бензола и толуола этиленом или метанолом представлены в работе [9]. Отмечается, что цеолит H-ZSM-5 более активен и селективен по этилбензолу при алкилировании бензола этиленом. Так, при 350 С, мольном соотношении бензол/этилен = 1, скорости подачи сырья 3.7 ч-1 конверсия этилена на H-ZSM-5 составляет 94.8 %, конверсия бензола - 65.7 %, а на цеолите Я при тех же условиях - 57.8 и
35.7 %; максимальный выход этилбензола на H-ZSM-5 - около 57 % , а на цеолите Я - лишь 34 %.
Около 90 % новых установок синтеза этилбензола основано на газофазном алкилировании бензола этиленом с использованием цеолита ZSM-5 [10].
Жидкофазное этилирование бензола с использованием кислотных форм цеолита, например Н-формы цеолита марки МСМ - 22, предложено фирмой "Mobil Oil Corp." [11]. Отмечается, что в процессе образуется мало полиэтилбензолов и ксилолов (менее 500 ррш). Катализатор нашел применение в промышленности.
Еще более активен и селективен по сравнению с цеолитом МСМ-22 новый алюмосиликатный цеолит марки МСМ-49 [12]. Так, при использовании цеолита МСМ-49 формулы X203 Y02 (X = Al, В, Fe, Ga; Y = Si, Ti, Ge; n = 2-35) с мольным соотношением Si/Al < 20 в результате алкилирования бензола этиленом в мольном соотношении (0.5-3.3) : 1 при 160-320 С, давлении 3.4 МПа получен катализат состава, %(мол.): этилбен - зол - 95.3, диэтилбензолы - 4.5, триэтилбензолы - 0.1 [13]. Тот же катализатор - цеолит МСМ-49 запатентован для жидкофазного алкилирования бензола, содержащегося в катализате ри - форминга бензиновой фракции, олефинами С2-С5 для снижения содержания бензола в бензине в соответствии с экологическими требованиями [14].
Алкилирование бензола и других аренов олефинами С2-С5 предложено также проводить с использованием цеолита МСМ-36 с мольным соотношением Si02/Al203>5 [15] и цеолита МСМ-56 [16,17].
;Так, при алкилировании бензола этиленом в мольном соотношении 5.5 при 220-300 С и давлении 3.5 МПа на цеолите МСМ-56 конверсия этилена 97 % и состав продуктов, %(мас.): этилбен - ,зол - 93.4, диэтилбензолы - 6.2, триэтилбензолы - 0.3, ксилолы, и кумол — 0.1. При последующем контактировании полиалкил - .бензолов с бензолом в присутствии катализатора переалкилиро - .вания (типа МСМ-22, цеолита X, цеолита Р или морденита) образуется дополнительное количество этилбензола [17].
"Amoco Corp." запатентован процесс алкилирования аренов. олефинами С2-С20 (лучше этиленом, пропиленом) и спиртами в вертикальном кожухотрубчатом реакторе, через трубки которого, имеющие отверстия для циркуляции исходных компонентов и выхода продуктов, пропускают сверху вниз частицы катализатора размером менее 0.8 мм (лучше < 0.25 мм). В качестве катализатора используются цеолиты типов X, Y, Р, L, £2 с А1203 в качестве связующего. Арены подают в межтрубное пространство сверху, алкилирующий агент - снизу. Процесс алкилирования проводится при 120-400 °С, давлении 0.1-3 МПа, объемной скорости 0.1-20 ч-1 [18].
Получение этилбензола или кумола алкилированием бензола олефинами и переалкилированием диалкилбензолов возможно также в присутствии кислотного морденитового катализатора с мольным соотношением Si02/Al203 >30 [19] или магнийсодержащих молекулярных сит [20].
I "The Dow Chemical Со." запатентован комбинированный процесс дегидрирования этана в присутствии катализатора на основе морденит/цеолита, содержащего Ga, Zn или металлы Pt-группы, причем полученную этан-этиленовую фракцию без разделения используют для алкилирования бензола в присутствии кислотного цеолита, пористого силиката магния [21] или Si02/А1203 [22]. Интеграция процессов производства этилбензола и олефинов должна привести к экономическим преимуществам [23].
Активным и селективным катализатором алкилирования бензола этанолом при 500 С с образованием этилбензола и стирола является Pt на цеолите H-ZSM-5 (6.8% (мае.) Pt, Si02/Al203= = 21.5) [24].
Улучшение технико-экономических показателей алкилирования аренов олефинами достигается при совмещенном реакци - онно-ректификационном процессе, запатентованном компаниями "Chemical Research Licensing Со." и "ABB Lummus Crest, Inc." [25-27]. Неподвижный слой катализатора - кислотные молекулярные сита - служит одновременно ректификационной насадкой. Легкую фракцию, содержащую бензол, направляют на орошение колонны-реактора. Из кубового остатка отгоняют этил-
бензол, а полиалкилбензолы направляют на переалкилирование. Этот перспективный совмещенный процесс получил применение в промышленности.
Как отмечалось выше, этилбензол может быть получен также по реакции трансалкилирования - при взаимодействии бензола с ди - и полиэтилбензолами [28-30]. Процесс может осуществляться в газовой фазе в присутствии неподвижного слоя катализатора [29] или в реакторе с движущимся слоем катализатора [28]. В последнем варианте регенерированный катализатор возвращают в верхнюю часть реактора. Катализатором процесса могут служить цеолиты типа X, Y, ос, Я, ZSM-5, со, морде - нит, шабазит.
Переалкилирование бензола полиалкилбензолами можно проводить в присутствии металлоксидов элементов группы IVB, например Zr, модифицированных повышающим кислотность ок - сианионом вольфрама, на носителе (А1203, Si02 или их смеси)
[31] .
Установлено, что прямое образование этилбензол а при транс- алкилировании на широкопористых цеолитах типа Я и Y происходит лишь из о - и п-диэтилбензолов, но не идет из лг-изомера
[32] .
Этилбензол может быть получен не только алкилированием бензола этиленом, но и другими методами. Так, голландская компания "DSM" разработала двухстадийный процесс переработки 1,3-бутадиена в этилбензол [33], продав исключительную лицензию на эту технологию японской компании "Teda" с правом предоставления ее третьим странам.
|
СН=СН2 СН—СН3 сн2сн3 |
![]()
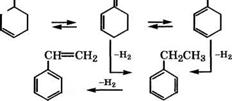 При димеризации 1,3-бутадиена по реакции Дильса - Альде - ра первоначально образуется 4-винилциклогексен [34, 35], который далее окислительным дегидрированием превращают в этилбензол или сразу в стирол [36]:
При димеризации 1,3-бутадиена по реакции Дильса - Альде - ра первоначально образуется 4-винилциклогексен [34, 35], который далее окислительным дегидрированием превращают в этилбензол или сразу в стирол [36]:
2СН2==СН—СН=СН2
Термическая димеризация 1,3-бутадиена протекает с конверсией около 40 % при селективности образования 4-винилцикло - гексена практически 100 % [35]. Для повышения конверсии возможно использование Ее-нитрозильной каталитической системы.
Окислительное дегидрирование 4-винилциклогексена возможно в присутствии следующих катализаторов: медно-магниевой оксидной системы состава 5 % СиО и 95 % (мае.) М^О, цеолитов: Ее-Ой-К-О/Н-морденит (8Ю2/ А1203 = 10) и Ее-ТЬ-К-0 / Н - к л и - ноптилолит (8Ю2/А^Од^ 5.4) [36]. Наибольший суммарный выход этилбензол а и стирола - до 77.6 % был достигнут на цеолите при 400-470 °С и мольном соотношении 4-винилциклогек - сен : 02: N2 = 1 : 0.3 : 4. Введение в систему С02 в мольном отношении к кислороду (100-200): 1 приводит к повышению выхода целевых продуктов до 82.5-83.3 %.
Окислительное дегидрирование 4-винилциклогексена может проводиться и в отсутствие 02 - при использовании в качестве источников кислорода оксидов В1, Се, Со, Сг, Си, Ее, 1п, Мп, Мо, N1), №, БЬ, Бп, РЬ или V на носителе, в частности на цеолите, БЮ, нитриде Б1 или В, ТЮ2 [37]. Так, в присутствии катализатора состава, % (мае.): К20 - 13, Ьа203 - 13, В1203 - 25, ТЮ2 - 49 при времени контакта 3.7 с конверсия 4-винилциклогексена составляет 99.7%, селективность образования этилбензола, стирола, бензола и толуола - 44.2, 49.2, 2.7 и 1.6 % соответственно.
Высокий выход этилбензола - 98.9 % достигнут при конверсии 4-винилциклогексена в смеси с 25-40 % (мае.) жидкого аммиака в присутствии 0.01-0.7 % (мае.) сплава Ма/К и небольшого количества инициатора, например ферроцена [38]. В качестве сырья можно использовать и 1,3-бутадиен: так, в присутствии магний-оксидного катализатора при 450 С, давлении 0.2 МПа и объемной скорости подачи сырья (смеси 38% (мол.) 1,3-бутадиена с N2) 190 ч 1 при конверсии 18 % селективность образования этилбензола 70 %, а в качестве главного побочного продукта получается 4-винилциклогексен [39].
Конверсия 1,3-бутадиена в присутствии промышленного шарикового цеолитсодержащего катализатора Цеокар-10 составляет 98 %, суммарная селективность образования 4-винилциклогексена и этилбензола - 67 % [40].
При использовании молибденовых катализаторов, промоти- рованных У205 и соединениями щелочных металлов (К, Се), конверсия 1,3-бутадиена 22% достигается при 560 С, давлении 0.112 МПа, объемной скорости 220 ч“1 [41]. Селективность образования продуктов следующая, %: стирол - 74, винилциклогек - сен - 12.5, этилбензол - 5.5, бензол - 4.3, толуол - 2.
Получение этилбензола и стирола различными методами возможно и из толуола - метилированием метанолом в боковую цепь [42], окислительным метилированием с использованием природного газа [43] и др. (см. главу 3).