ПРОЦЕССЫ ГРАНУЛИРОВАНИЯ в РОМЫШЛЕННОСТИ
ФИЗИКО-ХИМИЧЕСКИЕ основы. ПРОЦЕССОВ СТРУКТУРНОГО ГРАНУЛИРОВАНИЯ
В некоторых процессах гранулирования (окатывание, прессовое гранулирование ит. д.) исходным порошкам придается определенная структура в результате агломерирования с последующим формованием. Отсюда название этой группы процессов «структурное гранулирование». При этом промежуточной стадией процесса может быть перевод исходного порошкообразного материала в пастообразное состояние.
Ввиду сложности, многообразия и малоизученности процессов гранулирования единая теория гранулирования отдельных классов веществ, например порошков или паст, пока еще не разработана. В работах крупнейших исследователей процессов гранулирования [72; 78; 79; 811 освещены отдельные, хоть и весьма важные стороны процессов, выведены закономерности, которые применимы в практической работе.
Однако все явственнее ощущается потребность в разработке единого подхода к процессам гранулирования определенных классов веществ. При этом могут быть использованы достижения в иных областях науки и техники — теория адгезии Б. В. Дерягина [191, современные представления молекулярной физики о взаимодействии тел, физико-химическая механика дисперсных структур, разработанная школой Ребиндера, представления о капиллярно-пористых телах и т. д. Структурное гранулирование
объединяет широкую гамму процессов гранулирования, происходящих как под влиянием сил молекулярного взаимодействия, которые являются как бы внутренне присущими исходным частицам, так и под влиянием сил, обусловленных введением жидкости,— адсорбционных, поверхностно-активных, капиллярных.
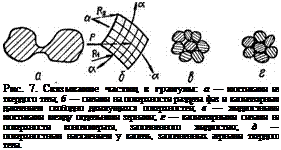
При структурном гранулировании мелкодисперсные частицы под влиянием различных сил соединяются в более крупные образования — гранулы — различными способами, среди которых по аналогии с теорией адгезии Б. В. Дерягина [19] можно выделить три основные группы:
д
1. Сухое гранулирование, которое осуществляется при отсутствии в зоне контакта частиц абсорбционных слоев и капиллярной конденсации, В этом случае частицы соединяются в гранулы под воздействием молекулярных и электростатических сил, а также в результате непосредственного соединения частиц вдавливанием их друг в друга при формовании, В конечном счете и при формовании частицы связываются молекулярными и электростатическими силами.
2. Граничное гранулирование, осуществляемое при зазорах между частицами такой малой величины, что находящиеся в них абсорбционные слои жидкости по своим свойствам существенно отличаются от нее и являются основной причиной образования гранул.
3. Жидкостное (влажное) гранулирование, соответствующее соединению сухих частиц посредством жидкости в таких условиях, когда решающим фактором гранулообра - зования становится гидродинамика вязкой жидкости без учета природы и молекулярных взаимодействий частиц порошка. '
Следующие группы характерны только для процессов гранулирования:
создание мостиков из твердого тела посредством сплавления, химической реакции, применения вязких связующих веществ, способных к отверждению, кристаллизации растворенных веществ;
прессовое гранулирование, основывающееся на создании определенной структуры в дисперсных системах с высокой концентрацией дисперсной фазы. Эта группа процессов будет рассматриваться отдельно, поскольку для нее характерны закономерности, обусловленные пастообразным состоянием вещества, рассматриваемые физико-химической механикой дисперсных систем.
Некоторые из этих групп представлены на рис. 7.
Сухое гранулирование. Теория межмолекулярных ван - дер-ваальсовых сил для атомов и молекул газов весьма подробно разработана многими учеными. При сближении атомов волновые функции их электронных оболочек искажаются: в каждом атоме появляется средний наведенный дипольный момент, причем взаимодействие этих моментов и обусловливает притяжение [19].
В полной мере эта теория применима только к разреженным системам — газам. При расчетах энергии взаимодействия между двумя молекулами, находящимися на расстоянии I, может быть применена формула [78]
Еі, і — —h, i/P, (38)
где hi,/— константа, характеризующая взаимодействие, знак минус условно обозначает притяжение.
Характерной особенностью ван-дер-ваальсовых сил является их аддитивность, т. е. энергия взаимодействия двух тел может рассматриваться как сумма энергий притяжения молекул, из которых состоят тела. Направление, развитое некоторыми учеными, позволило объяснить взаимодействие макроскопических тел следующим образом. При взаимодействии двух атомов возникает корреляция флуктуаций плотности их электронных облаков, В результате этого среднее значение флуктуационного дипольного момента, прежде равное нулю (для изолированного атома), становится отличным от нуля, т. е. в каждом атоме появился новый диполь.
Таким образом, исходя из положений квантовой механики, ван-дер-ваальсовы силы по своей сути представ
ляют взаимодействие дипольных моментов. Развитие этих идей привело к обоснованию макроскопической теории ван - дер-ваальсовых взаимодействий в конденсированных фазах, в которой ван-дер-ваальсовы силы рассматриваются как результат взаимодействий флуктуаций электромагнитного поля, что позволило использовать достижения макроскопической электродинамики и избежать предположения об аддитивности ван-дер-ваальсовых сил.
На основе этих общих положений предложен ряд вави - симостей для расчета энергии и силы взаимодействия макроскопических тел. В работе [78] дан переход от энергии взаимодействия молекул к энергии взаимодействия конденсированных систем, Энергия взаимодействия элементарных объемов двух сфер, содержащих в 1 м8 п молекул,
|
|
 |
— ** Ij 2 nitijki, і, где п£ и п,- — числа молекул і и / в 1 м3,
которую в данном случае можно принять равной А — ЛВХ£,,, энергию и силу ван-дер-ваалъсовского взаимодействия между двумя шарами можно представить в виде
Е = —Ad/24l; (40)
F = Ad/24P, (41)
где d — диаметр шара.
Эти уравнения применимы лишь в пределах значений / < 0,1 мкм. Для I > 0,2 мкм действует иной экспоненциальный закон и сила
F = Bd/m (42)
Константа В, как и константа Ван-дер-Ваальса А, зависит от свойств материала и, прежде всего, от поляризуемости и числа поляризующихся атомов или молекул на единицу объема, участвующих в переносе энергии.
В работе [78] приведены значения этих констант для кварцевого стекла. Так, установлено, что А = 10~1В Дж, В = 14 • 10-2« Дж • м.
Исходя из этих положений, было определено сопротивление гранул разрывающим усилиям: при I < 0,1 мкм
0г es 2 4, « 8,23 . 10-“ ^ Па; (43)
при А = 10_1в Дж I > 0,2 мкм, В= 1,4 • Ю-?8 Дж • м
7,64 . ЮгН^Па. (44)
Нетрудно убедиться, что для расстояние I > 0,2 мкм силы взаимодействия весьма малы.
Порядок полученных величин напряжений между 0,98 и 98 кПа для размеров частиц от 1 до 0,01 мкм и расстояний от 1 см до 1 мм лежит в пределах значений прочности, которые можно ожидать для сухого гранулята тонкодисперсных частиц, например, пигментов. Верхний предел значений 98 кПа практически недостижим при сухом гранулировании.
Итак, на основании вышеприведенных расчетов можно сделать вывод, что достаточно прочные гранулы при сухом гранулировании получаются при размерах исходных частиц порядка 0,1—1 мкм, поскольку для частиц более крупных размеров влияние сил Ван-дер-Ваальса слишком мало для соединения частиц в гранулы.
Электростатические силы. В процессе гранулирования частицы приобретают электрические заряды вследствие трения друг о друга и о стенки и рабочие органы аппаратов. Заряды отдельных частиц и особенно поля, возникающие вследствие этой электризации, могут существенно влиять на поведение частиц, их сближение, агломерирование. При отсутствии электрических полей силы электростатического притяжения появляются только на малых расстояниях, практически — при касании частиц.
В теории адгезии [19} используется представление о том, что при контакте твердых тел возникает микроконденсатор и двойной электрический слой, а работа отрыва затрачивается на разделение пластин микроконденсатора и разрушение двойного слоя. Непосредственные измерения и косвенные расчеты на базе использования экспериментальных данных определили плотность зарядов двойного слоя порядка 1/12я (0,01...0,1) Кл/м* [19]. В макроскопической картине сила взаимодействия поверхностей определяется как сила взаимодействия пластин конденсатора
на единицу площади F = 2па2, где а — плотность заряда обкладок. Такие значения заряда обеспечивают силу притяжения порядка 9,8—98 МПа [19].
Можно рассчитать прочность связи частиц под действием сил электростатического притяжения [78]. Принимаем, что положительно и отрицательно заряженные частицы ориентированы в такой же правильной последовательности, как и в решетке ионного кристалла. Поскольку такая высокая степень ориентированности практически недостижима, вычисленная сила сцепления является теоретическим максимумом. Считаем, что частицы имеют шарообразную форму и одинаковые размеры d и противоположные равные по величине заряды Qlt Q2, равномерно распределенные на поверхности частиц с плотностью ср. Расстояние между частицами намного меньше их размеров: I <£ d. По закону Кулона
![]() QiQi _. Q2 /2 /2 .
QiQi _. Q2 /2 /2 .
так как заряды частиц считаем сосредоточенными в их
центрах и Qj = Q2, поскольку
Q = tpwd2; (46)
F = <р2Л (47)
При ионной связи необходимо принимать во внимание взаимодействие смежных частиц, которое количественно учитывает фактор ионной связи (0,2905):
F„ = 0,29 уЧЧ*. (48)
При этом прочность гранулы на разрыв
02 = 2F/d? = 2 • 0,29тгу ^ 5,8сра. (49)
Из этого можно сделать вывод, что при действии сил электростатического притяжения прочность гранулы не
зависит от ее размеров.
Различными исследователями определена плотность заряда на поверхности многих веществ. Например, в работе [781 для частиц пыли злаков определена плотность заряда, при которой шар из вещества плотностью р = 1 г/см8 диаметром 24 мкм будет поддерживаться на гладкой пластинке силами электростатического притяжения. Но практические наблюдения показывают, что пластина может удер
живать частицы диаметром до 500 мкм. При этом ог2Макс =: с* 0,14 Па.
Как видно из этих вычислений, сцепление частиц, обусловленное силами электростатического притяжения, очень мало и обеспечивает ничтожное значение напряжения гранул на разрыв. Следовательно, при расчетах прочности гранулята их можно не принимать во внимание.
Граничное гранулирование. Этот термин определяет группу процессов гранулирования, состоящих в связывании сухих частиц адсорбированными на их поверхностях тонкими слоями жидкости.
Протекание гранулообразования при этом объясняется особыми свойствами граничных слоев [19; 30J: значительным отличием концентрации молекул или ионов в слое и иной молекулярной структурой слоя на расстоянии порядка 0,01 мкм от поверхности. При этом силы ионоэлектроста - тнческого характера подчиняются законам, отличающимся от законов притяжения Ван-дер-Ваальса, и обеспечивают гораздо более прочную связь частиц.
Механические свойства, в том числе и вязкость, жидкости в объеме и тонком граничном слое различны. Для каждой жидкости характерна своя величина предельной толщины слоя, при уменьшении которой жидкость переходит в квазитвердое или квазикристаллическое состояние [23]. По данным работы [64] толщина такого слоя составляет для миристиновой кислоты 0,08 мкм, олеиновой—0,058мкм, высокомолекулярных ненасыщенных жирных кислот — 0,05—0,1 мкм.
Адсорбционные слои жидкости, образующиеся на поверхности контактирующих тел, также обладают свойствами, отличающимися от свойств жидкости в объеме: большей прочностью на сдвиг, повышенной вязкостью [23]. Вязкость граничного слоя рг в несколько раз превышает объемную Роб.
Фукс Г. И. [64] предложил безразмерный коэффициент граничного загущения для оценки изменения свойств адсорбционных слоев жидкости
у^ЩогР' (50)
где х0тр — время отрыва; Fотр — сила отрыва в расчете на единицу площади; р — динамическая вязкость жидкости, Произведение т0Тр Аотр имеет размерность динамической вязкости, а отношение его к динамической вязкости в объеме отражает изменение механических свойств жидкости в процессе разъединения тел. Сила притяжения частиц адсорбционными слоями [19]
F — 2 ъга. (51)
Приравняв адсорбционную прослойку к твердому веществу, можно количественно рассчитать прочность адсорбционной связи [78].
Область, для которой наиболее существенным фактором, определяющим прочность гранул, являются адсорбционные силы, занимает промежуточное положение между сухим гранулированием, где определяющими являются силы Ван-дер-Ваальса, и влажным, где гранулообразова - ние определяется капиллярными силами.
Толщина слоя жидкости на поверхности частиц, для которого существенны адсорбционные силы, составляет от 0,3 нм — толщина мономолекулярного слоя жидкости— до 3 нм, поскольку выше этого значения жидкостный слой становится подвижным [37].
Введем обозначения: а — толщина адсорбированного слоя; /„ — нижний предел влажности, считая на 1 мя объема твердого вещества (о = 0,3 нм); fB — верхний предел влажности (а = 3 нм); q — коэффициент шероховатости. Тогда [78]
|
II 1-С) |
(52) |
|
( 1,8 - 10-е d <?. |
(53) |
|
fB — 1,8 • 10~8<7. |
(54) |
Сорбционные слои находятся в неподвижном состоянии до тех пор, пока толщина слоя а не превосходит некоторого предельного значения ак.
При этом поверхность, определяемая по формуле [781
*** * [[І + у) “ (I) ] * * у^. (55>
можсч полносгью передать когезионное напряжение окоге1,
так как
|
|
2 F I
0 2K — d2 ~ °КОГЄЗ яОк - y •
Максимальное теоретическое значение напряжения а*, достигается сцеплением сорбционных слоев на шарообразных частицах, касающихся друг друга (при а—0) при влажности /</в. На практике из-за шероховатостей аф 0,
Для определения Ощ по формуле (56) необходимо знать величины ак и оКогез. В данном случае принято предельное значение Ок — 3 нм.
Теоретически допускаемое когезионное напряжение превосходит 98 МПа, но его фактическую величину снижают пузырьки газа, выступы и т. д., поэтому можно принять оКогез=9,8 МПа. Тогда при допускаемой прочности гранул на разрыв d, равной 0,1; 0,1; 1; 10 мкм, когезионная прочность сорбционных слоев Ол< составит 9,8; 0,98; 0,098; 0,0098 МПа соответственно.
Влажное гранулирование. Во всех многочисленных и широко распространенных процессах влажного гранулирования наиболее существенным моментом является взаимодействие жидкости и сухих частиц. При этом в зависимости от количественного соотношения твердой и жидкой фаз и условий проведения процесса возможны разнообразные варианты связывания частиц в гранулы.
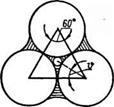
В точке контакта с частицами жидкость имеет вид двояковогнутой линзы (частицы приняты равновеликими сферическими). Боковая поверхность линзы также! является вогнутой, поскольку считаем, что жидкость смачивает частицы, т. е. © < 90°. Кривизна поверхности линзы измеряется радиусами гг и г2, которые при полном смачивании зависят от радиуса частицы R и угла &.
По формуле Лапласа капиллярное давление жидкости
|
|
где К — постоянная, зависящая только от угла &. .
В случае, если жидкости мало, она распределена дискретными разобщенными линзами (или мостиками) в точках соприкосновения частиц. Это капиллярно разобщенное состояние, или состояние защепленной жидкости.
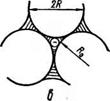
Капиллярное состояние. При увеличении количества жидкости она втягивается порами вследствие их капиллярности и мостики сливаются между собой. Это происходит при & = ЗСV (рис. 8). В момент слияния капиллярное давление при наиболее плотной укладке ра =4,1 o/R, а содержание жидкости составляет 22,6% от объема пор 137]. Данное состояние влаги именуется канатным.
 |
 |
 |
|
При слиянии жидкостных мостиков создаются условия для непрерывного перехода от одной точки жидкой фазы к другой. При дальнейшем увеличении количества жидкости она полностью заполняет поры, наступает так называемое капиллярное состояние, при котором капиллярное давление Pi=6,9ofR.
Рис. 8. Переход от стыкового состояния в канатное состояние:
а — защемленная вода: б — защемленный воздух; в —к расчету капиллярного
давления.
Если жидкость полностью обволакивает сухие частицы и ее участки сливаются на поверхности гранулы, то сила связывания частиц в этом случае определяется силой поверхностного натяжения жидкости на границе с воздухом. Такое состояние является предельным и временным, так как жидкость будет вновь смачивать другие частицы, тем самым открывая частицы и поры, прежде скрытые ею.
В работе [78] предложено произвести расчет прочности гранул при влажном гранулировании для двух вариантой при допущении, что частицы имеют одинаковый диаметр.
1. Рассмотрим прочность связывания частиц жидкостными мостиками. На основании анализа размерностей величина сил сцепления между частицами определяется из уравнения [78]
F ~adf (бр), (58)
где 0 — краевой угол смачивания; (3 — половина центрального угла жидкостного мостика. Функция /(©р) рассчитана из условий кругообразной кривизны зеркала, что справедливо при р > 10°.
При 0 = 0° (полное смачивание) и р = (10 ... 40)°
F^ (2,2... 2,7) ad. (59)
При а = 0,072 Н/м
(0,0016 ... 0,002) dH.
Как видно, изменения Р в пределах (10...40)° оказывают незначительное влияние на значение функций f и тем самым на величину F.
Введем в уравнение (58) минимальное значение F = =2,2 ad, тогда для величины сопротивления гранул на разрыв агв получим уравнение
(60)
Воспользовавшись уравнением (56), получим
Ozb^4,4-J. (61)
При а = 0,072 Н/м о2В й~ 32fd Па. Для d = 1 о2в 32 Па.
2. Если промежутки между частицами заполняются жидкостью, то во всем объеме действует капиллярное разрежение, обусловленное вогнутыми поверхностями менисков жидкости в порах.
В работе [78] на основании исследований в области гранулирования железной руды утверждается, что прочность влажных гранул зависит от капиллярного разрежения, т. е. от поверхностного натяжения жидкости в порах. Установлено, что более 80% пустот большинства гранул занято жидкостью и обычно более высокая прочность гранул достигалась, когда жидкость заполняла почти весь объем пустот.
При влажном гранулировании одновременно действуют оба механизма связывания частиц в гранулы: посредством жидкостных мостиков и капиллярного разрежения в порах. Независимо от формы поперечного сечения
в цилиндрических порах капиллярное разрежение при краевом угле © =* О
Рн = Ф, (62)
где г — гидравлический радиус (отношение поперечного сечения к периметру или объема к поверхности цилиндрической поры).
При статистическом распределении частиц в грануле гидравлический радиус определяется как отношение объема пустот к их поверхности:
![]()
![]()
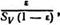 (63)
(63)
где Sv — удельная поверхность гранулы, приходящаяся на объем; отсюда
![]()
![]() Рк =
Рк =
Для сферических частиц одинакового размера 5 = 6Id 1781, отсюда
|
.. 1 (1~*)б |
![]() Рк =
Рк =
Этот расчет является весьма приближенным. Он дает лишь возможность определить среднюю высоту подъема жидкости в капиллярах. На практике из-за разной величины пор жидкость в них поднимается на разную высоту. Это приводит к тому, что некоторые поверхностные частицы окажутся не включенными в жидкостный объем и будут связываться друг с другом жидкостными мостиками. Однако, как увидим далее, подсчитанное на основании вышеприведенного расчета напряжение на разрыв и фактическое его значение, определенное опытным путем, весьма близки. При этом необходимо учесть, что на области гранулы, занятые только твердым веществом, капиллярное давление не распространяется и поэтому для определения предела напряжения на разрыв необходимо выбирать только участки поперечного сечения, занятые жидкостью.
Напряжение на разрыв, зависящее от капиллярного давления, определяется по уравнению
Оги = tpK — aSv (1 — є). (66)
В случае однородных сферических частиц напряжение на разрыв
Огк = ер* = Л. 6 (1 — є) 1 Id. (67)
Сопоставим оба теоретических механизма связи частиц при влажном гранулировании и оценим их на основании опытных данных. Отношение напряжений на разрыв для обоих механизмов связи
![]() °гк aSv(l —„ е .
°гк aSv(l —„ е .
огв“ (I — t) /(2,2a - 2Ж^й-
Использовав зависимость /Се=3,1 [78], определенную экспериментально для различных шаров, получим
Для значений е = 0,25; 0,30; 0,40 отношение огк/о2В соответственно составляет 0,69; 0,82; 1,10. Отсюда можно сделать вывод, что при более плотных упаковках (т. е. при меньших значениях е) прочность жидкостных мостиков превосходит прочность, определяемую капиллярным разрежением в грануле, пропитанной жидкостью. Это объясняется возрастанием координационного числа К при уплотнении упаковки, от которого в значительной мере зависит прочность жидкостных мостиков.
Выведенные отношения справедливы также в случае иолидисперсных частиц. При этом взамен d появляется dі — размер частиц, обеспечивающих оптимальную прочность. Получим выражение
J =* 3JTT2tSvdb ** °>46г <5^') №/«0. (70)
где d' — параметр тонины частиц; если частицы сфериче - кие, то оба множителя (Syd' и dhld') являются при распределении функциями экспоненты л[8]. Эксперимент [78] показал высокое совпадение результатов вычислений прочности гранул с действительным напряжением гранул на разрыв.
Мостики из твердого тела могут образовываться при различных по своей физико-химической сущности процессах. При спекании, сцеплении плавлением, в результате диффузии молекул или атомов в местах микроконтактов частиц возникают мостики из оплавленного материала, которые твердеют при остывании. Химическая реакция также может привести к образованию мостиков между частицами. В работе [78] описано гранулирование магнетитового
концентрата при температуре 200°С в окислительной атмосфере. При этом происходит окисление магнетита (Fe304) до гематита (Fe2Os), который образует мостики между частицами магнетита.
Связующие вещества могут отверждаться, образуя при этом твердые мостики. В зависимости от вида процесса и свойств взаимодействующих веществ связующее может вводиться в расплавленном состоянии (легкоплавкое вещество) либо в виде суспензии, которая при высыхании влаги скрепляет суспензированными частичками исходные частицы вещества. Таким способом, например, гранулируют рудную мелочь, добавляя 6—10% извести. При затвердении ее между частицами рудной мелочи образуются известковые мостики. Кристаллизация растворенных веществ происходит при сушке влажного гранулята. Возможны две разновидности связывания частиц твердыми мостиками при кристаллизации растворенных веществ. При напылении растворов частицы соединяются кристаллами, выделившимися из связующего; при напылении воды на соли они частично растворяются и при кристаллизации соединяют сухие частицы мостиками из того же вещества. Пространства между исходными частицами, занятые жидкостью, очень малы, следовательно, будут малы и размеры кристаллов, образующих мостики, определяющие прочность гранул.
Можно определить прочность гранулы, образованной вследствие кристаллизации солевых мостиков между частицами, условно считая, что доля объема мостиков в общем объеме вещества равна доле поперечного сечения их в общем сечении гранулы, что справедливо при статистическом распределении:
а г ~ (71)
где гк — доля объема выкристаллизовавшегося вещества К, считая на единицу объема зерна гранулы; ак — допустимое напряжение на разрыв вещества К. в кристаллическом мостике.
Для определения объема выкристаллизовавшегося вещества введем следующие обозначения: Y — количество растворенного вещества в процентах от массы; ft — влажность перед сушкой, считая на сухое вещество, в процентах от массы; р — плотность гранулообразующего твердого материала; р* — плотность вещества К в кристаллическом мостике; е — объем пор гранулы (пористость). При этом ftp(l — е) — влажность, приходящаяся на объем гранулы; YkftP (1 — е) — масса растворенного вещества, приходящаяся на общий объем;
efc = KKf, f (1-е); (72)
Ра
1-е) о*. (73)
Ра
В табл. 3 приводятся примеры определения прочности гранул, связанных кристаллическими мостиками [781.
Таблица 3
|
Сравнительная характеристика гранул из различных материалов
|
Допустимое напряжение на разрыв вещества До* принято произвольно в размере 5 МПа, поскольку обоснованных данных для расчета не существует. Экспериментальная проверка прочности гранулы состояла в нагружении ее грузом Р. При этом отношение
о = р/тгг® (74)
дало величину прочности гранул с солевыми мостиками 120 кПа, что подтверждает правильность произведенного расчета.