«Современные химические источники тока»
ЛИТИЕВЫЕ СИСТЕМЫ С ТВЕРДЫМ КАТОДОМ Система Li│MnO2
В качестве электролита чаще используется 1М раствор LiClO4. в смешанном растворителе ПК + ДМЭ, поэтому электрохимическая система может быть записана более подробно:
(–) Li│ LiClO4, ПК + ДМЭ │MnO2 (+)
Система Li│MnO2 имеет достаточно высокие удельные характеристики при относительно низкой цене. Удельная энергия 200 – 250 Вт·ч/кг или 450 – 550 Вт·ч/л (несколько ниже, чем у Li│SO2 и Li│CuO). Существенным недостатком этой системы является малая удельная мощность, обусловленная слабыми разрядными токами (менее 1 мА/см2) и ограниченный, по сравнению с другими ЛИТ, температурный интервал работоспособности: от –20°С до +50°С. В остальном же они обладают всеми достоинствами ЛИТ, в том числе и чрезвычайно высокой сохранностью своих характеристик (хранение до 10 лет и более). НРЦ = 3.5 В. Разрядное напряжение 2.8 – 3.0 В. Разряд обычно ведут до 2 В, глубокий разряд небезопасен. Эта систем появилась одной из первых и широко применяется во всем мире. В России производятся в г. Саратов.
Рассмотрим химию протекающих процессов. В результате токообразующей реакции
ХLi+ + ХЕ + MnO2 → LixMnO2
Или
ХLi + MnO2 → LixMnO2
Образуется так называемое соединение внедрения. Большинство твердых катодных материалов восстанавливается по аналогичному механизму внедрения.
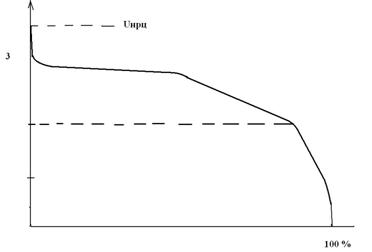
Схематичная разрядная кривая литий-диоксидмарганцевого ХИТ.
Вообще, при разряде твердых катодов (оксидов, халькогенидов и т. п.) первичный процесс протекает следующим образом: электроны, поступающие из внешней цепи, поглощаются электронной подсистемой кристаллической решетки, понижая степень окисления металла, а компенсирующие их заряд катионы Li+ десольватируются и внедряются в кристаллическую решетку из раствора. Например, рассматривая эту реакцию как окислительно-восстановительную, можно говорить о понижении степени окисления ионов марганца в MnO2 с +4 до +3.
Дальнейшая судьба такого соединения зависит от кристаллографической структуры, от соотношения параметров кристаллической решетки твердого тела и размеров катиона Li+. Если объем элементарной ячейки кристаллической решетки достаточно велик, то соединение внедрения оказывается стабильным, и именно оно будет продуктом разряда. Подобные соединения могут работать обратимо, так что катион Li+ может быть выведен обратно в раствор при изменении направления электрического тока. В последнем случае процесс внедрения называют также интеркаляцией, а образовавшиеся соединения внедрения – интеркалятами (от англ. «intercalate» – вставлять). Такое вещество является пригодным для использования в перезаряжаемых ЛИТ – литиевых аккумуляторах.
В противном случае внедрение иона лития совершается необратимо, с разрушением исходной кристаллической решетки и построением новых веществ. Такой вариант пригоден для первичных ЛИТ.
Как уже говорилось при рассмотрении элемента Лекланше Zn|MnO2, диоксид марганца – весьма сложное вещество, существующее во множестве модификаций и переходных форм. В зависимости от модификации MnO2 и от значения «Х» в уравнении токообразующей реакции, она может протекать как необратимо, так и обратимо.