АТОМЫ
Наряду с изменениями состояния вещества, которые происходят при изменениях его температуры, мы повседневно сталкиваемся с гораздо более сложными превращениями, когда меняется самое вещество — разрушаются старые и образуются новые молекулы. Так, например, железо, не защищённое от соприкосновения с воздухом, постепенно превращается в новое вещество — ржавчину.
Мельчайшие частички — молекулы ржавчины—образуются путём соединения частичек железа и частичек кислорода — газа, содержащегося в воздухе.
Частички, из которых строятся молекулы, называются атомами.
Ржавчина — вещество сложное, а железо и кислород — вещества простые.
Простое вещество не может быть получено соединением каких-либо других веществ, так как состоит из одинаковых атомов. Сложные же вещества получаются при соединении различных простых веществ, то-есть атомов разных сортов. Существуют такие молекулы, в которых содержатся тысячи атомов.
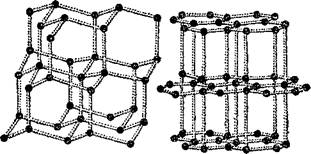
Итак, любое простое вещество состоит из одинаковых атомов. Однако построено оно может быть по-разному. У простых веществ — газов — кислорода, азота, водорода и многих других атомы соединяются по два в молекулы. В твёрдых простых веществах атомы не группируются в молекулы, но зато располагаются в строгом порядке. Замечательно, что одни и те же атомы, располагаясь по-разному, образуют вещества с совершенно различными свойствами. Так, например, мягкий графит, из которого делают сердечники для карандашей, и очень твёрдый драгоценный камень алмаз состоят из одинаковых атомов, но расположенных различно (их расположение в обоих случаях показано схематически на рисунке 1).
Алмаз и графит — разные простые вещества, хотя и состоят из одинаковых атомов. В дальнейшем такие различия нас интересовать не будут. Нам будет важен только сорт атомов«, из которого состоит вещество. Поэтому мы будем говорить не о простом веществе (например, графите или алмазе), а о химическом элементе (в данном случае углероде), атомы которого могут образовывать самые различные простые и, вместе с атомами других сортов, сложные вещества.
Все превращения вещества, при которых его молекулы перестраиваются — одни разрушаются, другие строятся
|
Рис. 1. Расположение атомов углерода в алмазе (слева) и в графите (справа). Силы, действующие между атомами, показаны условно Пружинками. |
Из атомов разрушающихся молекул, — называются химическими превращениями вещества.
Како'вы размеры и вес атомов?
Атомы очень малы. Диаметр водородного атома раївен одной стомиллионной доле сантиметра. Другие атомы по своим размерам не отличаются сильно от водородного атома. Зато по весу различные атомы очень отличаются друг от друга. Так, например, атом металла урана примерно в 236 раз тяжелее самого лёгкого атома — атома газа водорода. Но и вес тяжёлого атома урана равен всего
О, ООО ООО ООО ООО ООО ООО ООО 392 грамма.
Пользоваться такими величинами при любых расчётах, конечно, неудобно. Поэтому обычно за единицу веса атомов принимают Vie часть веса кислородного атома.
Эта единица веса была введена учёными задолго до того, как удалось узнать вес атомов в граммах, но уже было твёрдо установлено, во сколько раз одни атомы тяжелее других. В новых атомных единицах вес самого лёгкого атома —атома водорода — становится равным примерно 1,008, а самого тяжёлого —урана — 238,07.
В наши дни вес атомной единицы массы хорошо измерен. Вот чему он равен:
0, 000 000 000 000 000 000 000 001 660 350 грамма.
Сколько же атомов различных видов существует в мире? Иными словами, сколько существует различных
|
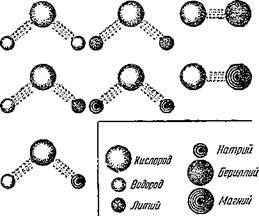
Рис. 2. Схематическое изображение молекул, образуемых кислородом с различными элементами. Рисунок показывает сходство химических свойств водорода, лития и латрия и их отличие от бериллия и магния, сходных между собой. |
Химических элементов? Есть ли какая-нибудь связь между весами атомов и их химическими свойствами?
На эти вопросы ответил великий русский учёный Дмитрий Иванович Менделеев ещё во второй половине прошлого века.
Изучая свойства химических элементов и зависимость этих свойств от веса атомов, Менделеев заметил, что по мере увеличения веса атомов химические свойства элементов периодически повторяются. Так, например, очень похожи по своим химическим свойствам газ водород и металлы—литий, натрий, калий, рубидий», цезий. Вес атома водорода в условных единицах, о которых мы говорили, равен примерно 1, лития — 7, натрия—23, калия — 39 и так далее. Атомы этих элементов могут за
менять друг друга в любых молекулах, как это показано на рисунке 2.
Так же схожи между собой бериллий, магний, кальций и некоторые другие элементы.
Рис. 3. Левый верхний угол таблицы Менделеева. Верхние цифры обозначают атомный номер, нижние — атомный вес. |
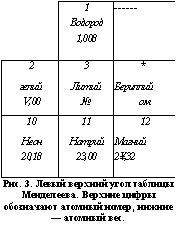 Обнаружив это, Менделеев решил выписать названия элементов в таблицу. Каждая клетка таблицы имела свой номер. В каждую клетку учёный поместил один элемент. При этом Менделеев расположил химические элементы так, что они следовали друг за другом по мере возрастания атомных весов, и так, чтобы элементы с близкими химическими свойствам« оказались в одном столбце таблицы. Таким образом, водород с номером 1, литий — 3, натрий — 11 и др. составили один столбец таблицы. Бериллий — 4, магний — 12, кальций — 20 и другие составили следующий столбец, и так далее (рис. 3). Эти цифры — номера элементов в таблице Менделеева — получили название атомных номеров.
Обнаружив это, Менделеев решил выписать названия элементов в таблицу. Каждая клетка таблицы имела свой номер. В каждую клетку учёный поместил один элемент. При этом Менделеев расположил химические элементы так, что они следовали друг за другом по мере возрастания атомных весов, и так, чтобы элементы с близкими химическими свойствам« оказались в одном столбце таблицы. Таким образом, водород с номером 1, литий — 3, натрий — 11 и др. составили один столбец таблицы. Бериллий — 4, магний — 12, кальций — 20 и другие составили следующий столбец, и так далее (рис. 3). Эти цифры — номера элементов в таблице Менделеева — получили название атомных номеров.
Некоторые клетки таблицы оказались пустыми, так как элементы с нужными свойствами ещё не были открыты. Великий учёный предсказал, какими должны быть эти новые элементы и в каких соединениях нужно
Их искать. Дальнейшие открытия химических элементов подтвердили правильность предсказаний Менделеева.
Это было большим торжеством науки.
В таблице оказалось от первой, занятой водородом, и до последней, занятой ураном, 92 клетки. Отсюда Менделеев заключил, что всего до урана включительно в природе должно существовать 92 различных химических элемента.
Существуют ли элементы тяжелее урана? О том, как учёные ответили на этот вопрос читатель узнает, прочтя последнюю главу. Пока укажем только, что элементы с атомным номером, значительно превышающим 100, существовать в природе не могут.