Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Производство синильной кислоты контактным окислением Метана и аммиака 23>129
Непосредственное образование цианистого водорода из метана и аммиака основано на эндотермической реакции:
CH4 + NH3= HCN + 3H,
Скорость этой реакции резко повышается при одновременном сжигании водорода, т. е. при неполном окислении метана и аммиака. При этом реакция становится экзотермической. Высокие выходы с одновременным значительным повышением скорости реакции достигаются при каталитическом осуществлении процесса (например, на платиновом и других катализаторах).
Существуют различные представления о механизме образования цианистого водорода при неполном окислении метана и аммиака на катализаторе. Предполагают, что процесс протекает с образованием промежуточного соединения — нитроксила HNO или распадом метана и аммиака на атомы или радикалы '30.
Углеводородные радикалы, образующиеся из углеводородов. и атомов О и Н, могут реагировать 131 с NH3 в зоне горения даже при отсутствии атомов азота. Более вероятной является радикально-цепная теория 132'133. Согласно этой теории механизм процесса складывается из следующих стадий: 1) адсорбции кислорода на платиновом катализаторе с образованием весьма активных поверхностных соединений, 2) взаимодействия молекул метана и аммиака с поверхностными соединениями на катализаторе с образованием новых радикалов и бирадикалов (СН3. NH2, OH, СН2, NH),
взаимодействия обра зующихся радикалов с метаном и аммиа-. ком, в результате чего получается метиламин CH3NH2 по реакциям:
CH2 + NH3 = CH3NH2 NH+CH4 = CH3NH2
окисления метиламина кислородом воздуха в синильную кислоту:
CH3NHa + 02 = HCN + 2Н20 + 77,6 ккал
Одновременно с образованием цианистого водорода идут реакции разложения азотных радикалов на азот и водород и окисления углеродных радикалов в окись углерода и водород. Полезно используется для образования цианистого водорода 60—63% аммиака и 56—57% метана. Остальное количество аммиака частично разлагается (12—18%) на азот и водород, частично (22—28%) остается непрореагировавшим. Для более полного использования аммиака необходим небольшой избыток метана и некоторый недостаток кислорода по сравнению со стехиометрическим количеством. Оптимальное соотношение газов (по объему) СН4 : NH3 равно 1,1 и 02 : СН4 — 1,33—1,43.
Предложено 134 использовать смеси и с иными соотношениями, например, 16,2% СН4, 10,8% NH3, 18,3% 02 и 54,7% N2. Избыток кислорода ведет к повышению температуры катализатора и частичному сгоранию цианистого водорода, т. е. к снижению его выхода.
Скорость процесса зависит от условий диффузии реагентов из объема к поверхности катализатора и продуктов реакции в обратном направлении. При большой линейной скорости газа реагенты не успевают продиффундировать к поверхности катализатора. При малой линейной скорости продукты реакции, вследствие длительного их пребывания на катализаторе, разлагаются с отложением углерода. Обычно выбирают линейную скорость газового потока в пределах 0,8—1,4 м/сек (считая на холодный газ).
В качестве катализатора применяют сплав платины с родием или иридием в форме сетки, изготовленной из нитей толщиной от 0,04 до 0,16 мм с количеством отверстий на 1 см2 от 3600 до 500. Свободный зазор между нитями равен от 0,127 до 0,287 мм.
Платиновый катализатор весьма чувствителен к действию различных примесей газообразных и твердых (пыли) веществ. Особенно вредным является углерод, образующийся при разложении нестойких в условиях синтеза углеводородов. Катализатор отравляется необратимо под влиянием этилена, пропилена и высших олефинов и особенно при наличии в газе ~0,1% ацетилена. Присутствие в газе до 0,1% сероводорода приводит к обратимому отравлению катализатора. В отсутствие сероводорода в газе катализатор, ранее отравленный сероводородом, быстро восстанавливает свою активность. Содержание окиси углерода до 8—10% не оказывает влияния на действие катализатора, а присутствие водорода в некоторой степени благоприятно сказывается на работе катализатора, предотвращая отложение углерода на его поверхности 133. Резкое снижение активности катализатора происходит при попадании на него железа, меди, свинца, а также при содержании в газе ничтожных количеств (0,00001%) соединений фосфора и мышьяка. Поэтому исходные реагенты — метан, аммиак и воздух — тш. а-
тельно очищают от механических примесей, а также от веществ, отравляющих катализатор.
Регенерацию отравленного катализатора предложено производить продувкой через него воздуха, а затем азото-водородной смеси i35.
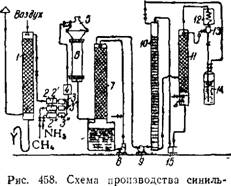
Источником метана служат метановые фракции нефтяного или коксового газа, а также природный газ, содержащие 97% и больше метана. Очищенные газы смешивают в указанном выше соотношении и направляют в кон - а тактный аппарат (рис. 458), аналогичный по своей конструкции аппаратам, применяемым для окисления аммиака в производстве азотной кислоты. Аппарат в верхней части представляет собой два конуса, сложенные основаниями. В расширенной части помещены 3—6 сеток из платинового сплава. Нижняя цилиндрическая часть аппарата представляет собой котел-утилизатор, служащий для использования тепла реакции и охлаждения контактных газов.
|
Ной кислоты каталитическим окислением Метана и аммиака: / — скруббер; 2, 2', 2" — фильтры; 3, 3', 3" — расходомеры; 4 — смеситель; 5 —контактный аппарат; 6 — котел утилизатор; 7 —поглотительная башня; 8, 15 — насосы; 9 — компрессор; 10— тарельчатая колонна; и— дистилл^- циониая колонна; 12— конденсатор; 13 — мерник; 14— приемник. |
Вначале сетку аппарата разогревают до 300—500°, затем в аппарат вводят аммиач- но-воздушную смесь (содержащую 10% NH3), которую продолжают пропускать через аппарат в течение 3—4 ч, пока устанавливается температура 800—900° и достигается определенная. активность катализатора. После этого в смеситель газов через специальный фильтр и расходомер начинают подавать метан. В выходящих из контактного аппарата газах содержится (при работе на метановой фракции нефтяного газа, содержащей 97—97,5% СН4) около 6% HCN, 1,5—1,7% NH3, 0,2% С02, 4,3—4,5% СО, 0,5% СН4, 7,5% Н2, 0,1% 02, 56,7% азота, 23—23,5% водяного пара. Степень превращения аммиака в HCN в зависимости от условий составляет 63—'70%. После контактирования газы с температурой 900—1000° проходят котел-утилизатор, где быстро охлаждаются до 150° (т. е. до температуры несколько выше точки росы с целью предотвращения гидролиза синильной кислоты). Охлажденную газовую смесь направляют в башню, орошаемую слабым раствором смеси серной кислоты и сульфата аммония для поглощения непрореагировавшего аммиака ц предотвращения образования полимеров цианистого водорода128' 137-13э<
Образовавшийся в башне раствор сульфата аммония перерабатывают в твердый продукт. Оставшуюся газовую смесь сжимают до 7 ат и подают в тарельчатую колонну, где ее промывают слегка подкисленной водой. Цианистый водород, растворяясь, образует синильную кислоту. Оставшийся газ, не содержащий аммиака и синильной кислоты, выбрасывают в атмосферу или сжигают.
В выбрасываемых в атмосферу газах допустимое санитарными нормами содержание HCN составляет 0,0003 мг/л. Очистка воздушных выбросов от синильной кислоты является важной проблемой и в процессах, осуществляемых с использованием синильной кислоты. Например, в производстве акриловой кислоты промывка отбросных газов растворами едкого натра при 60° в насадочных скрубберах не позволяет достичь санитарной нормы. Предложено 140 для полной очистки газа, отходящего из щелочного абсорбера, от синильной кислоты проводить дополнительную его промывку небольшим количеством чистого раствора щелочи низкой концентрации (0,85—3,5 г/л), не содержащего цианида натрия. Полученный водный раствор синильной кислоты подвергают дистилляции в колпачковой колонне с отгонкой жидкой синильной кислоты; кубовый остаток представляет собой слегка подкисленную воду, возвращаемую в колонну для улавливания цианистого водорода. К жидкой синильной кислоте, содержащей 98,5% HCN и 1,5% воды 141, а при дополнительной ректификации 142 до 99,5% HCN, добавляют стабилизатор — фосфорную кислоту в количестве 0,1—0,2% (или другие кислоты). На производство 1 т HCN расходуют: 1,05—1,08 т метана и 1,05 т аммиака, из которых 0,3 т превращается в сульфат аммония.
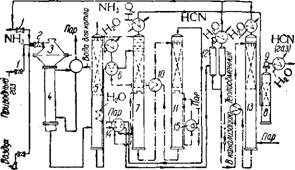
Извлечение аммиака из газовой смеси по описанной схеме является малосовершенным, связанным с затратами серной кислоты и необходимостью специальной обработки раствора для получения твердого сульфата аммония. Более совершенным способом разделения контактных газов является избирательная абсорбция из них аммиака водным раствором пентаэритритбората (или любого кислого эфира многоатомного спирта и борной кислоты). Образующаяся аммонийная соль при нагревании выше 100° разлагается с выделением аммиака и регенерацией поглотителя. Охлажденные в котле-утилизаторе контактные газы направляют в насадочную колонну (рис. 459), орошаемую холодным насыщенным водным раствором пентаэритритбората. При этом из газа переходят в раствор аммиак и цианистый водород. Непоглотившиеся газы сжигают в котельной. Вытекающий из поглотительной колонны слабокислый раствор после подогрева в теплообменнике направляют в первую десорбционную колонну, где при 80° отгоняется цианистый водород попутно с небольшим количеством аммиака. Десорбцию цианистого водорода осуществляют под пониженным давлением (200— 250 мм рт. ст.). В верхнюю часть колонны подают свежий раствор пентаэритритбората, который частично связывает аммиак, отгоняемый в процессе десорбции цианистого водорода. Основное количество аммиака выделяют в регенерационной колонне. После охлаждения и конденсации воды аммиак возвращают в процесс. Из полученной аммиачной воды выделяют остаток аммиака в отгонной колонне.
Недостатками описанного метода получения синильной кислоты являются не полное использование аммиака, образование в качестве побочного продукта окиси углерода и низкая концентрация
|
Рис. 459. Схема производства цианистого водорода с разделением аммиака и синильной кислоты: |
/ — фильтр; ! — смеситель; 3 — контактный аппарат; 4 — котел - утилизатор; 5 —поглотительная колонна; 6, 10, 14, 15 — теплообменники; 7 — десорбционная колонна; S — скруббер; 9 — ва - Куум-насос; 11 — регенерацнонная колонна; 12 — холодильник; 13 — отгонная колонна.
HCN в образующейся газовой смеси, а также определенные потери платины. Перспективным представляется некаталитическое получение цианистого водорода из метана и аммиака в псевдоожиженном Слое I2I, 127, 143 (см выше). Нагревание газов до 1400—1600° производится с помощью специальных графитовых электродов, помещенных в кипящий слой из электропроводных частиц кокса. В этих условиях концентрация HCN в газовых продуктах достигает 20—25% и основным побочным продуктом является водород. Процесс протекает в кипящем слое с большой скоростью и характеризуется быстрым подъемом температуры в реакторе и легкостью регулирования режима путем изменения скорости прохождения газа, глубины погружения электродов в кипящий слой и подводимой к электродам мощности. Эти реакторы отличаются длительностью работы при высоких температурах и могут работать как на переменном, так и на постоянном токе при напряжении, не превышающем 100 в.