Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Получение синильной кислоты плазменным методом 125’127
Известно, что вещества в плазменном (высокотемпературном) состоянии существенно отличаются от газов своими электрическими и магнитными свойствами. При 20—50 тысячах градусов в газообразном веществе практически отсутствуют нейтральные атомы и оно состоит исключительно из ионов. Даже в условиях низкотемпературной плазмы, образующейся при температурах в несколько тысяч градусов, химические процессы протекают с огромной скоростью. Это позволяет осуществить их высокоинтенсивным
путем в компактных аппаратах малых размеров и достичь больших выходов при эндотермических реакциях.
Низкотемпературная плазма получается в плазмотронах — влектродуговых устройствах, в которых электрическая дуга подвергается тепловому или магнитному сжатию. На рис. 460 показано принципиальное устройство плазмотрона с магнитной стабилизацией электрической дуги. Образующаяся дуга между катодом и анодом под влиянием магнитного поля перемещается вихре - образно по поверхности анода. Это позволяет сосредоточить тепловую энергию дуги в большем пространстве и большем объеме газа по сравнению с обычным горением дуги. В результате значительное количество энергии дуги идет на нагревание вводимого агента. Тепловой коэффициент полезного действия плазмотрона, выраженный отношением энергии, переданной газовому потоку, к энергии электрической дуги, со - составляет 60—70%, а в плазмотронах с предварительным подогревом газа, используемого для охлаждения электродов, может быть доведен до 95—98 % •
В качестве плазмообразующей среды используются аргон, азот, водород, метан и др. Изолирующими материалами служат нитрид бора, асбоцемент, фторопласт и др.
Образование цианистого водорода в плазменной среде основано на взаимодействии между атомами (в нормальном либо возбужденном состоянии), получаемыми при разложении плазменных и реагирующих газов. При получении синильной кислоты из элементов
2С + N2 + Н2 = 2HCN - 60,2 ккал
Процесс можно осуществить в азотной плазме, т. е. с одновременным использованием азота в качестве газа разряда. Источником углерода служит расходуемый графитовый катод, а водород вводится непосредственно в область разряда (в плазму). Вследствие большого эндотермического эффекта реакции достаточно высокие выходы HCN могут быть получены лишь при температурах выше 3000°. С понижением температуры равновесие реакции сдвигается В сторону разложения HCN на исходные вещества. Поэтому с целью сохранения возможно большего количества MCN в газе газовая смесь подвергается закалке—резкому охлаждению.
|
Газ |
|
1
|
И To |
X |
/М/ГА |
|
'ЖЖ |
|||
|
Рис. 460. Схема плазмотрона с маг - иитновихревой стабилизацией дуги: / — катод; 2 — соленоид; 3 — анод; 4 — дуга. |
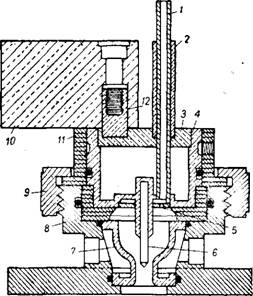
На рис. 461 представлена схема электродного узла реактора, использованного в опытах получения HCN в плазме 125. Электродный
узел реактора состоит из вольфрамового (~2% Th) стержневого катода диаметром 3 мм и съемного медного анода, запрессованного в держатель из нержавеющей стали. Медный анод помещают внутрь графитового цилиндра с целью более равномерного распределения разряда по поверхности анода. При использовании
|
Рис. 461. Конструкция электродного узла плазМенной форсунки: 1 — труба для подачи газа разряда; 2 —ниппель; 3—верхняя пластинка катода; 4 — катодный узел; 5 — газораспределительная тарелка; 6 — катод; 7—медная анодная накладка; 8 — анодный узел; 9 — чехол анодного узла; 10 — брусок, снимающий катод; // — найлоновый изолятор; 12 — втулка для снятия катода. |
В качестве исходного материала элементарного углерода вольфрамовый катод заменяют графитовым, который по мере испарения продвигается вниз, к отверстию форсунки. Катод и анод интенсивно охлаждаются водой и изолированы друг от друга корпусом из найлона, который служит также держателем катодного узла. Плазмо - образующий газ (аргон или азот) поступает через распределительную тарелку с шестью отверстиями. Мощность реактора составляла 10—12 кет.
Реагирующие газы вводятся при помощи охлаждаемых водой устройств через отверстия диаметром 0,75 мм, расположенные в съемном аноде перпендикулярно или под углом 30° к разряду.
Продукты реакции охлаждают и после отделения сажи они поступают на переработку в синильную кислоту или цианистые соли.
Процесс может быть осуществлен с применением других исходных Веществ, подаваемых в азотную плазму, например, по реакциям:
C + Nh3 = Hcn + H2
2сн4 + N2 = 2Hcn + зн2 Nh3 + сн4 = Hcn + зн2
Во всех случаях при получении 1 г-мол цианистого водорода расходуется около 2,7 кет • ч электроэнергии. Выходы HCN зависят 126, помимо других условий, также от соотношения С : N : Н.
Выход синильной кислоты составляет около 50% при синтезе из элементов, ~40% при синтезе из углерода и аммиака, 45—46% — из метана и азота и выше 50% — из метана и аммиака.
Получение дициана в плазме основано на синтезе циана при 3500—7000° по реакции
• 2С + N2 = 2CN
И полимеризации его в дицнан при охлаждении продуктов реакции. Процесс изучали 125 при температуре плазмы 4000—4500° и продолжительности контакта реагентов 5-Ю-6 сек с применением азота в качестве плазмообразующего газа и углерода, поступавшего в зону реакции за счет испарения графитового анода.
Теоретический выход дициана при атмосферном давлении и сте - хиометрическом соотношении компонентов может составить 53,5% при оптимальной температуре 4150° На 1 г связанного азота в ди - циане расходуется (без учета рекуперации тепла) 13 600 квт-ч энергии.
4 М. Е. Позия
Меси кальциевых боратов при размере зерен 2 мм к моменту полного разложения ашарита успевают разложиться в сравнительно небольшой мере 148.
148
При одновременном присутствии в сырье магниевых бора -
Тов, углекислого кальция и соединений железа оказывается возможным дозировать серную кислоту из расчета только на MgO, без практического снижения скорости и уменьшения степени разложения боратов. Это позволяет вести процесс с уменьшенным против стехиометрических количеств расходом серной кислоты за счет уменьшения степени разложения примесей. Оптимальными условиями являются: температура в реакторе не ниже 80° (обычно до 95°), количество серной кислоты 85—90% по отношению к стехиометрической норме, рассчитанной по анализу сырья на связывание MgO, СаО, Fe203 и А1203 в сульфаты (за вычетом содержащегося в сырье S03); продолжительность перемешивания 30—60 мин величина частиц сырья —2 мм. Серную кислоту вводят постепенно, при начальной температуре не выше 60°. По окончании разложения пульпа должна иметь кислотность 0,2— 0,5% H2S04. При таких условиях в раствор переходит 98—99,5% В203, а степень разложения примесей значительно ниже — в растворе содержится меньше 0,4% R203 [в виде R2(S04)3], При большей кислотности пульпы сильнее разлагаются примеси, увеличивается расход фильтровальной ткани, затрудняется отмывка бор -
1. Н. К. Воскресенская, Г. Н. Кащеев, ИСФХА, 25, 168 (1954). —
Перекисные соединения, под ред. М. Е Позина, Госхимиздат, 1951.—
Ф
® ' 22 о, 4
G " О
У CQ го
О s га ш ш <и о о) о. f - a> a> i> 3
Я й S § К s
О.»
§3
2(Kl-Ki)v
(9)
Из которого видно, что степень перехода практически не зависит от концентраций, а лишь от молярного отношения кислоты и хромата.
В практически важном случае, когда а —с, уравнение (9) после преобразований дает:
Рис. 287. Степень разложения апатита фосфорной кислотой концентрации 53,6% Р205 прй стехио - метрической норме кислоты и разных температурах:
/-20; 2-40; 3-50; 4-60; 5-80;
В отброс
ТШг
Крупные частицы извести
Рис. 301. Схема одноступенчатого непрерывного преципитирования известняком и известью (без декантации фильтрата):
1 — преципитатор для реакции с известняком; 2 — преципитатор для реакции с известковым молоком; 3 — сборник преципитатной пульпы; 4, 8, /2—центробежные насосы; J —барабанный вакуум-фильтр;
6 —шаровая мельница для мокрого размола известняка; 7 —сборник суспензии известняка; 9 —аппарат для гашения извести; 10 — классификатор известкового молока; 11 — сборник известкового молока.
Разлагается на 95—98%. Затем пульпу обрабатывают при 35—40° известковым молоком в течение 1,5 ч. Общая степень осаждения Р2О5 в обеих стадиях составляет 95—97%.
Если исходная кислота достаточно чиста (например, полученная из апатитового концентрата), то возможно ее преципитирование одним известняком76. При этом получается продукт высокого качества, содержащий 40—44% Рг05 в цитратнорастворимой форме (в пересчете на сухое вещество). Отделенный от преципитата фильтрат, содержащий остаток Р205 (0,2—0,3%), частично можно использовать для приготовления известкового молока и известняковой суспензии. Остальная часть его должна сбрасываться для сбалансирования воды в процессе и для отвода примесей (например, хлорида кальция).
На рис. 301 приведена одна из схем 51 •75,77, 84-89 получения преципитата непрерывным способом. Преципитатная пульпа перетекает последовательно через шесть реакторов-преципитаторов. В первых четырех фосфорная кислота осаждается известняком, а в
Состав фосфатного вещества шлаков твердо не установлен. Предполагают, что эффективным компонентом томасшлака является тетракальцийфосфат (хильгенштокит) 4СаО-Р2С>5 или Са4Р209 2,~23. Считают также, что Р205 в томасшлаке находится в виде силикокарнотита и Са4Р209 • CaSi03 и что часть Р205 связана в виде основного фосфата железа24. В настоящее время полагают, что томасшлак содержит и другие силикофосфаты кальция и железа, например, стедит 3(3CaO • Р2Об)-2СаО-(2СаО • Si02), томасит бСаО • Р205 • 2FeO • Si02.
Химический состав основного томасовского шлака колеблется в широких пределах (в %) 25'-
Р205 ................................ 11-23 Мл02........................................... 1-6
Si02.................................. 3-13 А1203 ........................................... 0,2-3,7
СаО................................. 38-59 MgO............................................ 2-8
Fe2C3............................... 6-25 S............................................... 0,2-11.4
Мартеновский основной шлак содержит от 7 до 14% Ра05 (из них 85% в лимоннорастворимой форме)26. Менее растворимый мартеновский шлак получают при переделе чугуна с большой добавкой плавикового шпата CaF2 в качестве флюса 27.
Химически чистый метафосфат кальция Са0'Р20Б или Са(Р03)2 содержит 71,7% Р205, технический продукт — до 65% усвояемой Р2Ов. Высокая концентрация питательного элемента является главным достоинством этого удобрения. Метафосфат кальция растворим в нейтральном растворе лимоннокислого аммония. Под воздействием воды он медленно превращается в водорастворимый монокальцийфосфат28.
[1] Мп2Ов и Мп03 в свободном состоянии не выделены; существуют их соли ПШоманганаты (Мп5+) и манганаты (Мп6+).
[2] Плотности минералов относятся к плотным разностям.
[3] Разными авторами приводятся также следующие значения констант: К - 8,83 • Ю-11 и 1 • Ю-10; Kf 2,5 • Ю-11; /ff° = 4,52 • 10~9; Kf" - 4,45 • 1<Г7 ;
АГ/Г - 4,70 • Ю-11.
[4] 100.
[5] Об аммиачном способе получения CaF2 см. стр. 1168.