Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
СОЕДИНЕНИЯ МЕДИ
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Медь легко соединяется с кислородом при нагревании1'2, обра- 8уя окислы СигО и СиО. Давление кислорода над СиО при 4500, равно 6,963-Ю-25, при 1000°—118, а при 1070° —458 мм рт. ст. Давление кислорода над Cu20 при 450° равно 7,561 • 10~26 мм рт. ст. И 760 мм рт. ст. при 1935°.
Закись меди Cu20 образует красные кристаллы кубической син- гонии с плотностью 6,0 г/см3, плавящиеся при 1235°. Окись меди СиО черного или коричнево-черного цвета кристаллизуется в триклинической и кубической сингонии; плотность 6,4—6,45 г/см3. Окислы меди в воде не растворимы.
При взаимодействии растворов солей меди с основаниями образуются осадки зеленого или коричневого цвета. Считают, чта осадки зеленого цвета являются гидратами гидроокисей, а коричневого— гидратами окислов меди3. Гидрат закиси меди СиОН образует желтые кристаллы с плотностью 3,4 г/см3, не растворим в воде, дегидратируется при 360°. Гидрат окиси меди Си(ОН)2 окрашен в цвета от синего до желтого, имеет плотность 3,4 г/см3г При нагревании обезвоживается с образованием окиси меди. В холодной воде плохо растворим, в горячей воде разлагается. Произ - бедение растворимости гидратированной окиси меди, соответствующее равновесию
СиО ■ «Н20 + Н20 Си2+ + 20Н~ + яН20
При 25—28° равно4 1,5-Ю-20; по другим данным 5 ПРСи <он)2 =» =4,8 • Ю-20, ПРси (он),.н2о = 2,0 • Ю-19. Гидрат окиси меди растворяется в водных растворах аммиака с образованием темно-синего комплекса [Cu(NH3)J(OH)2 5. Аналогичные комплексы образуют и соли меди. Гидроокись меди растворяется также в водных растворах NaOH. С солями меди неорганических и сильных органических кислот гидроокись меди образует зелено-желтые основные еоли типа C11SO4 • ЗСи(ОН)26 или CuS04- 2Cu(OH)27.
Карбонат одновалентной меди С112СО3 имеет желтый цвет и плотность 4,4 г/см3. Карбонат двухвалентной меди СиСОз не выделен в свободном состоянии, но существует в виде основных солей. Основной карбонат меди—азурит (медная лазурь) 2СиСОз-Си(ОН)2 образует моноклинные кристаллы синего цвета с плотностью 3,88 г/см3-, разлагается при нагревании до 220°. Основной карбонат меди — малахит CuC03-Сц(ОН)2 образует моноклинные кристаллы темно-зеленого цвета, свежеосажденный окрашен в голубой цвет; плотность 4,0 г/см3. Эти основные соли не растворимы в холодной воде (растворимость малахита 0,0008%, азурита 0,006%), а в горячей воде разлагаются.
Хлорид одновалентной меди Си2С12 выделяется в виде кубических кристаллов белого цвета с плотностью 3,53 г/см3, плавится при 422°, кипит при 1366°; при 0° в 100 г воды растворяется 0,0062 г Си2С12. Растворим в соляной кислоте и аммиаке с образованием Н[СиС1]2 и [Cu(NH3)2]C1.
Хлорид двухвалентной меди СиС12 — коричнево-желтый порошок с плотностью 3,05 г/см3, плавится при 498°, при 993° разлагается с образованием Си2С12. Из водных растворов выделяются: ниже 15° СиС12 • 4Н20, ниже 26° СиС12-ЗН20, ниже 42° СиС12. • 2Н20 (ромбические кристаллы синего цвета) и до 117° СиС12-Н20. Насыщенный водный раствор содержит при 0° 40,7%, при 101,8° 52,8% СиС12.
Основной хлорид меди СиС12 • 2СиО • 4Н20 сине-зеленого цвета не растворим в воде; при нагревании до 140° отщепляет ЗН20. Известны и другие основные хлориды меди: ЗСиО • СиС12 • Н20, ЗСиО ■ СиС12 • 4Н20 (минерал атакомит), ЗСиО • СиС12- 5Н20, 4СиО • СиС12 • 6Н20, 4СиО • СиС12 • 8Н20 и др.8'9.
В концентрированных водных растворах СиС12 образуется комплексное соединение [CuCl4]Cu, которое не диссоциирует на ионы и обусловливает зеленую окраску растворов. При их разбавлении происходит разложение:
[CuCl4]Cu 2Си2+ + 4СГ
|
30 40 50 ВО 70 60 90 Температура,°С |
|
Рис. 185. Давление водяного лара над кристаллогидратами сульфата меди: |
|
400 щ350 Зоо %250 |гоо I 50 О |
|
1-C11SO4 ■ 5Н20 CuS04 ■ ЗН20 + 2Н20; 2 — CuSO-4 • ЗН20 CuS04 ■ Н20 + 2Н2О; 3-CuS04 • 5Н20 CuS04 • Н20 + 4Н20. |
С повышением температуры равновесие этой реакции сдвиТается влево10. Ионы Си+ и Сц2+ образуют комплексы и с другими хлори
дами, например кальция, 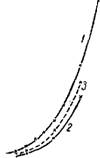 ртути, цинка —CuCl2*CaCl2, СиС12«
ртути, цинка —CuCl2*CaCl2, СиС12«
HgCl8t CuCl2-ZnCl2 12.
Пятиводный кристаллогидрат сульфата меди CuS04-5H20 (хальконтит), называемый медным (синим) купоросом, образует асимметричные ярко-синие кристаллы триклиноэдрической системы с плотностью 2,29 г/см3. При нагревании он плавится при 110° с потерей части кристаллизационной воды и переходит в трехводный (голубого цвета) и одноводный (белого цвета) сульфат меди. Выше - 258° образуется безводный сульфат меди белого цвета, сильно гигроскопичный. При 819—860° CuS04 разлагается по реакции
2CuS04 = S03 + CuO • CuS04
А при 897—934°полностью диссоциирует на CuO и SO313-15. Давление водяного пара над кристаллогидратами сульфата меди показано на рис. 185. При обычной температуре кристаллы медного купороса на Воздухе не выветриваются 16.
Насыщенный водный раствор медного купороса содержит при 0°— 12,9%, при 20° — 17,4%, при 55° —26,9%, при 100° —42,4% CuS04. Безвариантное равновесие CuSC^»
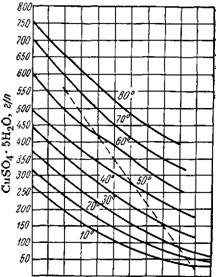
5Н20 + CuS04 • ЗН20 + раствор + пар существует при 96° .и 540 мм рт. ст. Растворимость медного купороса в присутствии свободной серной кислоты понижается (рис. 186); в растворе образуется 17-19 комплексный ион [Си (S04)2]2~. При повышенных температурах из кислых растворов кристаллизуется CuS04 • ЗН20 (в области, лежащей правее и выше пунктирной линии).
|
О So Мо Wo 200250300350 Mmsoossff М, онцентрация H^SC^, Г/л |
|
Рнс. 186. Изотермы растворимости медного купороса в присутствии свободной1 серной кислоты. |
В системе CuS04 — FeS04 — H2S04 — Н20 в интервале 27—95° и диапазоне концентраций H2S04 от 7 до 37 г/л и FeS04 от 10 до 300 г/л твердые фазы представляют собой три типа твердых растворов (Си, Fe)S04-5H20 с содержанием FeS04 (в вес. %): 0—2,6, 2,7—4,7 и 8,5—9,2. С повышением температуры растворимость твердого раствора уменьшается, а содержание FeS04 в нем возрастает. В растворах с увеличенной кислотностью повышается содержание FeS04 в кристаллах, но понижается их растворимость20.
ПРИМЕНЕНИЕ
Из соединений меди в наибольших количествах применяется медный купорос. Его используют в гальванических элементах в Качестве электролита, в гальванотехнике, для консервирования дерева, для изготовления некоторых минеральных красок, в производстве искусственного волокна и при обогащении руд.
Растворимые соединения меди ядовиты. Этим обусловлено широкое использование в сельском хозяйстве препаратов, содержащих медь21. Преимущественное применение находят сульфат меди, основной сульфат меди, хлорокись меди, основные карбонаты меди, закись и окись меди. Препараты меди, предназначенные для опрыскивания, содержат 16—55%, а иногда до 80% Си. За границей выпускают также медные препараты с повышенной фунгицидной активностью в форме высокодисперсных веществ под общим названием «коллоидная медь». Например, препарат «Duphar Colloidal Copper» представляет собой пасту, состоящую из коллоидной хлорокиси меди (с размерами частиц 0,01 мк) и поверхностно-активного вещества. По рекламным данным, этот препарат, содержащий 27% Си, дает экономию меди по сравнению с сульфатом меди В 4 раза, по сравнению с хлорокисью меди — в 3 раза и по срав< нению с закисью меди — почти в 2 раза. Выпускают также минерально-масляную эмульсию — пасту, с 40% меди в виде одной из солей. Соединения меди входят также в комбинированные фунгициды, содержащие коллоидную или молотую серу (5—25 % Си и 40—50% S). Соединения меди добавляют к органическим фунгицидам, заменителям медных, для усиления их эффективности и придания универсальности действия 22.23. Закись меди используют как компонент красок для подводной части морских судов с целью защиты от обрастания водорослями.
Среди неорганических веществ медный купорос является одним из наиболее эффективных препаратов для борьбы с болезнями плодовых деревьев, виноградников и других растений, и из всех медных препаратов применяется в СССР в наибольших количествах. Чаще всего его используют в смеси с известью или другими наполнителями. Смесь водного раствора медного купороса с известью (1 кг CuS04- 5Н20 и 0,75 кг свежегашеной извести на 100 л воды) известна под названием бордосской жидкости, представляющей собой водную суспензию основного сульфата меди ЗСи(.ОН)2« • CuS04 и CaS04. Основная соль полностью разрушается в щелоч* ной среде. Для образования суспензии стойкой основной соли молярное отношение СиО : СаО должно быть равным 1 : 0,75, а весовое отношение 1:0,53, или весовое отношение СиО:Са(ОН)2, равным 1 :0,7. В связи с частичной карбонизацией известц при хранении и перевозках, при изготовлении бордосской жидкости принимают весовое отношение медного купороса к извести 1 :0,-71э.
При смешении раствора медного купороса с раствором соды получается бургундская жидкость — суспензия основного карбоната меди ЗСи(ОН)2 • 2СиС03. Преимуществом ее перед бордосской жидкостью является хорошая прилипаемость и отсутствие комков, забивающих распылительные устройства. Медный купорос применяют для изготовления парижской зелени (см. гл. XXXVI).
Описано24'25 применение медного купороса для борьбы с чрезмерным развитием водной растительности в водохранилищах, придающей воде запах и привкус.
Требования к качеству медного купороса представлены в табл. 44>
ТАБЛИЦА 4*
Состав медного купороса (в %)
CuS04-5H20, Не Менее ....
В пересчете на Си, не менее Железо (Fe), не более.... Свободная H2S04, не более . Не растворимый в воде остаток
Не более.....................................
Мышьяк (As), Не более. . .
|
По гост 5.1688-72 |
Марка А |
|||||
|
(со знаком качества) |
Сорт I |
|||||
|
«2 3 К |
О) 3 |
« Я К |
I> А |
- |
Я |
П Я |
|
QJ А |
А |
Ь А, |
Н А |
О. Я |
||
|
И |
X X |
О |
К и |
О |
И |
S |
|
99,0 25,19 0,035 0,25 |
95,0 24,17 0,03 0,25 |
98 24,9 0,06 0,25 |
94 23,9 0,03 0,25 |
94 23,9 0,1 0,25 |
92 23,4 0,3 0,25 |
96 0,02 0,25 |
|
0,05 0,005 |
0,04 0,001 |
0,1 0,015 |
0,05 0,015 |
0,1 0,015 |
0,4 0,03 |
0,05 0,018 |
Медный купорос I и II сортов марки А предназначается для сельского хозяйства, III сорта — для обогатительных предприятий, марки Б — для предприятий искусственного волокна. Тарой для медного купороса служат деревянные бочки, фанерные барабаны или ящики с бумажными или полиэтиленовыми вкладышами, а также двойные полиэтиленовые и джутовые мешки и четырехслой - ''ные бумажные мешки.
Все большее значение приобретает хлорокись меди, которая содержит 55—56% Си и имеет ряд преимуществ по сравнению с медным купоросом. Расход меди при применении хлорокиси на 30% меньше, чем при употреблении медного купороса и при этом нет надобности в расходовании извести, необходимой для изготовления из медного купороса бордосской жидкости. Помимо этого хлор - окись меди и препараты на ее основе оказывают меньшее ожигающее действие на растения26.
Согласно ГОСТ 13200—67, 90%-ный смачивающийся порошок: хлорокиси меди, представляющий собой смесь хлорокиси меди,, концентрата сульфитно-спиртовой барды и декстрина, применяющийся в виде водных суспензий в качестве фунгицида, должен содержать 51 ± 2% Си и не более 0,8% С1_ и 2% влаги.
Медь является одним из микроэлементов, необходимых для жизни всех растений и животных. В качестве медных микроудобрений могут быть использованы низкопроцентные руды, содержащие медь, а также пиритные огарки27.
СЫРЬЕ И СПОСОБЫ ПРОИЗВОДСТВА МЕДНОГО КУПОРОСА
Основным сырьем для получения медного купороса служат серная кислота и медь: медный лом или отходы металлообрабатывающей промышленности — стружка, опилки и т. п., а также отходы или полупродукты металлургии меди — белый матт и окись меди, ватержакетная пыль, шлаковые отходы, электролитные растворы ■медеэлектролитных заводов, цементная медь, извлекаемая из рудничных вод и из колчеданных огарков и др.
Важным видом сырья для получения солей меди является ватержакетная пыль, представляющая собой тонкий порошок и содержащая 0,5—5% Си в форме сульфида и сульфата, 40—50% Fe, 3—5% А120з, 3—6% Zn, до 15% S, 7—10% Si02 и др. Перспективным видом сырья являются шлаковые отходы медеплавильных заводов, накапливаемые в течение многих лет в виде отбросов. Медь в этих отходах содержится в окисной, сульфидной и силикатной формах, а также в форме металла и ферритов. Примерный состав шлаковых отходов следующий: 2—7% Си, 5—7% Fe203, 15—25% А120з, 45-50% Si02, 1-5% СаО, 5—10% MgO, 1-3% S и 1—2% прочих примесей.
Некоторый интерес в качестве сырья для производства медного Ttynopoca представляют рудничные воды, образующиеся при выщелачивании отвалов атмосферными осадками и содержащие до 0,7 г/л меди 28.29.
Большим резервом сырья для производства солей меди являются накапливаемые массы огарков от обжига колчедана на сернокислотных заводах. В старых огарках от сжигания рядового колчедана содержится до 1,5% меди в виде CuS04, CuS03, CuO, Cu2S, CuS, CuFeS2. Необходимость извлечения соединений меди из огарков диктуется условиями их использования металлургической промышленностью в качестве заменителя железной руды.
Указанные виды сырья в основном перерабатывают в медный •купорос, который, помимо непосредственного употребления, служит также исходным материалом для получения всех других солей меди.
Способы производства медного купороса различают главным образом по видам применяемого сырья:
1) из медного лома и отходов меди (стружки, высечки, проволоки, опилок и т. п.) с окислением меди кислородом воздуха,'электролизом или раствором хлорной меди;
из окиси меди, получаемой из белого матта;
из окиси меди и сернистого газа;
из окисленных медных руд, содержащих незначительное ко* личество меди, переработка которых на металлическую медь плавкой в печах является неэкономичной;
, 5) из колчеданных огарков и других отходов;
6) из отбросных электролитных растворов медеэлектролитных. заводов.
За рубежом основными производителями медного купороса яв«- ляются Франция и Италия, где в качестве сырья используют главным образом медный лом и окисленные руды. В отличие от этого» в США используют в основном электролитные щелоки, из которых производят больше половины ваех солей и препаратов меди.