ПЕНООБРАЗОВАТЕЛИ
На вопрос, что такое пенообразователи, можно было бы ответить просто: это те вещества, которые при определенных условиях образуют пену. Однако на вопрос, какие же именно вещества образуют пену, столь однозначно ответить нельзя. Пена из водных растворов поверхностНо-активных веществ-это одно, а пена из вязких растворов сахара или из раствора дизельного топлива в эфире - другое. Дабы в дальнейшем определить границы описываемого, условимся, что главное внимание мы будем уделять пенам, получаемым из водных растворов поверхностно-активных веществ или, сокращенно, ПАВ. Именно они и являются основными пенообразователями. ПАВ-это собирательное понятие, это тысячи различных веществ, каждое из которых в той или иной мере обладает пенообразующей способностью.
Поверхностно-активные вещества при растворении в жидкостях существенно понижают избыточную (свободную) поверхностную энергию, т. е. поверхностное натяжение, на границе раздела раствор-газ. Поясним, что при этом происходит.
Молекулы поверхностно-активных веществ состоят из полярных и неполярных групп. Полярные группы-это ОН, СООН, NH2, SOJH и другие, а неполярные-это углеводородные цепи: прямые, разветвленные, замкнутые или их сочетание. Такая двойственность в структуре и определяет поведение молекул ПАВ в растворе и на границе раздела фаз.
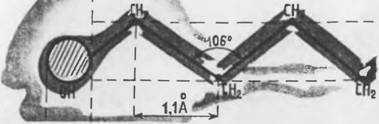
Принято изображать молекулы ПАВ в виде головастика: тем самым подчеркивается различие в свойствах Полярной «головки» и неполярного «хвоста» молекулы. Действительно, молекулы ПАВ имеют два «лица», это своего рода двуликие Янусы. Если продолжать образные сравнения, то молекулу ПАВ можно уподобить спичке с головкой. Площадь поперечного сечения такой «спич-
|
|
Гидрофиль-j Гидрофобная Часть Ная часть 1
«Головяствк», он же «спичка». Так выглядит молекула ПАВ.
Ки» около 20 А2 (0,2 нм2). В новейшей литературе отступают от строгих линий и изображают молекулы ПАВ в более «свободной форме».
Прибегнув к некоторым упрощениям, можно объяснить структуру и свойства ПАВ таким образом. Полярная часть молекулы ПАВ гидрофильна («водолюбивая»), а неполярная - гидрофобна («водоненавидящая» или. как чаще говорят, «водоотталкивающая»). Конечно, она никого не «отталкивает», как не отталкивает воду и «водоотталкивающая» ткань. Просто она воду «не любит», «враждебна воде», т. е. не смачивается водой. Гидрофильная же часть смачивается водой хорошо и увлекает за собой в раствор всю молекулу. Для гидрофобной части молекулы-обычно это длинная углеводородная цепочка- характерна, наоборот, «водобоязнь» и практически нерастворимость в воде. Из-за наличия гидрофобной группы молекулы ПАВ в объеме раствора притягиваются молекулами воды слабее, чем молекулы воды друг к другу. Именно поэтому ПАВ склонны скапливаться (адсорбироваться) на поверхности раствора (поверхности разделг
|
Плотным строем, как футболисты перед воротами при штрафном ударе. |
Фаз), образуя слой вещества толщиной в одну молекулу (мономолекулярный слой, или монослой). При этом концентрация ПАВ на поверхности раздела фаз может быть очень высокой, даже если в объеме раствора содержание ПАВ незначительно. В этом слое гидрофобные части молекул «торчат» в воздух, а гидрофильные «головки» погружены в воду.
Адсорбция молекул ПАВ на поверхности раствора приводит к понижению свободной поверхностной энергии и к появлению некоторых особых свойств: поверхностной вязкости, «эластичности» и т. д. Из такого раствора легко получить «мыльный» пузырь.
Если каплю раствора с поверхностно-активным веществом превратить в пузырек, можно подсчитать толщину его стенки H (в см):
H = V/4nR2
Где V-Объем жидкости на кончике трубки, см3; R-радиус образовавшегося мыльного пузырька, см. При постоянном объеме мыльной жидкости толщина стенки пузырька Л будет уменьшаться по мере увеличения размера шара. Когда мы дуем в трубку, чтобы растянуть жидкость в пленку, мы совершаем работу для преодоления сопротивления внешнего слоя жидкости.
Поясним это простой схемой из учебника. Молекулы в жидкости притягиваются друг к другу. Внутри жидкости силы такого взаимодействия (обозначены большой стрелкой) для всех молекул этой жидкости уравновешивают друг друга. Но у молекул, находящихся на самой поверхности, некоторые составляющие межмолекулярного взаимодействия (на нашем рисунке они условно обозначены более короткими стрелками) нескомпенснро- ваны. Таким образом, молекулы жидкости как бы втягивают внутрь (правильнее сказать, стремятся втянуть) молекулы из наружного слоя. Разница этих двух сил, обозначенных большой и малой стрелками и направленных в противоположные стороны, очень велика.
Величину такого взаимодействия характеризуют понятием «внутреннее давление»; для жидкостей, особенно полярных, оно очень велико. Так, для воды внутреннее давление превышает 1,1 ГПа (гигапаскаля), что соответствует 11 тыс. атмосфер. Именно вследствие огромного внутреннею давления жидкости практически несжимаемы.
Так как силы молекулярного притяжения в поверхностном слое жидкости (и твердого вещества также) не скомпенсированы, в нем появляется свободная поверхностная энергия. Количественно эту энергию характеризуют удельной величиной, т. е. величиной, отнесенной к единице поверхности. Эта энергия, обозначаемая греческой буквой а, является основной характеристикой поверхностного слоя жидкости или твердого вещества.
В большинстве случаев без особых оговорок термин «удельная свободная поверхностная энергия» заменяют термином «поверхностное натяжение».
|
У молекул в поверхностном слое силы межмолекулярного взаимодействия не уравновешены. |
Поверхностное натяжение - это работа, которую нужно затратить на образование единицы поверхности данного вещества, т. е. на то, чтобы увеличить его поверхность на 1 см2. Чем меньше эта работа, тем меньше поверхностное натяжение, тем легче диспергируется вещество (для жидкостей-легче образуются пены и эмульсии). Поверхностное натяжение в первую очередь зависит от природы вещества. Напомним читателю, что у воды поверхностное натяжение очень велико-72,58 дин/см, или эрг/см2, это почти в 3,5 раза больше, чем у этилового спирта и в 2,5 раза больше, чем у бензола
Поверхностное натяжение традиционно выражали в динах на сантиметр (дин/см) или в эргах на квадратный сантиметр (эрг/см2). Численно эти значения совпадают. Таким образом, поверхностное натяжение - это сила, приходящаяся на единицу длины, или энергия, приходящаяся на единицу поверхности. В СИ силу выражают в ньютонах (Н), а единицу длины-в метрах (м). Размерность поверхностного натяжения выражается в ньютонах на метр (Н/м). (Для тех, кто еще не полностью освоился с переходом на новые единицы, в скобках будем указывать и старые.) Для воды а = 72,58 • 10~3 Н/м.
Поверхностное натяжение на границе раздела двух жидкостей или жидкости и газа измеряют с помощью хотя и простых, но весьма точных приборов. Для определения поверхностного натяжения на границе раздела жидкость-воздух чаще других пользуются методом максимального давления образования пузырька. Для этого служит капиллярный прибор, усовершенствованный П. А. Ребиндером. В растворе, для которого необходимо определить поверхностное натяжение, выдувают воздушный пузырек и измеряют давление, при котором пузырек отрывается от капилляра. Прибор представляет собой стеклянный капилляр, соединенный трубкой с чувствительным устройством для измерения давления; обычно это барометрическая трубка, заполненная подкрашенной водой.
С помощью прибора П. А. Ребиндера определяют сначала максимальное давление газового пузырька в чистой воде, а затем в исследуемом растворе. Для конечного расчета достаточно составить простую пропорцию, в которой не известна только искомая величина.
Пользуются и другими методами: взвешивания капли, капиллярного поднятия, отрыва кольца от поверхности, колеблющейся струи, скорости течения в капиллярах и др
Чем меньше поверхностное натяжение раствора, тем меньше работа, которую нужно затратить, чтобы получи гь большую поверхность раздела газ-жидкость и тем легче создать большую поверхность пленок в пене и получить большой объем пены. Из растворов поверхностно-активных веществ с малым поверхностным натяжением можно получать пены повышенной кратности. Поверхностное натяжение пенообразователей легко определить экспериментально, что позволяет предсказывать пенообразующую способность известных и вновь создаваемых ПАВ и оценивать их пригодность для изготовления пен. Но это далеко не единственный технический критерий, по которому выбираются пенообразователи. Для практики важны и такие характеристики, как растворимость в воде, моющая и смачивающая способность, способность к ценообразованию в жесткой и морской воде и многие другие. Зная эти показатели, можно, не проводя дополнительных специальных испытаний, определить рациональные области применения пенообразователей.
В последние годы к числу важнейших оценочных критериев относят биологическую разлагаемость ПАВ. К сожалению, ПАВ могут оказывать отрицательное воздействие на растительный и животный мир, на природу вокруг нас. Использование пены для флотации, в текстильном производстве и в пищевой промышленности, при пожаротушении, промывке танкеров и машин, стирке (этот перечень можно продолжать и продолжать) привело к тому, что в сточных водах неизбежно появляются поверхностно-активные вещества-пенообразователи. Со сточными водами они попадают в очистные сооружения, на поля орошения, в реки и озера. Поэтому токсичность пенообразователей и скорость их биологического разложения необходимо тщательно контролировать.
В очистных сооружениях под действием бактерий, кислорода и ультрафиолетовых лучей происходит биологическая очистка сточных вод. Этот процесс-так называемое самоочищение-продолжается в естественных водоемах. Биохимический распад приводит к тому, чтс входящие в состав пенообразователей органические веще ства окисляются до С02 и воды (40% от массы ПАВ) а остальная масса становится безвредной и усваиваете микроорганизмами. Если же биохимического разложенш не происходит, то окружающей среде наносится громадный экологический вред: болеет и погибает рыба, водоплавающая дичь, зоопланктон, замедляется рост водяных растений, возможны и другие вредные последствия.
По стандартам, действующим в странах СЭВ, выпускаемые промышленностью поверхностно-активные вещества в зависимости от биологической разлагаемое™ подразделяются на три группы:
I-биологически хорошо разлагающиеся вещества (количество биологически разлагающегося вещества АГра1Л не менее 85%);
II-биологически средне разлагающиеся вещества (*раал = 70-85%);
III-биологически трудно разлагающиеся вещества (Крах-, менее 70%).
К поверхностно-активным веществам третьей группы-
Биологически жестким ПАВ-относится большинство катионоактивных препаратов, а среди неионогенны* и анионоактивных веществ-такие, как рафинированный алкиларилсульфонат (препарат РАС), сульфонол НП-1, а также ОП-7 и ОП-Ю и ряд других (о химической классификации ПАВ речь пойдет чуть дальше).
В Советском Союзе составлен список ПАВ, рекомендуемых для применения в промышленности в зависимости от их биологической разлагаемости. Повсеместно вещества группы III заменяются веществами групп I и II. По существующим требованиям моющие средства должны содержать не менее 80% биорасщепляемых компонентов. Эти меры должны способствовать сохранению экологического равновесия в окружающей нас природе.
Все выпускаемые в нашей стране поверхностно-активные вещества проходят тщательную токсикогигиени- ческую проверку. Оценивается их раздражающее воздействие на кожу, дыхательные пути, глаза человека и животных, а также отравляющее действие при попадании в организм человека. Установлено, что пенообразоВатели, получаемые из пищевых продуктов, абсолютно безвредны. Безвредны также большинство ПАВ, производимых из других видов животного и растительного сырья; синтетические ПАВ требуют более осторожного обращения Так, если разбавленные растворы синтетических ПАВ не вызывают побочных явлений при попадании на кожу и даже в глаза человека, то концентрированные растворы при многократном действии могут вызвать дерматиты и ухудшение зрения. Все применяемые ныне пенообразователи не обладают кумулятивным действием, т. е. не накапливаются в организме, и попавшие в нас мелкие дозы ПАВ быстро выводятся из организма без ощутимых последствий. Опасны для человека лишь дозы в сотни граммов. В этом смысле и обычная поваренная соль опасна: двести граммов соли вызовут смертельное отравление, если их проглотить сразу. Оговоримся, что это данные экспериментов на животных.
Не следует думать, что пену можно получать только в растворах, содержащих ПАВ. Известно, что растворы электролитов не дают пены, так как воздушные пузырьки в такой среде живут считанные доли секунды. Поэтому невозможно получить пену, например, в растворе ацетата свинца или во взвеси гидроксида алюминия. Но смесь этих растворов при определенных условиях дает пену, которая может существовать двое суток. Еще более живуча пена из смеси растворов солей салициловой кислоты и гидроксида алюминия (более 20 суток).
Как мог заметить читатель, названные электролиты - это соли органических кислот. Поэтому некоторые исследователи считают, что ценообразование в таких смесях (только вместе!) связано с возникновением сложных вну - трикомплексных, или многоядерных, соединений, изучением которых заняты химики многих стран. Правда, такие соединения в качестве пенообразователей находят пока еще крайне ограниченное применение.
Образование пены из жидкости, независимо от характера этого процесса и типа вспенивающего агента, предполагает растворение в жидкости поверхностно-активных веществ. При растворении ПАВ получаются истинные либо коллоидные растворы. Истинные (иначе-молекулярные) растворы содержат частицы размером не более 0,001 мкм, т. е. Ю-5 м, что сопоставимо с размером молекул, они в растворе уже не образуют отдельной фазы. Растворы, содержащие частицы размером от 0,001 до 0,1 мкм, т. е. Ю-7-Ю-9 м, называют коллоидными. Эти растворы менее дисперсны, чем истинные, но более дисперсны (менее грубые), чем суспензии и эмульсии.
Между ПАВ и растворителем, например водой, происходят сложные взаимодействия. В зависимости от вида образующихся при этом систем все поверхностно-активные вещества принято разделять на две категории. Это деление. имеет прямое отношение к эффекту ценообразования в растворах.
К первой категории относятся мицеллообразующие (полуколлоидные, или мылоподобные) вещества, к другой-вещества, не образующие мицелл. ПАВ первой категории в растворе выше некоторой определенной концентрации, называемой критической, образуют коллоидопо - добные объединения, называемые мицеллами. Обычно такие растворы обладают высокой пенообразующей способностью. ПАВ второй категории не образуют мицелл ни в растворах, ни в адсорбционных слоях. При любой концентрации они находятся в истинно растворенном состоянии и являются слабыми пенообразователями.
К поверхностно-активным веществам первой категории относятся некоторые природные соединения (белки
ллыинаты, пектиновые вещества и т. д.), продукты химиЧеской обработки природных полимеров (производные целлюлозы) и синтетические полимеры.
Пенообразователи из природных соединений на основе растительного сырья и животных продуктов используются человеком для мытья и стирки, приготовления нищи и для некоторых технологических процессов уже несколько тысячелетий. В жарких районах Кавказа, Средней Азии, Африки, Южной Америки издавна широко применялся мыльный корень. Это корень растения сапо - ниноноса, содержащего легко извлекаемый водой сильный пенообразователь-сапонин. Корень очищали, сушили, размалывали, порошок смешивали с глиной и формовали кусочки «мыла». Последние хорошо мылились (давая пену) в мягкой и даже в жесткой воде. Предостерегаем читателя от поспешного вывода о том, что основой моющего действия является пенообразование. О моющем действии-позднее. А пока заметим, что вещество, дающее в растворах отличнейшую пену, не всегда хорошо отмывает.
К числу эффективных природных пенообразователей относится также агар-агар-смесь полисахаридов морских водорослей. Известно несколько десятков водорос - Ен, нз которых агар-агар получают в промышленном масштабе; это, например, морская капуста. Все они содержат агар-агар в виде солей щелочных и щелочноземельных металлов. Он и сейчас широко применяется в кондитерской промышленности и в медицине в качестве пенообразующего и желирующего средства, а также стабилизатора.
|
33 |
Наиболее устойчивые пены образуются на основе белковых пенообразователей, которые получают из разнообразных веществ, либо полностью состоящих из белка, либо содержащих его в значительном количестве. Эти белки извлекают из крови животных, кожи, костей, рогов, копыт, щетины, перьев, рыбьей чешуи, жмыха мас-
3 III
Личных культур, а также продуктов, получаемых из молока. При производстве таких пенообразователей белки предварительно гидролизуют, так как продукты их гидролиза обладают гораздо более высокой пенообразую - щей способностью, чем сами белки. Для этого белки подвергают тепловой обработке в кислотной, щелочной или нейтральной среде, причем гидролиз не должен идти до конца, так как продукты конечного распада белков - аминокислоты-не обладают способностью образовывать устойчивую пену.
Все белковые пенообразователи представляют собой питательную среду для различною рода микроорганизмов, поэтому в состав этих пенообразователей обязательно вводят антисептики (фторид натрия, фенол и другие). Без них пенообразователи быстро теряют свои свойства и начинают дурно пахнуть.
Промышленные пенообразователи на основе белкового сырья (например, ПО-6, ПО-7 и другие) приготавливают многостадийной переработкой. Так, при производстве пенообразователя ПО-6 белок крови животных вначале гидролизуют едким натром, затем нейтрализуют хлоридом аммония или серной кислотой, полученный раствор упаривают до заданной концентрации. Для повышения устойчивости пены в состав пенообразователя вводят сульфат железа, фторид натрия или другие стабилизаторы.
При производстве пищевых продуктов используют пенообразователи из яичного белка и молочных продуктов. По пенообразующим свойствам не уступают яичному белку выжимки из семян сои и хлопчатника, экстракт чая. Для повышения устойчивости пищевых пен, как правило, вводятся стабилизаторы - казеин, альгинаты, желатин.
Однако сырьевая база для производства пенообразователей из растительных и животных продуктов весьма ограниченна, поэтому в развитых странах освоено про-
ігінодство поверхностно-активных веществ, называемых сн н гетическими (искусственными).
Еще до конца 50-х годов основным моющим всще - с і ном было жировое мыло, для изготовления которого использовались сотни тысяч тонн продуктов животного И растительного происхождения: жир бараний, свиной, молений, китовый, а также масло подсолнечное, хлопковое, льняное и другое. Нет нужды говорить, что это жиры, которые моїут найти и другое применение.
Мыла, изготовленные из такою сырья,-это соли предельных и непредельных жирных кислот. Такие мыла долгое время были чуть ли не единственными пенообразователями. Интересно, что уже в XIII веке на Руси было налажено производство мыла, его даже вывозили в другие страны.
В 1912 году русский ученый Г. С. Петров путем сульфирования нафтеновых кислот получил первое синтетическое моющее средство. Это был так называемый «контакт Петрова»; ныне по этому способу производится большинство моющих веществ. В недалеком прошлом такие вещества называли заменителями или вспомогательными. Но это как раз тот случай, когда «заменитель» оказался лучше заменяемого.