Точка нулевого заряда
Точка нулевого заряда (тнз), когда заряд на поверхности кремнезема равен нулю, так же как и изоэлектрическая точка, когда подвижность частиц кремнезема равна нулю, измерялась многими методами. При измерении тнз геля кремнезема калориметрическим методом [47] пришли к заключению, что она должна находиться между рН 2,5 и 3. Однако в данных, полученных этими авторами, отсутствовала возможность оценки значений ниже рН 2, поскольку теплота реакции нейтрализации при рН<3 становится чрезвычайно малой.
Де Бур, Линеен и Оккерс [48] в своем обширном исследовании процесса полимеризации кремнезема нашли, что значение иэт лежит между рН 1 и 1,5 и что именно здесь наиболее медленно протекает конденсация, как это было показано различными методами, в том числе изучением вязкости.
Высоцкий и Стражеско [49] отметили, что исследователи уделяли мало внимания изучению тнз или иэт кремнезема, несмотря на тот очевидный факт, что для других коллоидных систем эти характеристики являются ключевыми. Авторы напомнили о наблюдениях Фрейндлиха [2], показавших, что, в то время как в изоэлектрической точке лиофобные коллоидные системы наименее устойчивы, лиофильные коллоидные системы, в частности кремнезем, напротив будут, по-видимому, в ней наиболее стабильными. Это не совсем верно, так как коллоидный
кремнезем находится в устойчивом состоянии, когда частицы заряжены отрицательно при рН 9—10. Но как указал Фрейндлих, заметный максимум устойчивости системы во времени наблюдается при иэт около рН 2 (см. рис. 3.2).
|
|
Высоцкий и Стражеско показали также, что в присутствии какой-либо кислоты (например, серной) иэт является не только точкой минимальйой скорости процесса гелеобразования, но и синерезиса и, кроме того, точкой, в которой гели образуются наиболее прочными и с максимальной величиной удельной поверхности. Все эти характеристики получаются не только из-зз
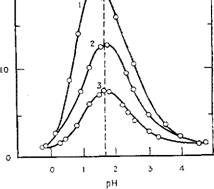
Рис. 3.4. Зависимость времен» гелеобразования от рН для золей кремневой кислоты, приготовленных из H2S04 н силиката натрия, при 25 °С и различных концентрациях золя t'no данным [49]). J — 1,09 М, 65,4 г/л Si02; 2 — 1,33 М. 79,8 г/л SiO/, 3—1,78 М, 106.8 г,'л Si02.
Того, что скорость процесса агрегации в иэт минимальна, на и потому, что скорость роста первичных частиц, образующихся из мономера, также минимальна. Следовательно, при формировании геля в иэт первичные частицы являются наименьшими по размеру.
Те же авторы отметили существование взаимосвязи между значениями рН при наиболее медленном процессе гелеобразования и рКа выбранной кислоты. Их данные показаны на рис. 3.4 и 3.5. Полученные значения рН для HN03, H2SO4 и Н2Сг04 аналогичны данным Айлера [50]. Айлер также указал ряд других сильных кислот, например NH2SO3H, НСЮ4 и CH(S03H);, дающих наиболее продолжительное время гелеобразования примерно при том же самом" значении рН, что НС1 и HN03. Однако подобное значение рН не было выявлено в случае более слабых кислот, например уксусной, хотя известно, что золь, полученный в присутствии этой кислоты, может быть наиболее стабильным при рН 3,5. Тем не менее следует отметить, что золь, приготовленный в уксусной кислоте при рН 3,5, значительно менее устойчив, чем золи, приготовленные в более сильных кислотах ПШЇ рН 1,5—2,0.
Тай и Кианг [51] получили близкие результаты и сообщили, что в соляной, серной и азотной кислотах максимальное время гелеобразования наблюдалось при рН 2, в фосфорной — 2,5 и
РКа
|
|
|
Н3Р04 |
|
HN0 |
|
РН |
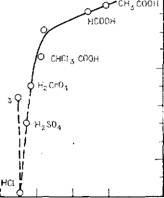
Рис, 3.5. Зависимость величин р/Са от рН при наименьшей скорости гелеобразования для различных кислот, используемых при нейтрализации силиката натрия (по данным Высоцкого и Стражеско [49]).
Кривые 1—5 — температура обработки 300, 500, 700. 900 и 1000°С соответственно.
Уксусной — 4,0. Они предположили, что скорость процесса полимеризации пропорциональна отношению
__________ [(НО) 4Si]__________
[(НО)з SiOH2+] [(HO)3SiO-j
|
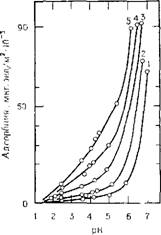
Рис. 3.6. Изоэлектрическая точка. Зависимость величины адсорбции ионов рубидия иа силикагелях, предварительно термически обработанных при различных температурах, от рН раствора (по данным Кириченко и Высоцкого [53].) |
По-видимому, значение иэт находится около рН 1,5, как на это указывают исследования, выполненные Высоцким и Стражеско [52] и Кириченко и Высоцким [53] методом ионообменной сорбции ионов рубидия из 0,1 и. раствора RbN03 на силикагелях, предварительно термически обработанных при температурах до 1000°С (рис. 3.6). Все кривые, представленные на рис. 3.6, сходятся к указанному значению рН, когда величина адсорбции равна нулю. Такой вывод сделан в работе Климен - товой, Кириченко и Высоцкого [54].
Резюмируя, необходимо отметить, что значения иэт и тнз для кремнезема, по приведенным в литературе данным, охватывают область рН 0,5—3,7. Об этом сообщает Парке [55], который цитирует 12 библиографических ссылок. Тем не менее рН 2±0,5 можно, по-видимому, принять за среднее для различных типов кремнезема — от очищенного молотого кварца до коллоидного кремнезема. Следует ожидать проявления некоторого разброса значений, зависящего от типа поверхности кремнезема (кристаллическая или аморфная), возможно, от размера частиц и главным образом от присутствия примесей. Остается невыясненным вопрос, как определять иэт\ по максимальному времени гелеобразования или по минимальной скорости убывания мономера, поскольку метод определения иэт связан с возможными механизмами полимеризации последнего.
Климентова, Кириченко и Высоцкий [54] обобщили данные, устанавливающие взаимосвязь между изоэлектрической точкой поликремневой кислоты и устойчивостью золей, скоростью гелеобразования и свойствами формируемых гелей. Можно Кратко сказать, что все подобного рода наблюдаемые явления затрагивают образование и гидролиз связей Si—О—Si и что скорости таких реакций зависят от каталитического эффекта, который минимален при рН 1,5—2,0 в присутствии анионов сильных кислот. Каталитический эффект несколько возрастает при более высоких значениях рН в присутствии анионов более слабых кислот.
На основании того факта, что скорость исчезновения мономера в процессе полимеризации имеет второй порядок при рН>2 и третий порядок при рН<2, Оккерс [29] пришел к заключению, что в первом случае играет роль анионная форма кремнезехма, а во втором — катионная. Таким образом, изоэлектрическая точка должна находиться при рН 2. Подобным же образом авторы работы [56] полагали, что изоэлектрическая точка должна находиться около рН 2, так как скорость полимеризации с каждой стороны от этой точки является функцией концентрации ионов Н+ и ОН~. В последующей работе [57] в результате исследований методом электрофореза было установлено, что иэт находилась между рН 1,0 и 1,5 для 0,5%-ного золя Si02 и при рН 2, когда золь разбавляется до 0,26%- Вязкость имела резкий минимум при рН 1,9.
При установлении связи между временем гелеобразования и константой диссоциации кремнезема были сделаны аналогичные наблюдения [58].
Все еще остается невыясненной важность величины иэт кремнезема в системе кремнезем—вода, когда в растворе помимо мономера Si(OH)4 имеются полимеризованные формы или твердые кремнеземные поверхности. Большинство данных доказывает, что в этом случае для мономерной формы Si (ОН) 4 иэт может находиться в интервале рН 2—3, а для полимерных форм — в интервале 1,5—2.