Расчет растворимости и константы диссоциации
Когда константа диссоциации и растворимость неизвестны, как, например, при некоторых необычных значениях рН, из данных по величине рН и суммарному количеству растворимого кремнезема можно легко подсчитать концентрацию ионов и растворимость [114]. Растворимый кремнезем включает в себя обе разновидности — и мономер Si(OH)4, и ионную форму, которые определяются по реакции с молибденовой кислотой. В общих чертах этот метод можно представить следующим образом:
Пусть 5j — общая концентрация растворимого кремнезема при pHj;
|
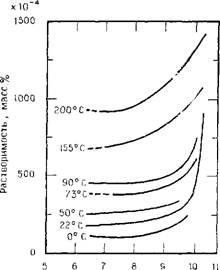
РН Рис. 1.7. Зависимость растворимости аморфного кремнезема от рН при различных температурах. (Данные Гото [167а]). |
S2 — общая концентрация растворимого кремнезема при рНг;
Sо — концентрация Si (ОН) 4, которая представляет собой растворимость кремнезема в нейтральном растворе, т. е. в чистой воде.
Тогда концентрация ионной фомы кремнезема при pHt равна
51— So, а концентрация ионной формы кремнезема при рН2 равна
52— S0. Так как уменьшение концентрации ионов Н+ сопровождается повышением концентрации ионов HaSiO - , то
51 — Sp _ Jqph,-рнг
52 — S0
Перегруппировкой получаем
S2(lOpH'-pH;)-S] __ „ 10рн,-Рн2 _ j — ъо
Концентрации силикат-иона в растворе могут быть получены вычитанием, а константа ионизации подсчитана при использовании соответствующего значения константы диссоциации чистой воды:
|
Т, °С |
С |
|
0 |
14,944 |
|
25 |
13,996 |
|
50 |
13,26 |
|
90 |
12,42 |
|
100 |
12,26 |