ТЕХНОЛОГИЯ ПОЛУЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ
Ввиду высокой химической прочности соединений лантаноидов (оксидов, галогенидов) чистые металлы или их сплавы получают методами металлотермии или электролоиза расплавленных сред.
Исходные соединения для производства металлов
Редкоземельные металлы преимущественно получают из безводных хлоридов или фторидов.
Получение хлоридов. Для получения хлоридов используют способы обезвоживания кристаллогидратов РЗЭ С13 • лН20 (выделяемых в процессе выпаривания растворов) или "сухие" методы хлорирования оксидов.
С. целью предотвращения образования оксихлоридов JL/iOCl (в результате гидролиза) обезвоживание кристаллогидратов проводят в токе сухого хлористого водорода при 400 - 450 °С. В этом случае оксихлориды превращаются в хлориды:
L/iOCl + 2НС1 = L/iCl3 + Н20. (11.10)
Сухие методы основаны на взаимодействии оксидов РЗЭ с различными хлорирующими агентами: хлором в присутствии углерода, хлоридом аммония и хлористым водородом.
Хлор в присутствии углерода и СС14 реагирует с оксидами РЗЭ при 700 - 800 °С. При этом получают расплав хлоридов. Взаимодействие с хлоридом аммония протекает при 200 - 300 °С:
Ьпг Оэ + 6NH4C1 = 21лС13 + 6NH3 + ЗН20. (ll. ll)
После окончания реакции отгоняют избыточный NH4C1 нагреванием смеси в вакууме 66,5 - 267 Па при 300 - 320 °С. Безводные хлориды РЗЭ гигроскопичны. Ввиду этого при работе с ними необходимо исключить контакт материала с влажным воздухом и хранить хлориды в атмосфере инертного газа. 364
Получение фторидов. Фториды РЗЭ получают обезвоживанием гидратированных солей, осажденных из растворов или действием фтористого водорода на оксиды РЗЭ.
Фториды РЗЭ осаждают из азотнокислых или солянокислых растворов плавиковой кислотой. Некоторые РЗЭ (лантан, церий и др.) выделяются в виде полугидратов LnҐ3 • 0,5Н20, другие (празеодим, неодим) - без кристаллизационной воды. При нагревании раствора с осадком фторидов с помощью инфракрасной лампы гидратированные фториды превращаются в безводные. Отфильтрованные и промытые спиртом осадки затем сушат при 400 °С в атмосфере сухого аргона. Полученные этим способом фториды содержат примесь оксифторидов JL/iOF. Исключить их образование можно сушкой в токе HF.
Более чистые фториды получают действием фтористого водорода на оксиды при 550 - 575 °С:
Ln203 + 6HF = 2L/iF3 + ЗН20. (11.12)
Фторирование таблеток оксидов проводят в трубе из никеля или сплава 70% Ni + 30% Си, через которую навстречу потоку газа перемещаются лодочки с оксидами. Можно проводить фторирование оксидов в кипящем слое. Фториды, в отличие от хлоридов, малогигроскопичны, что облегчает работу с ними.
Электролитическое получение редкоземельных металлов
Разработаны различные способы получения лантаноидов электролизом в расплавах солей. Среди них более распространен электролиз безводных хлоридов РЗЭ в расплавах хлоридов щелочных и щелочно-земельных металлов. Этим способом в производственных масштабах получают преимущественно мишметалл (сплав церия, лантана, неодима и др.), а также церий, иногда лантан и неодим и другие металлы цериевой группы. В процессе электролиза эти металлы выделяются на катоде в расплавленном состоянии, поскольку они имеют сравнительно низкие точки плавления.
Более сложным оказалось получение электрлизом металлов группы иттрия, которые, за исключением иттербия, имеют высокие точки плавления (от 1350 до 1700 °С). Проводить электролиз при столь высоких температурах (для получения на катоде жидкого металла) практически невозможно из-за испарения галоидных солей, а также трудностей с подбором материалов для ванны и электродов. В связи с этим металлы подгруппы иттрия не получают электролизом.
Электролиты для получения мишметалла или металлов це - риевой группы большей частью содержат смесь 50% КС1 + 50 % СаС12, отвечающую эвтектике с точкой плавления 660 °С, или смесь 50% КС1 + 50% NaCl, плавящуюся при 658 иС. В расплавах этих солей хлориды лантаноидов хорошо растворимы. Ванна содержит примерно 58 - 60% L/iCl3, остальное - хлориды щелочных и щелочно-земельных металлов. Рекомендуются небольшие добавки фтористого кальция.
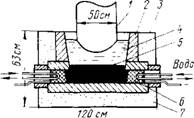
Для получения мишметалла используют электролизеры различных конструкций. Одна из них приведена на рис. 87. Внутренняя футеровка ванны - из огнеупоной керамики. Пространство между футеровкой и стальным кожухом заполнено теплоизолирующей засыпкой. У дна ванны введены водоохлаж - даемые катоды. В центре - графитовый анод. Температуру электролита - 800 - 900 °С поддерживают за счет тепла, выделяющегося при прохождении тока через расплав.
Электролиз ведут при напряжении 10 - 15 В и силе тока 1000 - 2000 А (в зависимости от размера электролизера). Выход по току составляет примерно 50 - 70%.
Жидкий мишметалл либо вычерпывают ковшом, либо выпускают все содержимое ванны в стальные изложницы, нагретые до 500 - 550 °С. После расслоения и остывания электролит возвращается в процесс.
Получаемый мишметалл или церий содержит 94 - 99 % суммы РЗЭ и ряд примесей: углерод, кальций, алюминий, до 1% кремния, 1,0 - 2,5 % железа и др. Чистоту металла можно повысить применением для изготовления электродов метал-
Ржс.87. Схема электролизной ванны для получения мишметалла: 1 — графитовый анод; 2 - огнеупорная керамика; 3 - железный кожух; 4 - электролит; 5 - жидкий мишметалл; 6 — железный катод;
Лов, не взаимодействующих с лантаноидами (молибден и особенно тантал), использованием для футеровки тигля чистых оксидов магния и бериллия, а также проведением электролиза в атмосфере инертного газа.
Металлотермические способы получения лантаноидов из галогенидов
Металлотермическим восстановлением галогенидов можно получить все лантаноиды, за исключением самария, европия и иттербия, восстановление которых протекает только до низших галогенидов. Поэтому для получения этих лантаноидов разработаны способы их восстановления из оксидов лантаном или углеродом с вакуумной их возгонкой. Для восстановления фторидов и хлоридов лантаноидов используют преимущественно кальций. Кроме того, для производства тяжелых РЗМ и иттрия используют метод восстановления литием.
Восстановление галогенидов кальцием
Восстановление галогенидов кальцием необходимо проводить при температурах выше точек плавления лантаноидов, чтобы обеспечить выплавку металлического слитка. При этом шлак должен находиться в расплавленном состоянии. Это определяет обличия в условиях восстановления таких сравнительно легкоплавких металлов, как La, Се, Pr, Nd (температуры плавления 800 - 1050 °С) и металлов иттриевой группы, плавящихся в интервале 1350 - 1650 °С (см. табл. 10).
Восстановление хлоридов. Легкоплавкие лантаноиды (La, Се, Pr, Nd) можно получить восстановлением хлоридов и фторидов кальцием. Безводные хлориды этих элементов восстанавливают с получением металлов высокой чистоты в стальных герметичных стаканах (бомбах) небольшого размера, футерованных чистым оксидом магния или доломитовой смесью оксидов кальция и магния.
Кальций высокой чистоты (очищенный дистилляцией в вакууме) в форме зерен размером ~ 0,6 - 1 мм, взятый с избытком 15 - 20%), перемешивают с хлоридом лантаноида в атмосфере сухого аргона в специальной камере. При проведении процесса в малых масштабах теплоты реакции недостаточно для обеспечения расплавления образующегося металла и шлака. С целью повышения термичности процесса в шихту добавляют в качестве подогревающей добавки иод (0,3 - 0,7 моля на 1 моль хлрида) и соответствующее количество кальция для образования Са12 (теплота образования Са12 538 кДж/моль).
Герметично закрытую бомбу с шихтой нагревают до 700 °С для возбуждения реакции. Металлы получаются в виде плотного слитка, хорошо отделяющегося от шлака, при среднем выходе 95%. Они содержат около 2% кальция, который удаляется переплавкой металла в вакууме в тиглях из оксида магния, оксида бериллия или тантала.
В случае необходимости ведения восстановления выше 1200 °С (например, для гадолиния) тигли из оксида магния непригодны. Наиболее инертным материалом по отношению к лантаноидам явяется тантал, практически не реагирующий с большей частью этих металлов вплоть до 1500 - 1600 °С.
Росстановление ведут в сварном танталовом тигле, закрытом дырчатой крышкой, в атмосфере аргона. Тигель нагревают токами высокой частоты (в шихту не добавляют подогревающей добавки). Металлы плотно пристают к танталу и приходится механически отделять от них танталовую оболочку. В целях экономии тантала тигли изготовляют из тонких листов толщиной 0,02 - 0,06 мм.
Восстановление фторидов. Для получения тугоплавких лантаноидов (Tb, Dy, Но, Er, Tu, Lu, Y) способ восстановления хлоридов непригоден. Основное затруднение состоит в высоком давлении пара хлоридов РЗЭ при 1500 - 1600 °С, необходимых для получения слитков. Более высокие точки кипения, чем хлориды, имеют фториды лантаноидов. Кроме того, фториды имеют преимущество перед хлоридами в том отношении, что они малогигроскопичны.
Восстановление фторидов кальцием проводят в танталовых тиглях в атмосфере аргона. Кальций и фторид РЗЭ смешивают при возможно меньшем контакте с атмосферой. В шихту вводят кальций с избытком 10% против необходимого для реакции восстановления:
2L/iF3 + ЗСа = 2Ln + 3CaF2. (11.13)
Шихту набивают в предварительно дегазированный нагреванием в вакууме танталовый тигель, который ставят в кварцевую трубу вакуумной индукционной печи. Для удаления газов из шихты тигель медленно нагревают в вакууме до 600 °С. При этой температуре впускают чистый аргон до давления 66,5 кПа (500 мм рт. ст.) и продолжают нагрев до температуры, при которой начинается активное взаимодействие фторида с кальцием. Эта температура в зависимости от получаемого металла составляет 800 - 1000 °С. Хотя реакция экзотермическая, но тепла не хватает для достижения необходимой конечной температуры и нагрев продолжается. Чтобы получить хороший выход в слиток, температура в конце процесса должна быть выше температуры плавления металла и шлака (точка плавления CaF2 1418 °С). Для легких РЗЭ, а также гадолиния, тербия и диспрозия достаточна температура 1450 °С, для более тугоплавких РЗЭ - на 50 °С выше точки их плавления.
369
По достижении температуры активного взаимодействия реакция заканчивается за несколько минут; затем максимальную температуру поддерживают в течение 15 мин для хорошего отделения металла от шлака. В этих условиях выход металла в слиток достигает 97 - 99%. После охлаждения хрупкий шлак легко отделяется от слитка. Основная примесь в слитке - кальций, содержание которого составляет 0,1 - 2 %. Для его удаления слиток плавят в вакууме в том же танталовом тигле.
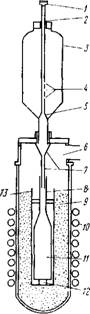
Рис.88. Схема аппарата для восстановления фторидов РЗМ кальцием:
1 - смотровое окошко; 2 - подвижное уплотнение; 3 - загрузочная воронка из стекла пирекс; 4 - отверстия для эвакуации загрузочной воронки и шихты; 5 - затвор; 6 - патрубок для очистки или подачи аргона; 7 - танталовый патрубок для подачи шихты; 8 - танталовая трубка; 9 - теплоизоляция из дробленого графита; 10 - индукционная катушка; И - танталовый тигель; 12 - подставка под тигель; 13 - стакан, ограничивающий теплоизоляцию
13-1325
Содержание тантала в легких лантаноидах (от лантана до неодима) составляет 0,02 - 0,03 %, в тяжелых лантаноидах 0,1 - 0,5 %. Содержание других примесей, %: Са 0,01 %; N 0,005; О 0,1 - 0,03; С 0,0075; F 0,005.
С целью увеличения количества единовременно получаемого металла можно проводить процесс с догрузкой шихты в танталовий тигель по мере того, как шихта реагирует и плавится (рис. 88).
Литиетермический способ восстановления РЗМ из хлоридов
Метод используют для получения тяжелых РЗМ, иттрия, имеющих высокие точки кипения.
Все щелочные - металлы восстанавливают РЗМ из их хлоридов, однако литий обладает преимуществом по сравнению с натрием и калием - более высокой температурой кипения (у лития, натрия и калия Гкип равны 1370, 833 и 760 °С соответственно).
Полное восстановление хлоридов литием происходит при 800 - 1000 °С. При этом тяжелые РЗМ и иттрий находятся в твердом состоянии, что является преимуществом по сравнению с кальциетермическим способом. Поскольку LiCl плавится при 614 °С, его можно удалить сливом с последующей вакуумной сепарацией оставшегося в губчатом металле хлорида (у LiCl tma = 1380 °С).
Описаны различные варианты литиетермического восстановления хлоридов РЗМ. Для получения металла технической чистоты применяют способ прямого взаимодействия жидкого лития с двойной солью ЗКСІ • L/iClj (соли с YC13, YbCl3, ТЬС13 и LnC\3 имеют точки плавления 780, 825, 810 и 816 °С соответственно). Двойной хлорид в виде кусков помещают в ниобиевый стакан, устанавливаемый в стальной реактор. Герметизированный реактор вакуумируют и заполняют аргоном. Реактор нагревают до 200 °С, затем из бачка - плавильника в реактор подают жидкий литий (їпл = 180,5 °С). Вследствие экзотермичности реакции происходит разогрев реагирующих веществ до 700 °С. Образующийся жидкий LiCl с помощью вакуумного сифона сливают в изложницу.
Оставшийся хлорид (~ 20 %) удаляют вакуумной сепарацией. После охлаждения реторты во избежание возгорания губки РЗМ выдерживают в атмосфере технического аргона для пассивирования поверхности (образование пленки оксида в результате взаимодействия с примесью кислорода в аргоне).
Металл после переплавки в дуговой печи содержит, % (по массе): О 0,3 - 0,4; С1 0,01; С 0,02; Fe 0,01 - 0,03; Nb 0,001.
Восстановление самария, европия и иттербия из оксидов
Выше сказано, что самарий, европий и иттербий не удается получить восстановлением из галогенидов вследствии того, что процесс протекает только до образования дихаль - когенидов. Эти металлы получают восстановлением из оксидов лантаном или углеродом.
Ланганотермический метод. Восстановление оксидов самария, европия и иттербия лантаном проводят в вакууме с одновременной дистиляцией образующихся металлов, которые имеют более высокое давление пара, чем лантан (см. табл. 10):
Sm203 + 2La = 2Sm* + Ьа2Оэ. (11.14)
По одному из описаний восстановление ведут в высоком танталовом тигле, в верхней части которого установлен охлаждаемый воздухом медный конденсатор (для предотвращения загрязнения медью поверхность конденсатора покрывают тонким слоем оксида получаемого металла. Для обмазки используют суспензию оксида в спирте). Смесь оксида с лантано - вой стружкой (взятой с избытком - 20%) помещают в танталовый тигель, нижнюю часть которого нагревают в вакуумной индукционной печи до 1400 °С. В процессе нагрева поддерживают вакуум не ниже 1,33 • 10"2Па. Начало возгонки сопровождается резким падением давления (до 1,33 10~5Па), так как испаряющиеся металлы активно поглощают остаточные газы. Конденсацию ведут при 300 - 400 °С. В этом случае металл получается в форме крупнокристаллической корки. При более низких температурах образуется порошкообразный металл.
Получаемые самарий, европий и иттербий практически не содержат тантала и лантана. Содержание примесей С, N, О и
Н не превышает 0,01 %. Вместо лантана в качестве восстановителя можно использовать церий или мишметалл.
Карботермический способ. Способ включает две стадии:
Восстановление ЬпгОг углеродом при 1600 - 1700 °С с получением карбида:
Ln203 + 7С = 2LnC2 + ЗСО; (11.15)
Диссоциацию карбида в вакууме с возгонкой лантаноида:
LnC2 = L/i* + 2С. (11.16)
Метод применяют для получения самария, европия и иттербия, которые отличаются относительно низкими температурами кипения (1900, 1400 и 1430 °С соответственно).
Процесс ведут в графитовом тигле, куда загружают брикетированную смесь оксида с углеродом (сажей), взятым с 10%-ным избытком. Тигель помещен в вакуумную печь, нагрев индукционный.
Первую стадию ведут при разрежении в печи 13,3 Па при 1600-1700 °С, выдерживая шихту при этой температуре ~3 ч. В результате получают карбид лантаноида. Вторую стадию проводят при остаточном давлении ОДЗПа и температуре 1600-1900 °С. В результате диссоциации карбида самарий летит и осаждается на охлаждаемом конденсаторе, изготовленном из тантала или молибдена. Полученный этим методом самарий содержит, %: С 0,05; О 0,1; Н 0,035, N < 0,1.
Очистка редкоземельных металлов дистилляцией
Рафинирование редкоземельных металлов, полученных одним из описанных способов, можно осуществить дистилляцией в вакууме. Этот метод эффективен для очистки тугоплавких металлов иттриевой группы и самого иттрия.
Металл помещают в танталовый тигель, соединенный с танталовым конденсатором. Тигель с конденсатором помещают в кварцевую трубу, соединенную с вакуумной системой. Тигель нагревают с помощью индуктора. Плавка ведется при вакууме ^0,0013 Па. При плавке диспрозия, гольмия, эрбия поддерживают температуру в тигле 1600-1700 °С, конденсатора - 900-1000 °С. Для более тугоплавких металлов - иттрия, тербия, лютеция - 2000-2200 °С и 1300-1400 °С соответственно. 372