КОТЕЛЬНЫЕ УСТАНОВКИ И ПАРОГЕНЕРАТОРЫ
Кристаллизация веществ из раствора
Процесс кристаллизации состоит из двух стадий: образование центров кристаллизации (зародышей) и рост кристаллов (зародышей). Зародышами
|
Таблица 12.4. Допустимые значения показателей работы блока СКД, определяемые качеством водно-химического режима
|
Могут служить не только самопроизвольно образовавшиеся частицы самого вещества, но (центрами кристаллизации) любые другие частицы, способные адсорбировать на своей поверхности молекулы или ионы кристаллизующегося вещества. Такого типа центры всегда присутствуют на поверхности труб и в объеме водного теплоносителя. Поэтому первая стадия кристаллизации в реальных условиях не лимитирует скорость всего процесса.
JPoct кристаллов определяется двумя процессами: диффузией строительных частиц к поверхности кристалла и введение их в определенные места кристалла.
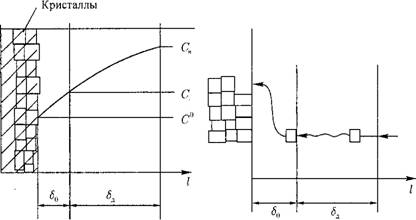
Рассмотрим изменение концентрации примеси вблизи поверхности кристалла (рис. 12.50).
На поверхности кристалла концентрация примеси соответствует растворимости вещества С° при температуре в данной точке (на поверхности кристалла, трубы и т. д.).
Около кристалла находится поверхностный слой жидкости толщиной So, в пределах которого действуют силы ван-дер-ваальсовского, электростатического взаимодействия между молекулами твердой фазы и жидкости. Этот слой жидкости практически неподвижен.
Поверхностный слой жидкости контактирует с диффузионным пристенным слоем толщиной <5д, в котором перемещение примеси (в молекулярной или дисперсной форме) происходит за счет диффузии под воздействием градиента концентрации (точнее — градиента химического потенциала). На
Рис. 12.50. Изменение концентрации примеси около поверхности кристалла в процессе кристаллизации вещества из раствора.
Границе этих слоев концентрация примеси С*. Дальше располагается ядро потока (в двухслойной модели пристенного слоя) с концентрацией примеси Сп.
Интенсивность доставки вещества через диффузионный слой к поверхности кристалла </д, кг/(м2с), рассчитывается по уравнению Фика
Где Дк — коэффициент диффузии, рассчитанный по'средней температуре жидкости в диффузионном слое.
|
500 ГЛАВА 12
Рис. 12.51. Схема процесса собственно кристаллизации вещества. |
Принимая, что изменение концентрации примеси в диффузионном слое близко к линейному, преобразуем (12.78):
-вд-зд^дй-а)
Процесс собственно кристаллизации вещества можно разделить на два этапа (рис. 12.51): адсорбция частицы поверхностью, миграция ее в поверхностном слое жидкости к свободному месту в кристаллической решетке,
внедрение в кристаллическую решетку Этот процесс обычно описывается уравнением химической реакции первой степени
JKp = Кр(Сі-С°), (12.80)
Где JKp — скорость роста кристалла, кг/(м2с); Кр — константа скорости реакции.
Константа скорости реакции зависит от вещества, коэффициента диффузии частицы в поверхностном слое DCT (по температуре стенки), кристаллической решетки, дефектов в ней и т. д.
В стационарном режиме 7Д = JKp = J. Результирующий поток будет равен
J = Ккр(Сп — С0), (12.81)
Где Ккр — коэффициент скорости кристаллизации. Исключим из (12.79) и (12.80) концентрацию Сі.
Из<12-79 •■с°-с< = Чтй)>
|
Cn~c° = J(jDjs:) + 'k)- |
Из (12.80): С, - С° = Лр(^). После сложения
Или
П--П<> = .т(
'(АкЛд) к^
Сопоставление полученного выражения с (12.81) показывает, что
Ккр - (ВД,) + кр (12-82)
Отсюда коэффициент скорости кристаллизации будет равен
Ту - __ ______ 1______ __ _____ ^ж_____________ / 1 2
Кр SjDn + 1/Кр {5а -f Дк/Кр) 1 ■
Коэффициент скорости кристаллизации определяется скоростью доставки примеси к месту кристаллизации и скоростью самого процесса кристаллизации.
Если скорость доставки значительно меньше скорости реакции (Дс/5д <^.Кр), то Ккр « Дк/5д, т. е. весь процесс кристаллизации контролируется доставкой вещества. Наоборот, при Кр < DyK/SJX коэффициент
Ккр ~ Кр. Следовательно, процесс кристаллизации какого-либо вещества из раствора на твердой поверхности определяется стадией, идущей с наименьшей скоростью.
Введем понятие пересыщения раствора (3
(С - С°)
/З-1-^. (12.84)
Тогда скорость кристаллизации
^^"(кткщ)^ (12-85>
При больших пересыщениях скорость собственно кристаллизации высока и лимитирующей стадией становится диффузия вещества к поверхности кристалла. Доставка вещества к кристаллу ограничивает скорость его роста и при высоких температурах, так как с увеличением температуры Кр растет. Для водных растворов солей и некоторых веществ органического происхождения диффузия контролирует рост кристаллов при температуре выше 45-50°С.
С уменьшением пересыщения возрастает роль процесса собственно кристаллизации. Рост кристаллов происходит и при очень маленьких пересыщениях. Этот процесс связан с наличием дефектов в структуре и дислокациями в растущем Кристалле. К дефектам относятся трещины, изломы, шероховатости поверхности. При пересыщении порядка [3 « 10~3 и выше скорость роста кристаллов может быть представлена в виде зависимости
J — йкрДк/ЗС0, (12.86)
Где акр характеризует опорные размеры кристалла.
Как видно из анализа процесса кристаллизации, в доставке вещества и собственно кристаллизации существенную роль играют диффузионные процессы. При Дк « 0 Ккр « 0, кристаллизация вещества происходить не будет. Если же DCT « 0, то Кр « 0, т. е. при наличии примеси около поверхности твердой фазы сам процесс кристаллизации не происходит.
Когда возможны эти случаи в паровых котлах?
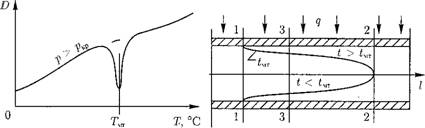
При сверхкритическом давлении в зоне максимальной теплоемкости (рис. 12.52) происходит резкое снижение коэффициента диффузии вещества в водном теплоносителе. Это связано с коренной перестройкой структуры воды, когда подвижность ее молекул и коэффициент самодиффузии воды резко снижаются.
Рассмотрим изменение температуры водного теплоносителя при сверхкритическом давлении по длине обогреваемой трубы в какой-то момент времени. На рис. 12.53 показано, что в сечении 1-1 температура воды становится равной температуре максимальной теплоемкости Тмт у поверхности
|
Рис. 12.52. Зависимость коэффициента. Рис. 12.53. Граница температуры макси - диффузии вещества в водном теплоно - мальной теплоемкости Тмт в потоке вод - сителе при сверхкритическом давлении ного теплоносителя, от температуры. |
Трубы, а затем, по мере прогрева среды, зона с Тмт проникает все дальше по сечению трубы, пока ядро потока (в сечении 2-2) не прогреется до этой температуры.
Когда температура среды в поверхностном слое у кристалла близка к Тмт (в районе сечения 1-1 на рис. 12.53), DCT резко снижается, что тормозит сам процесс кристаллизации (рис. 12.54). Дальше по ходу среды DCT увеличивается, рост кристалла возобновляется. Но зона Тмт смещается в диффузионный пристенный слой, Дк и скорость доставки резко уменьшаются (условно сечение 3-3 на рис. 12.53), что приводит к снижению скорости роста кристалла (рис. 12.54, сечение 3-3).
Таким образом, при изменении температуры водного теплоносителя СКД по длине трубы возможны участки, где скорость кристаллизации примеси и, следовательно, роста массы отложений на поверхности трубы замедляется из-за снижения скорости диффузии вещества.