КОТЕЛЬНЫЕ УСТАНОВКИ И ПАРОГЕНЕРАТОРЫ
Горение твердого топлива
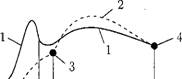
Горение твердого топлива (угольной пыли) включает два периода: тепловую подготовку и собственно горение (рис. 4.5). В процессе тепловой подготовки (рис. 4.5, зона I) частица топлива прогревается, высушивается и при температуре выше 110°С начинается тепловое разложение исходного вещества топлива с выделением газообразных летучих веществ. Длительность этого периода зависит главным образом от влажности топлива, размера его частиц, условий теплообмена и составляет обычно десятые доли секунды. Протекание процессов в период тепловой подготовки связано с поглощением тепла, главным образом, на подогрев, подсушку топлива и термическое разложение сложных молекулярных соединений, поэтому нагрев частицы в это время идет замедленно.
|
Веществ и находится по приближенной формуле |
|
Тг п |
|
|
|
(4.15) |
Собственно горение начинается с воспламенения летучих веществ (рис. 4.5, зона II) при температуре 400-600°С, а выделяющаяся в процессе их горения теплота обеспечивает ускоренный прогрев и воспламенение твердого коксового остатка. Горение летучих веществ занимает 0,2-0,5 с. При большом выходе летучих (бурые и молодые каменные угли, сланцы, торф) выделяющейся теплоты их горения достаточно для воспламенения коксовой частицы, а при малом выходе летучих возникает необходимость дополнительного прогрева коксовой частицы от окружающих раскаленных газов (зона III).
Горение кокса (рис. 4.5, зо - на IV) начинается при температуре около 1 000°С и является наи - 50лее длительным процессом. Это определяется тем, что часть кислорода в зоне у поверхности частицы уже израсходована на сжигание горючих летучих веществ и оставшаяся концентрация его снизилась, кроме того, гетерогенные реакции всегда уступают по скорости гомогенным для однородных по химической активности веществ.
В итоге общая длительность горения, твердой частицы (1,0-2,5 с) в основном определяется горением коксового остатка (около 2/3 общего времени горения). У молодых топлив, имеющих большой выход летучих веществ, коксовый остаток составляет менее половины начальной массы частицы, поэтому их сжигание (при равных начальных размерах) происходит достаточно быстро и возможность недожога снижается. Старые по возрасту топлива имеют плотную коксовую частицу, горение которой занимает почти все время пребывания в топочной камере.
Коксовый остаток большинства твердых топлив в основном, а для ряда твердых топлив почти целиком состоит из углерода (от 60 до 97% массы частицы). Учитывая, что углерод обеспечивает основное тепловыделение при сжигании топлива, рассмотрим динамику горения углеродной частицы с поверхности. Кислород подводится из окружающей среды к частике углерода за счет турбулентной диффузии (турбулентного массоперено-
|
|
|
III |
|
II |
|
IV |
|
Рис. 4.5. Температурный режим при горении отдельной частицы твердого топлива: 1 - температура газовой среды вокруг частицы; 2 - температура частицы; 3 — воспламенение коксового остатка; 4 — завершение горения коксового остатка; 1 — зона термической подготовки; II — зона горения летучих веществ; III — зона «прогрева коксового остатка; IV — зона горения коксового остатка. |
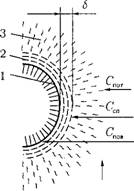
Имеющего достаточно высокую интенсивность, однако непосредствен - Но У поверхности частицы сохраняется тонкий газовый слой (пограничный Сл°й), перенос окислителя через который осуществляется по законам молекулярной диффузии (рис. 4.6). Этот слой в значительной мере тормозит подвод кислорода к поверхности. В нем происходит догорание горючих 1 азовых компонент, выделяющихся из частицы в ходе термического разложения. Количество кислорода, подводимого в единицу времени к единице Поверхности частицы посредством турбулентной диффузии определяется
По формуле
|
Go |
= Л(СП0Т-Ссл). (4.16)
|
Газовоздушный поток |
|
Рис. 4.6. Схема горения углеродной частицы: 1 — поверхность углеродной частицы; 2 — ламинарный пограничный слой; 3 — зона турбулентного потока. |
|
Go |
Такое же количество кислорода диффундирует через пограничный слой толщиной 5 посредством молекулярной диффузии:
/^(Ссл С|тов)
(4.17)
В (4.16) и (4.17) Спот ~ концентрация кислорода в окружающем частицу потоке; Ссл — то же на внешней границе пограничного слоя; Спов — то же на поверхности топлива; S — толщина пограничного слоя; D — коэффициент молекулярной диффузии через пограничный слой; А — коэффициент турбулентного массообмена.
|
Сок — |
Совместное решение уравнений (4.16) и (4.17) приводит к выражению
1
(Спот-Спов) (4.18,а)
1/A + 5/D
Или
|
G0 |
|
(4.18,6) |
^д(Спот СПОв) 5
В котором
AD
1/A + 5/d (A6 + D)
— обобщенная константа скорости диффузии.
|
(4.19) |
Из формул (4.18, а) и (4.18,6) следует, что подвод кислорода к реагирующей поверхности твердого топлива определяется константой скорости диффузии и разностью концентраций кислорода в потоке и на реагирующей поверхности.
|
(4.20) |
В установившемся процессе горения количество кислорода, подводимого диффузией к поверхности реагирования, равно его количеству, прореагировавшему на поверхности в результате химической реакции. Отсюда скорость реакции горения углерода с поверхности Ks из равенства массовых скоростей двух процессов — диффузионного подвода и расхода кислорода на поверхности в результате химической реакции:
Ks ~ /3/гл(С,,0Т — Спов) — /ВД.
Где дополнительно (і — отношение расхода углерода и кислорода в химической реакции. Так, например, в реакции С+О2 =С02 значение Р = 12/32 = -. 0,375.
Из уравнения (4.20) можно получить приведенную константу скорости і прения Кп учитывающую как условие диффузии, т. е. значение кд, гак и интенсивность химической реакции кр:
К кЛ (4 21)
Величина, обратная константе скорости горения, 1/Кг представляет собой общее сопротивление процессу горения.
В соответствии с законом Аррениуса, определяющим параметром скорости химической реакции, является температура процесса. Константа скорости диффузии /сд достаточно слабо изменяется с ростом температуры (рис. 4.1,а), в то время как константа скорости реакции /ср — весьма сильно (экспоненциальная зависимость). При относительно невысокой температуре для топки (800-1 000°С) химическая реакция протекает медленно, несмотря на избыток кислорода около твердой поверхности, так как кр < кд. В этом случае горение тормозится кинетикой химической реакции, поэтому эту зону температур называют областью кинетического горения. Наоборот, при высоких температурах горения (выше 1 500°С) и сжигании угольной пыли значение /сд <С кр и процесс горения тормозится условиями подвода (диффузии) кислорода к поверхности частицы. Этим условиям соответствует область диффузионного горения. Создание в этой зоне температур факела дополнительных условий для перемешивания горящей смеси (приводящей к увеличением значения кд) способствует ускорению и углублению выгорания топлива.
Аналогичный эффект в части интенсификации горения достигается уменьшением размера частиц пылевидного топлива. Частицы малых размеров имеют более развитый тепломассообмен с окружающей средой и, таким образом, более высокое значение /ед. Повышение температуры приводит к смещению процесса окисления в область диффузионного горения, так как быстро растет константа /ср.
Область чисто диффузионного горения пылевидного топлива характерна для ядра факела, отличающегося наиболее высокой температурой Прения, и зоны догорания, где концентрации реагирующих веществ уже малы и их взаимодействие определяется законами диффузии. Воспламенение любого топлива начинается при относительно низких температурах, в Условиях достаточного количества кислорода, т. е. в кинетической области. ^ этой области горения определяющую роль играет скорость химической Реакции, зависящая от таких факторов, как реакционная способность топлива и уровень температуры. Влияние аэродинамических факторов в этой области горения незначительно.