Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Конверсионные способы получения сульфата калия
Рассмотрим конверсионный способ получения сульфата калия Иа примере взаимодействия хлористого калия с эпсомитом:
2КС1 + MgS04 MgClj + K2S04
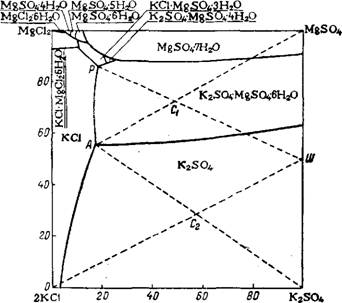
Процесс ведут в две стадии с образованием на первом этапе шенита92. Для получения максимального выхода шенита точка Сi (рис. 50) состава исходной смеси должна лежать на луче кристаллизации ШР, идущем из полюса шенита Ш в точку Р, положение которой соответствует составу маточного раствора, насыщенного шенитом, КС1 и каинитом. Раствор Р — шенитовый щелок сбрасывают, а шенит обрабатывают хлоридом калия в водной среде с образованием сульфата калия и маточного раствора А, насыщенного хлоридом калия, сульфатом калия и шенитом. Этот раствор полностью используют в первой стадии конверсии и цикл, таким образом, замыкается. Для получения высококачественного сульфата калия (~52% К2О) целесообразно использовать хлорид калия с Высоким содержанием основного вещества 93.
Разработан ряд вариантов рассмотренной схемы. Для повышения степени использования калия проводят выпарку и охлаждение шенитовых щелоков с выделением калийных солей в виде хлорида калия и леонита, возвращаемых в цикл. Выпарка и охлаждение
|
Рис. 50. Растворимость в водной системе 2KCl+MgS04 < K2S04 + MgCl2 при 25°. |
Маточных растворов с выделением возвратных солей могут быть проведены также при одностадийной конверсии с прямым получением сульфата калия. При выпуске части шенита без разложения, степень использования калия повышается, так, например, при получении всей продукции в виде сульфата калия она составляет 70%, а при выпуске только товарного шенита — 87%. Повышение степени использования калия до 87% с выработкой только сульфата калия возможно при выпарке шенитового щелока; расход пара при этом составляет 0,45 т на 1 т К2О.
Процесс конверсии мирабилита (или безводного сульфата) с Хлористым калием аналогичен рассмотренному выше. Конверсию осуществляют в две стадии с образованием промежуточного соединения—глазерита. Глазерит полностью или частично разлагают на сульфат калия. Маточные растворы после выделения глазерита могут быть переработаны на поваренную соль, при этом выделяются возвратные калийные соли (смесь глазерита и хлористого калия), которые используют в основном цикле переработки 94-95.
Промышленное получение сульфата калия на основе хлористого калия и эпсомита осуществляется на калийных предприятиях ГДР при комплексной переработке хартзальцевых руд45. Отвал после переработки руд на хлористый калий, содержащий галит, кизерит и ангидрит, подвергают быстрой промывке водой, при этом галит, скорость растворения которого значительно выше, чем у кизерита, практически полностью растворяется. Затем растворяют кизерит при 75°. При охлаждении раствора кристаллизуется эпсомит, который конвертируют с КС1 в K2SO4 в две стадии, через шенит. Часть шенита смешивают с ангидритом, сушат и выпускают в качестве товарной продукции под названием «реформкалий»; содержание К2О в этом продукте составляет 26—30%. В товарном сульфате калия содержится после сушки 48% К2О.
Конверсионные методы получения сульфата калия в США основаны на переработке хлористого калия с лангбейнитом или беркеи - том79.
В последние годы в Канаде организовано производство сульфата калия на базе природного сульфата натрия и хлористого калия79. При конверсии на сульфат калия астраханитовых солей процесс можно вести через промежуточные соединения — шенит и глазерит или их смеси.
Сульфат калия может быть получен также из стехиометриче - ской смеси хлористого калия и сульфата аммония. Образующийся при этом хлористый аммоний возгоняется в токе инертного газа или водяного пара96.
Сульфат калия может быть получен ионообменным способом, например, при пропускании горячего (90°) раствора MgS04 через К-катионит:
2RK + MgS04 R2Mg + K2S04
При охлаждении раствора до 10° из него кристаллизуется K2SO4. Регенерацию катионита можно осуществить, обрабатывая его раствором хлористого калия:
R2Mg + 2KCl ^ 2RK + MgCl2
Суммарное уравнение процесса:
2КС1 + MgS04 ^ K2S04 + MgCl2