Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ РАЗЛОЖЕНИЯ ФОСФАТОВ АЗОТНОЙ КИСЛОТОЙ
Впервые еще в 1908 г. Д. Н. Прянишников высказал соображения о целесообразности азотнокислотного разложения фосфатов. Однако в то время, в условиях отсутствия производства дешевой азотной кислоты, этот метод переработки фосфатов не мог быть реализован. Возможность получения азотных и фосфорных удобрений путем азотнокислотного разложения фосфатов приобрела реальную основу лишь в 20-е годы, когда стало быстро развиваться производство азотной кислоты из синтетического аммиака.
Азотнокислотная переработка фосфатов заключается в разложении фосфатов азотной кислотой и последующей переработке образующегося раствора (вытяжки), содержащего нитрат кальция и свободную фосфорную кислоту. В зависимости от метода переработки, вытяжки можно получать как односторонние азотные и фосфорные удобрения, так и сложные, двойные или тройные удобрения с самым широким диапазоном соотношения питательных веществ 28-32.
Разложение фосфатов азотной кислотой является сложным процессом, протекающим согласно следующему основному уравнению33-35:
Ca5(P04)3F + IOHNO3 = ЗН3Р04 + 5Ca(N03)2 + HF
Содержащиеся в фосфатах примеси — карбонаты кальция и магния, окислы железа, алюминия и редких земель и фторид кальция также взаимодействуют с азотной кислотой с образованием нитратов:
(Mg, Ca)C03 + 2HN03=(Mg, Ca)(N03)2 + С02 + Н20 R203 + 6HN03 = 2R(N03)3 + 3H20 CaF2 + 2HN03 = Ca(N03)2 + 2HF
Окислы железа и алюминия разлагаются также выделяющейся фосфорной кислотой с образованием не растворимых в воде фосфатов, что приводит к потере Р205 36:
Fe203 +. 2Н3Р04 = 2FeP04 + ЗН20 |
А1203 4- 2Н3Р04 = 2А1Р04 + ЗН20- 1
Поэтому фосфаты, содержащие больше 12% Fe203 (по отношению к Р2О5), считаются пригодными к химической переработке Только после предварительного обогащения.
Присутствие в фосфатах AI2O3 не так вредно, как РегОз, однако также нежелательно, так как это приводит к загрязнению раствора фосфорной кислоты (вытяжки). Выделяющийся фтористый водород взаимодействует с кремневой кислотой, всегда сопутствующей фосфатам, и обычно остается в растворе в виде кремнефтористоводородной кислоты. Присутствующие в небольших количествах в апатитовом концентрате нефелин и эгерин также разлагаются азотной кислотой:
KAIS1O4 • 4NaAlSi04. ReSi02 + 20HN03 = = KNO3 + 4NaN03 + 5Al(N03)3 + «Si02 + 10H20 Na20 . Fe203 • 4Si02 + 8HNO3 = 2NaN03 + 2Fe(N03)3 + 4Si02 + 4H20
Для полного разложения природных фосфатов процесс необходимо вести в присутствии стехиометрической нормы азотной кислоты, взятой из расчета на СаО в апатите или на СаО и MgO в фосфоритах 37.
Если количество азотной кислоты меньше стехиометрического и соответствует реакциям
2Ca5(P04)3F + 14HN03 = 3Ca(H2P04)2 + 7Ca(N03)2 + 2HF Ca5(P04)3F + 4HN03 = 3CaHP04 + 2Ca(N03)2 + HF
То первая из этих реакций будет проходить только при концентрации исходной азотной кислоты не ниже 60%. Вторая реакция в обычных условиях практически не идет.
Скорость гетерогенного процесса разложения природных фосфатов азотной кислотой в значительной степени определяется величиной поверхности соприкосновения реагентов. Практически степень измельчения фосфатов устанавливают, учитывая не только продолжительность их разложения, но и расходы, связанные с их измельчением 38>39.
Существенное влияние на скорость разложения фосфатов оказывают консистенция пульпы и концентрации реагирующих композитов. Оптимальная концентрация раствора характеризуется его плотностью, которая не должна превышать 1,55 г/см3. Чтобы избегать изменения установившихся концентраций, осуществляют хорошее перемешивание фосфата и кислоты. Перемешивание обычно производят механическим способом. Применение для этого сжатого в°здуха связано с усилением вспенивания раствора. Образование пены происходит вследствие выделения газообразных продуктов Реакции — двуокиси углерода, фтористого водорода, паров воды и окислов азота, получающихся при частичном разложении азотной ислоты органическими примесями, которые содержатся в природных
фосфатах. Перемешивание же раствора путем циркуляции с помощью центробежного насоса сопряжено с трудностями, возникающими при эксплуатации насосов в условиях сильно агрессивной среды (раствор азотной и фосфорной кислот) и из-за наличия твердой фазы (шлама).
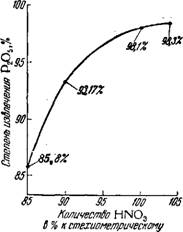
Скорость разложения трикальцийфосфата и степень извлечения Р2О5 в раствор зависят от количества применяемой азотной кислоты 40~44.
На рис. 386 показана степень извлечения Р2О5 из кролевецкого фосфорита при обработке его разными количествами азотной кислоты в течение 30 мин (15 мин приливание и 15 мин смешение) с изменением при этом температуры от 17—20° до 40—52°42.
При стехиометрическом количестве азотной кислоты, по мере протекания реакции разложения, скорость ее постепенно замедляется вследствие накопления в растворе солей 45 и уменьшения кислотности раствора. Для обеспечения постоянной скорости разложения процесс обычно проводят при 2—5%-ном избытке азотной кислоты против стехиометрического количества. В некоторых случаях избыток азотной кислоты увеличивают до 20—50% —это необходимо для обеспечения последующих операций переработки полученного раствора в удобрение.
|
Рнс. 386. Влияние количества HN03 На степень извлечения Р205 из фосфата. |
|
|
|
С? 100
Э 4* ■Е 95 |
|
40 50 |
|
Рис. 387. Зависимость степени извлечения Р205 из апатитового концентрата от концентрации азотной кислоты. Продолжительность процесса: загрузка 30 мин и перемешивание 1 ч 30 мин-, температура 40—50°. Числа на кривык — количество кислоты в % от стехиометрического. |
|
90 |
|
30 |
|
Концентрация HNOj,% |
Обычно разложение природных фосфатов ведут при температуре 45—50°, которая является оптимальной 4I. При уменьшении температуры (ниже 45°) разложение замедляется. С повышением температуры уменьшается вязкость раствора, улучшаются условия диффузии вещества и скорость разложения увеличивается 46. Однако выше 50° резко усиливается коррозия аппаратуры. Требуемая температура (45—50°) поддерживается главным образом за счет теплового
эффекта реакции; температуру азотной кислоты, которая должна составлять 30°, регулируют подогревом или охлаждением кислоты в теплообменнике.
Степень извлечения P20s в раствор мало зависит от концентрации кислоты (рис. 387) 47.
|
ТАБЛИЦА 93 Растворы, получаемые при разложении природных фосфатов азотной кислотой
|
В табл. 93 приведен примерный состав растворов, получаемых в результате разложения фосфатов азотной кислотой при 20%-ном ее избытке против стехиометрического количества (из расчета на СаО) и при коэффициенте разложения для Р205, СаО, MgO и R2O3 — 0,98, для фтора — 0,95 и для Fe203 — 0,70.