Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Адиабатическая абсорбция хлористого водорода
Наиболее совершенным является способ абсорбции хлористого водорода без отвода тепла, называемый также способом Гаспа - ряна110,111, доказавшего ошибочность мнения о невозможности получить при этом соляную кислоту концентрированнее 20,24%- Принцип, лежащий в основе способа, заключается в следующем. Если пропускать в воду хлористый водород, то за счет теплоты растворения температура образующейся соляной кислоты начнет повышаться, что приведет к увеличению давления ее паров. Когда общее давление пара станет равным внешнему, например, атмосферному давлению, жидкость закипит и начнется интенсивное испарение воды. Затрата тепла на испарение воды в адиабатических условиях вызовет снижение температуры, кипящей кислоты и поэтому концентрация ее, являющаяся функцией температуры, начнет при дальнейшей подаче хлористого водорода возрастать.
На рис. 111 приведены кривые общего давления пара над соляной кислотой разных концентраций. Пересечение кривых с пунктирной линией соответствует точкам кипения под атмосферным давлением (760 мм рт. ст.). С понижением температуры кипящей кислоты ее концентрация, начиная от 20,24%, может и возрастать и убывать. Это же видно из рис. 124. При общем давлении 700 мм рт. ст. азеотропная смесь кипит при 105,8° и содержит 20,4% НС1. При более низкой концентрации кислоты ее пары обогащены водяным паром, а при более высокой — хлористым водородом. Охлаждение кислоты азеотропного состава вследствие ее испарения при абсорбции, т. е. переход от изотермы /аз, например, к Ti, Может привести к образованию как более разбавленной (точка Л), так и более концентрированной (точка В) кислоты. Возрастание или убывание концентрации кислоты будет зависеть от состава газовой фазы. Если парциальное давление НС1 в газе превышает давление НС1 над постоянно кипящей смесью, то концентрация кислоты должна возрастать. Поэтому при подаче хлористого водорода кипящая в адиабатических условиях кислота будет концентрироваться.
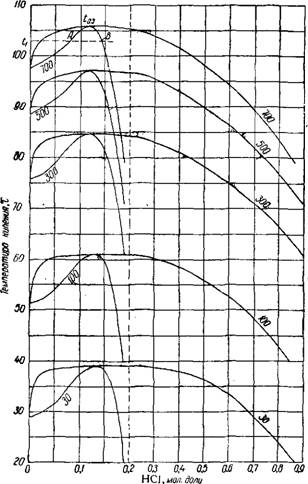
По мере укрепления соляной кислоты содержание HCI в уходящих из абсорбера парах также будет повышаться. На рис. 125 показано, например, изменение давления паров Н20 и НС1 над соляной кислотой, получаемой по мере насыщения воды с начальной температурой 30° при общем давлении 700 мм рт. ст. 100%-ным хлористым водородом без охлаждения абсорбера. Пока концентрация кислоты невелика, в паровую фазу переходит, главным
образом, вода, и раствор концентрируется как вследствие продолжающегося поглощения хлористого водорода, так и вследствие
|
Рис. 124. Кривые состав — температура кипения системы HCl—Н20 прн различных давлениях. Цифры на изобарах: Р — Pjjqj + Pfj2o в мм Р'1- ст - (масштаб абсцисс вправо от пунктирной линяй в 2 раза меньше). |
|
'10 15 ZD 25 30 3 Концентрация соляной кислоты, Ввс.% |
|
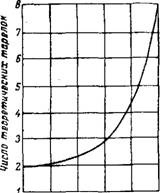
Рис. 126. Число теоретических тарелок, обаспечивэю - щее получение соляной кислоты заданной концентрации. |
|
Ь 1 |
|
ООО е 500 I л S 400 5 I |
|
300 |
|
0,050.072 0./0 0,15 0.20 Концентрация НС1 в жидкости, моли |
|
025 |
|
Рис. 125. Изменение давления паров НС1 (кривая 1) и Н20 (кривая 2) в процессе насыщения воды хлористым водородом (начальная температура воды 30°, давление 700 мм рт. ст.). |
|
* Наиболее рационально процесс горячей абсорбции может быть осуществлен в тарельчатой или насадочной абсорбционной колонне. Для получения стандартной соляной кислоты, содержащей 27,5% НС1, требуются всего 4 теоретические тарелки (рис. 126), а 31% НС1 — 5. На практике применяются не тарельчатые, а на - садочные колонны, более простые и удобные в эксплуатации. Понижение температуры, подаваемой на верх абсорбера воды, немного уменьшает количество уходящего из него водяного пара, а следовательно, и потери уносимого им хлористого водорода. Не должна быть слишком высокой и температура поступающего на абсорбцию газа. Увеличение содержания в газе инертных компонентов также влияет на абсорбцию благоприятно (несмотря на понижение концентрации НС1 в газе), так как понижает температуру в абсорбере. Но высота абсорбера должна быть при этом больше, так как увеличивается высота слоя насадки, эквивалент- |
Удаления воды. При достижении концентрации кислоты 14% НС1 (молярная концентрация НС1 в жидкости х = 0,072) и температуры 102,6° раствор закипит. Дальнейшее насыщений раствора хлористым водородом будет идти при постоянном давлении паров над кислотой, равном 700 мм рт. ст., но по мере возрастания концентрации кислоты парциальное давление водяного пара над ней будет уменьшаться, а парциальное давление хлористого водорода—увеличиваться. Поэтому при получении концентрированной кислоты в одноступенчатом абсорбере большая часть хлористого водорода останется неабсорбированной.
Ная одной теоретической тарелке. Если поступающий на абсорбцию хлористый водород содержит водяные пары, то максимальная концентрация получаемой соляной кислоты одинакова с концентрацией кислоты, конденсирующейся при охлаждении газа до точки росы. Если хлористый водород разбавлен инертным газом (воздухом), то максимальная концентрация соляной кислоты будет соответствовать концентрации кислоты, находящейся в равновесии с поступающим на абсорбцию газом. Эту концентрацию можно определить по рис. 112 или вычислить по формуле112 с == (0,304/ — 0,0016) р0'15, где с — концентрация кислоты, г НС1 на 1 г Н20; t-—температура кислоты, °С; р — парциальное давление НС1, мм рт. ст. Так, при содержании в поступающем на абсорбцию газе 30% НС1 (парциальное давление НС1 — 228 мм Рт. ст.) максимальная концентрация соляной кислоты при 80° будет 28,5%, при 60° —31,8%, для 50%-ного газа — соответственно 30,5 и 33,3%.
Производственные колонны для абсорбции хлористого водорода без охлаждения изготовляют из фаолита и заполняют насадкой из керамических колец (25X25 мм). Широко применяют также абсорбционные колонны из графитовых блоков, пропитанных термореактивными смолами с последующей термообработкой). При диаметре колонны 0,45 ж и высоте 6,4 м в ней можно получить из синтетического хлористого водорода до 30 г в сутки 31%-ной соляной кислоты. Температура поступающего в колонну газа не должна превышать 250°, а концентрация НС1 в нем должна быть не меньше 80%. Воду подают в колонну через фэолитовый ороситель. Вытекающая из колонны соляная кислота должна иметь температуру не выше 60° и плотность 1,155—1,160 г/см3 при 20°. Она поступает в оросительный холодильник из графолитовых трубок (диаметром 78/102 мм, длиной 3,6 м) и течет по трубкам, орошаемым снаружи холодной водой. Охлажденная до 40° соляная кислота направляется в хранилище готовой продукции, например, стальные, футерованные диабазовой плиткой резервуары. При повышении температуры выходящей из колонны кислоты уменьшают количество подаваемой воды, так как это указывает на избыток' воды. При понижении температуры ^зеличивают расход воды на орошение, во избежание получения слишком концентрированной кислоты и увеличения потерь НС1 с газом.
Уходящая из верхней части абсорбционной колонны паро-га - зовая смесь содержит незначительное количество НС1. Перед выбросом в атмосферу содержание НС1 в ней снижают до санитарной нормы, для чего ее пропускают через промывную, также фао - литовую колонну диаметром 0,6 м и высотой 4 м, с насадкой из керамических колец, орошаемую водой. Стекающая из промывной колонны кислая вода, содержащая всего — 1,5% НС1, не ис - пальзуется и является отбросом производства. Перед спуском в
Канализацию ее нейтрализуют известняком. Иногда нейтрализацию осуществляют в промывной башне, орошая ее раствором соды.
Имеется опыт40'113 горячей абсорбции газа (выходящего из сульфатных печей и содержащего 30—50% НС1) в системе из шести последовательно соединенных фаолитовых барботажных абсорберов, расположенных каскадом.