Каталитическое действие. HF
Следы фторид-ионов оказывают заметное каталитическое действие при низких значениях рН, когда присутствует главным образом HF. Айлер [87] обнаружил, что, в то время как при рН>2 реакция полимеризации катализируется гидроксил-иона - ми, о чем уже сообщалось другими исследователями, при рН<2 катализатором является фторид водорода, или, точнее сказать, скорость реакции пропорциональна концентрациям ионов водорода и фторид-ионов (см. рис. 3.14).
Значение рН, при котором наблюдается оптимальная устойчивость кремневой кислоты, зависит от того, какие примеси присутствуют в растворе. Следы ионов алюминия, и в меньшей степени— ионов железа, тория и бериллия, способны отчасти компенсировать влияние фторид-ионов за счет образования фторид - ных комплексов и, таким образом, тормозить процесс полимери-
100
50
1,0 ' 2,0 рН
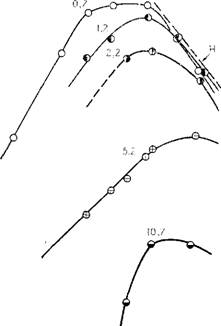
Рис. 3.14. Зависимость продолжительности гелеобразования золей кремневой кислоты от рН и концентрации (по данным Айлера [89]).
Ниже изоэлектрической точки (рН 2} скорость гелеобразования (величина, обратная времени гелеобразования} пропорциональна концентрациям ионов и F - при условии, что содержание примесей А13+ и "Fe3+ остается постоянным. Из показанных на рисунке данных следует, что HF представляет собой катализатор процесса. Пунктирная линия Н отражает действие иона ОН—. Цифрами показана концентрация NaF в ммоль.'л. Золь содержал 1,0 моль/л Si02 и 0,3 ммоль/л АЪОз. Данные взяты для технического силиката.
Зации при данном рН. В зависимости от чистоты раствора область рН, в которой наблюдается оптимальная устойчивость, составляет от 1 до 3—3,5. В растворах кремневой кислоты, свободных от примеси алюминия, заметное действие на скорость полимеризации в кислых средах может оказать F~ при его содержании до 0,0001 %.
|
|
Айлер выдвинул гипотезу, согласно которой механизм полимеризации может включать в себя временное повышение координационного числа кремния от четырех до пяти или шести в случае участия в процессе иона ОН-. Неизвестно, является ли
реакция, катализируемая фторидом водорода, реакцией третьего порядка, как и реакция, катализируемая ионами Н+ в отсутствие фторидов при рН<2, или же она имеет второй порядок и, следовательно, аналогична реакции, катализируемой ионами ОН~ при рН>2. Стрелко также признавал возможность альтернативных вариантов механизма реакции полимеризации, но в настоящее время не имеется достаточно надежных экспериментальных данных, чтобы сделать определенный выбор.
В то время как Айлер показал влияние примеси фторида на скорость гелеобразования — конечную стадию полимеризации, Тарутани [95] продемонстрировал, что скорость полимеризации мономера пропорциональна содержанию ионов F~ вплоть до 0,0019 % в 3 н. растворе НС1. Фториды не оказывали никакого действия при рН 7. Тай и Чен [96] нашли, что, когда гель кремнезема формировался при низких рН в присутствии фторид- ионов, последние удерживались на поверхности геля и совсем не появлялись в жидкости, выделяемой при синерезисе. В щелочной среде на поверхности геля никаких фторид-ионов не содержалось.
Как было измерено авторами работы [97а], удаление ионов F"~ ионами А134" можно оценить из значения константы устойчивости реакции
AIF„_i +F=AIF„
При 25°С значения рКп при п 1, 2, 3, 4 соответственно составили 6,69; 5,35; 3,68 и 2,75 (погрешность для всех значений была меньше чем ±0,04).
Согласно Щербаню [346], константа химического равнове-
О
Сия при рассмотрении реакции гидролиза SiFg в присутствии избытка Si02 имеет следующее значение:
S iFg~ + 2Н20 = S Ю2 + 6F~ + 4Н+ [Г-УЧНЧ4 =1 [SiF-]