ПОЛУЧЕНИЕ АКРИЛОВОЙ КИСЛОТЫ ИЗ ПРОПИЛЕНА ИЛИ АКРОЛЕИНА
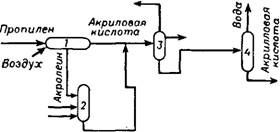
Акриловую кислоту можно получить из пропилена либо одноступенчатым прямым окислением, либо двухступенчатым окислением вначале до акролеина, который или выделяют, или окисляют в акриловую кислоту во втором реакторе (рис. 40). В табл. 15 приведены
Катализаторы для получения
Катализатор
Мо03 на Si02 Молибдат Со Молибдат Со Молибдат Со Молибдат Со
Молибдат Со
Молибдат Со с добавками Молибдат Со с добавками
Молибдат Со с добавкой Ni. . . . Молибдат Со; окись Sb—Sn (наряду с окисью Sb — Sn—>V и окисью Sn-V)
Фосфоромолибдеяовая кислота Фосфоромолибденовая кислота
Молибдат Bi......................................
Ві203; фосфоромолибдат+ Fe203
Фосфоромолибдат Bi Молибдат Bi (I ступень)
Фосфоромолибдат Bi (II ступень)
Фосфоромолибдат+ 0,1—5% As205
На Si02.....................................................
Молибдат Co + As205 .................................................
Молибдат Bi—Со.......................................
Молибдат Bi —Со
|
Состав исходных продуктов, % |
А? |
|||
|
Пропилен |
Воздух (или Ог) |
«а О и к Н Q, Os Я О |
Г» - ■ Йs Р. а Й и Я п ОЭ о Е-| в, |
|
|
— |
13,5 10 X X 3-5 |
43,2 54 X X 25-30 |
43,2 36 X X 40 |
376 351' 330-385 |
|
— |
10 |
60 |
30 |
360 |
|
— |
X |
X |
X |
— |
|
— |
X |
X |
X |
— |
|
X |
X |
X |
— |
|
|
— |
X |
X |
— |
|
|
— |
20 10,5 |
10 26,3 |
60 63,2 |
425 468 |
|
- |
9,5 |
61,8 |
28,7 |
400 |
|
26 |
— |
27 |
46 |
— |
|
1 Ч. |
X |
X 1,5 ч. (02) |
X 5,8 ч. |
490/3,8 КГС/СМ2 |
|
— |
X |
X |
X |
467/3,5 КГС/СМ2 |
|
1 ч. 10 |
10 |
1,5 ч. 50 54 |
6 ч. 40 36 |
514 450 350 |
|
X |
— |
X (02) |
X |
420—480 |
|
Таблица 15
|
|
Акриловой кислоты из пропилена |
|
Состав исходных продуктов, |
|||||
|
Катализатор |
О. Я Вв |
К S |
Воздух (или Ог) |
« О « I® М с |
& „ Се а -2 ® 3 § х Ь а |
|
Фосфоромолибдат Li и окись As. . |
14 |
— " |
71 |
15 |
400 |
|
Молибдат Sn на фарфоре............................ Окись Sn—Мо (3: 1) ................................... |
1 ч. |
— |
1 Ч. (02) |
2 ч. |
340 |
|
Молибдат Sb—Sn или окись Sb — Sn-Mo (9:3: 12)........................................ Фосфоромолибдат S'n................................. Соли V или Се кремнемолибденовой или оловомолибденовой кислоты Молибдат Sn + As205 ................................... Молибдат ТІ —Sn —Со............................... Молибдат Fe............................................... |
10 13,3 |
X 8,3 22 X |
X 41,7 56,7 50 X 33,4 |
X 50 21,3 40 ' X 53,3 |
435 425 350 406 270 |
|
Молибдат Fe, Сг, V и Ті..... Фосфоромолибдат Fe — Сг......................... Фосфоромолибдат Fe—Bi............................ |
7 я. 1 ч. |
X |
X 60 ч. 1,5—Зч. (02) 8,2 (02) |
X 23 ч. 3-10 ч. |
380 350- 450 |
|
Fe7Bi2PMoi2059 на Si02 ...... |
7,3 |
3,6 |
— |
400 |
|
|
FeCo0,3Nii2BiPMo12O5e...................................................... |
— |
1 ч. |
8 ч. |
15 ч. |
340 |
|
Молибдат Ті на Аі203 ................................. |
— |
10 |
50 |
40 |
275 |
|
Фосфоро-или боромолцбдат W+10% активатора.................................................. |
— |
— |
— |
— |
— |
|
В2,5-75іРз-57іМо2з_229в(Н2О)0_250 • ■ Борофосфомолибдат Ві на Si02 • • Борофосфоромолибдат Fe, Еі... Sn5_i2Sb5_12B30_12()P3o-i2oMoi20^; . . Боромолибдат Co........................................ |
5,3 |
10 X X 4,5 |
51 X 4,5 (02) 75,1 (N2) 42,7 |
60 X X 15,0 52 |
427 365 36-5 390 425 |
|
Борофосфаты тяжелых металлов, например окись Си, Ві, В, Р. . |
1,1 ч. |
— |
8,25 ч |
6 ч. |
440-460 |
|
Молибдат Со + теллу рид Си (0,5—1 %) Теллуромолибдаты тяжелых металлов, например окись Ті—Те —Мо |
10 10,7 |
— |
48 59,3 . |
42 30. |
438 400 |
|
Продолжение табл. 15
|
|
_ |
70 |
50-70 |
_ |
Наряду с 10—15% акролеина; улуч |
[64] |
|
Шенная селективность в резуль |
|||||
|
Тате добавкн Li20 |
|||||
|
— |
— |
— |
Исследования реакции |
[65] |
|
|
— |
— |
- |
— |
При соотношении Sn02 : Мо03=-3 : 1 |
[66] |
|
Наилучшая селективность |
|||||
|
2,5 |
85 |
63 |
53,5 |
— |
[67] |
|
12 |
60 |
60 |
36 |
Предложен фосфоромолибдат Sb |
[54] |
|
5 |
74,8 |
_ |
— |
— - |
[681 |
|
4 |
■— |
— |
18,4 |
Наряду с 11,9% акролеина |
[69] |
|
— |
- - |
— |
— |
— |
[70] |
|
— |
- - |
— |
■ 2,9 |
Наряду с 9,5% акролеина и 36,5% |
[71] |
|
Уксусной кислоты |
|||||
|
— |
— |
— |
— |
— |
[721 |
|
8 |
82,5 |
15,6 |
12,9 |
Наряду с 52,6% акролеина |
[731 |
|
— |
■— |
— |
60, |
— |
[74] |
|
— |
— |
_ |
54,3 |
53 ч. СОг, 19,9 ч. СО и 8 ч. Н2 в |
[751 |
|
Качестве разбавителя |
|||||
|
4,5 |
80 |
62,5 |
50 |
Общий состав: Fei_3Co0-7Ni3_i4 |
[76] |
|
Віі_3РМо12045 |
|||||
|
— |
29 - |
58 |
16,8 |
Предложен молибдат Ті—W И |
[77] |
|
Вольфрамат Ті |
|||||
|
— |
— |
— |
— |
Активатор: окись Fe, Mn, Cr, Bi или V |
[781 |
|
.— |
43,7 |
46 |
20 |
V |
[791 |
|
— |
46 |
56 |
, 25,8 |
— |
[80] |
|
— |
81 |
75 |
61 |
— |
[801 |
|
3,2 |
87,3 |
80,2 |
70 |
— |
[81] |
|
0,44 |
32 |
42 |
13,5 |
Кроме того, боромолибдат Ni, фос |
[82, 83] |
|
Форомолибдат Со и молибдат |
|||||
|
Со —V |
|||||
|
1 |
40-45 |
40-42 |
_ |
В качестве катионов предлагают: |
[84] |
|
Си, Ag, Fe, .Со, Sb, Bi, Mo, VV, |
|||||
|
U, Pb, Sn, Ce, Th, Nb, Та, V или |
|||||
|
Cr |
|||||
|
2,9 |
27 |
43 |
11,6 |
33% акролеина |
[851 |
|
9,3 |
75 |
18,5 |
13,6 |
69% акролеина; в качестве катио |
[86] |
|
Нов предлагают Ті, Bi, Sn, Sb, |
|||||
|
W, V, Cr, Cu, Ni, Mn |
Состав исходных продуктов,
Катализатор
|
10 |
Фосфоромолибдат Те Фосфоромолибдат Те
|
10,6 |
Фосфоромолибденовая кдолота + То02 Молибдат Со + 1% Те02
Фосфоромолибдат Ni—Те Фосфоромолибдат Мп—Те Те — Мо— Мп2Р207 . . .
Молибдат Мп + ТеОг...............................
|
1 ч. X |
Катализатор на основе МПРО4, Мо03 и Те02
Фосфат Cu + HRe04+Te02
|
X 60 |
|
X 39 |
|
X 1 |
Молибдат Со—Sn —Те (7:1:12:2) Молибдат W—Sn — Те
|
68,5 ч - X |
|
30 |
СгОз на Si02
Окись Sn — Sb -}- молибдат Со. . . Окись Sn —Sb, Sn—V, Sn —Fe. . Ванадат Sb, активированный тяжелыми металлами, например ванадат Fe —Sn—Sb...................................................................
Тяже- окись
Ванадат Sb — Sn с катионом лого металла, например Fe —Sb—Sn —V.... Окись Си —Sb —Sn —V. . Окись Sb и 5-^25% V205 . Ванадат Sb на Si02 .... Фосфорованадат Sb.... Фосфорованадиевая кислота Фосфорованадат Sn.... Фосфорованадат Си на А1203 или Si02
|
Продолжение табл. 15
|
|
Состав исходных продуктов, |
||||||
|
70 |
• go |
|||||
|
Катапиватор |
« |
Ь. А м |
||||
|
S |
4 а |
О В |
О а к Ва ° л |
АЗ А> д - В К ®8 |
I |
|
|
G п |
< ё |
И и |
Е-< a |
|||
|
Фосфорованадат Мп.............................. . |
X |
X |
X |
|||
|
Арсенованадат Си; окись Си —As— |
||||||
|
-V (1:3:2) ............................................... |
10 |
— |
49 |
41 |
386 '. |
|
|
Фосфороарсенованадат Си; окись |
||||||
|
Си—As—Р—V(1: 2 : 2 : 2) . . . . |
10 |
— |
49 |
41 |
450 |
|
|
Молибдат 'V; окись V—Мо (1:1) |
— |
X |
X |
X |
— |
|
|
Молибдаг VO и добавки............................. |
— |
22 |
56,7 |
21,3 |
350 |
|
|
V205, ванадат Ag или Ag20 . » . . |
_ |
_ „ |
— |
____ |
____ |
|
|
Фосфоровольфрамовая кислота. . |
— |
10,4 |
54,2 |
35,4 |
371 |
|
|
Фосфо^омолибдено вольфрамовая ки |
||||||
|
Слота...................................................... |
6,3 |
9,1 |
84,6 |
420 |
Данные о катализаторах для одно - и двухступенчатого процесса получения акриловой кислоты. Из всех окисей металлов наилучшим катализатором для окисления акролеина является Мо03 [115].
|
Газ
Воздух НгО Рис. 40. Схема прямого окисления пропилена в акриловую кислоту: 1,2 — реактор; з — холодильник; 4 — блок очистки. |
Описаны также методы окисления пропилена или акролеина в акриловую кислоту в паровой или жидкой фазе.
Окисление акролеина в жидкой фазе можно проводить в щелочном растворе с использованием СиО или Си(ОН)2 [116], Ag20 [117] или катализаторов CuO—Ag20 [118]; максимальный выход 98%. Окисление протекает уже при комнатной или несколько повышенной
|
Продолжение табл. 15
|
Температуре [119], но может идти и при 4 °С на катализаторах Ag [120].
Окисление акролеина в жидкой фазе происходит в присутствии нафтената Со и хелатов Со [121, 122], ацетата Мп или Ni в уксусной кислоте при 200 °С и давлении 20 кгс/см2 в присутствии НВг [123]. Уже при 20—34 °С акролеин окисляется ванадиевой кислотой в уксусной кислоте [124].
Эффективными промоторами окисления акролеина кислородом являются триалкил - или триарилфосфаты. В присутствии стеарата Ni и трибутилфосфата акролеин окисляется в акриловую кислоту в бензоле при 65 °С и 6 кгс/см2 с конверсией 28% и селективностью 87,5% [125]. Промоторами при окислении акролеина кислородом в жидкой фазе, могут быть и ароматические нитросоединения, например, возможно окисление - при 50 °С и 5 кгс/см2 в гексане в присутствии нитробензола [126, 127]. При 75 °С смесь пропан — пропилен окисляется с образованием окиси пропилена или акриловой кислоты [128]. Предложен целый ряд катализаторов для окисления акролеина в бензоле: молибдат Си (при 50 °С и давлении кислорода 10 кгс/см2 получают 67% акриловой кислоты); молибдат Ті (62%), молибдат Со (64%), смесь молйбдатов [129], иод [130]. Возможно окисление под давлением и без добавки катализатора (при 25—30 ""С и давлении кислорода 5 кгс/см2 конверсия 32%) [131].
Перекись водорода окисляет акролеин в акриловую кислоту в присутствии вольфрамовой кислоты [132], гетерополикислоты на основе вольфрама (например, селено-вольфрамовой кислоты) [133] или Se02 [134]. Вместо перекиси водорода можно использовать и органические гидроперекиси в присутствии Se02 [135] или Сг03 [136]. Можно проводить комбинированное окисление пропилена, например, окислить его в акролеин на катализаторе фосфорована - домолибдате, а затем перевести перекисью водорода в акриловую кислоту в присутствии Se02 [137].
Катализатором при окислении пропилена кислородом в газовой фазе может сйужить НВг; при 224 °С получают наряду с аллилбро - мидом смесь кислот, в той числе и акриловую кислоту [138].
Существует метод одновременного получения акрилонитрила, акролеина и акриловой кислоты [139]. Реакционная смесь из окиси азота и водяного пара, получаемая при 800—900 °С из смеси NH3—Н20—02 на сите Pt—Rh, взаимодействует с пропиленом при 400—420 °С. Наконец, пропилен можно окислять смесью Se—NH3 с одновременным образованием акрилонитрила [140].