Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ЖИДКИЕ УДОБРЕНИЯ
ОБЩИЕ СВЕДЕНИЯ
Жидкие удобрения (ЖУ)1-9 могут быть простыми и комплексными. Простые жидкие удобрения представляют собой растворы аммиачной селитры, карбамида, кальциевой селитры и их смесей в жидком аммиаке или в концентрированной аммиачной воде — так называемые аммиакаты 10' В качестве жидких удобрений особенно широко применяют также жидкий аммиак и аммиачную воду (20—22% NH3) 12' 13.
Жидкие комплексные удобрения (ЖКУ) приготавливаются обычно на основе экстракционной или термической фосфорной кислоты. В последнее время для этой цели стали использовать суперфосфорную и полифосфорные кислоты, что дает возможность получать более концентрированные жидкие удобрения. Производят также суспендированные жидкие удобрения 14~18.
Еще в 1932—1935 гг. было показано, что аммиак и аммиакаты так же усваиваются растениями и дают такой же эффект, как и Обычные, твердые азотные удобрения19-20. Производство же их проще и дешевле, чем производство твердых удобрений. При растворении в аммиаке нитрата аммония и нитрата кальция или их смесей давление паров аммиака значительно снижается, и при определенной концентрации солей для обычной температуры оно равно атмосферному 21~23.
Аммиакаты на основе нитрата аммония и карбамида применяют и для аммонизации суперфосфата и тукосмесей 24-25.
Особенно широкое распространение жидкие удобрения получили в США: в 1966 г. было произведено 1248 тыс. г жидких комплексных удобрений (в натуре)9'26-29, в 1969 г. общее производство жидких удобрений около 4 млн. т 30. Жидкие азотные и комплексные удобрения применяются в большинстве стран Европы31, а также в СССР32.
Применение жидких удобрений обеспечивает - возможность полной механизации работ по погрузке, выгрузке и внесению удобрений. Трудовые затраты их по внесению при условии допосевного внесения фосфорных и калийных удобрений, сокращаются в 2— 3 раза по сравнению с затратами на внесение твердых удобрений. Достигается более равномерное распределение удобрений в поч -
Gg 33—36
Некоторые виды жидких удобрений могут применяться для подкормки растений с самолетов и автомобилей.
Непосредственное использование аммиака 37>38 и аммиачной воды в качестве жидких азотных удобрений обеспечивает возможность ускоренного строительства азотных заводов по «короткой» схеме, без цехов переработки 'аммиака в азотную кислоту и аммиачную селитру. При этом сокращается объем строительных работ по энергетическому, транспортному и складскому хозяйству, вспомогательным службам и жилью.
Значительно сокращаются также эксплуатационные затраты и, следовательно, удешевляются удобрения, так как себестоимость единицы азота в аммиаке приблизительно на 35% ниже, чем в самом дешевом твердом азотном удобрении — аммиачной селитре. Отпадает необходимость в бумажных мешках (или другой таре), расход которых на упаковку продукции одного завода составляет много миллионов штук. Кроме того, жидкие удобрения не обладают такими отрицательными свойствами твердых удобрений, как слеживаемость, сегрегация и т. п. 39~41.
Наряду с преимуществами, в производстве и применении жид - ких удобрений имеются известные трудности и недостатки. Стоимость Р205 в крепкой фосфорной кислоте, требующейся для производства концентрированных ЖКУ, выше, чем в более слабой кислоте, пригодной для получения твердых удобрений.
В жидких удобрениях водных — растворах солей — в случае большой их концентрации происходит высаливание, кристаллизация солей при понижении температуры42. Применение же менее концентрированных растворов приводит к необходимости перевозить большие количества растворителя — воды. Поэтому стремят-, ся найти такие композиции жидких удобрений, которые имели бы высокие концентрации и низкие температуры кристаллизации (замерзания). Для хранения жидких удобрений требуется сооружение резервуаров большой емкости, так как они используются лишь в течение относительно короткого времени.
Жидкий аммиак экономичнее хранить при низком давлении и искусственном охлаждении; для этой цели применяют сферические емкости вместимостью 2—14 тыс. т 43. Применение жидких удобрений требует капиталовложений на организацию распределительных г пунктов вблизи районов потребления, создания специального оборудования для внесения удобрений в почву44, а также парка ци - ;
Стерн (железнодорожных и автомобильных) для их перевоз - кИ 45-47- применение безводного аммиака в качестве удобрения требует специального оборудования, рассчитанного на повышенное давление. Возможна транспортировка жидких удобрений по трубопроводам 48-49, а жидкого аммиака в контейнерах50'51.
Существенным недостатком некоторых жидких удобрений является их корродирующее действие4. В особенности это относится к растворам аммиакатов нитрата аммония, обладающим повышенными коррозионными свойствами по отношению к черным металлам. Это затрудняет производство, хранение, транспортировку и внесение удобрений в почву, так как связано с применением дорогостоящих материалов (нержавеющей стали, алюминия и др.).
Аммиакаты, аммиачную воду и особенно безводный аммиак во избежание потерь азота требуется вносить в почву на глубину не менее 12—15 см. Поверхностное внесение жидких удобрений типа аммиакатов недопустимо, так как при этом будут большие потери аммиака. Кроме того, возможны ожоги листьев и стеблей растений при попадании на них аммиака и аммиакатов 52-53. Поэтому для внесения в почву жидких удобрений применяют машины.
Оценка технико-экономических факторов, характеризующих производство и применение твердых и жидких удобрений, показывает, что в итоге преимущества остаются за жидкими удобрениями 54-59.
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Жидкий аммиак содержит.82,3% N и является самым концентрированным азотным удобрением. Под атмосферным давлением аммиак кипит при —33,35° и замерзает при —77,7°. Абсолютное давление пара над жидким аммиаком:
Температура, °С........................... —30 —10 0 10 20 40 50
Давление, ат ......................................... 1,18 2,87 4,24 6,08 8,46 15,34 276
Жидкий аммиак хранят и транспортируют в стальных цистернах, рассчитанных на давление 20—30 ат. Плотность газообразного аммиака при нормальных условиях 0,77 кг/мъ. Согласно ГОСТ 6221—70, жидкий аммиак высшего, 1- и 2-го сортов должен содержать, соответственно, не менее 99,95, 99,9, 99,6% NH3 и не более 0,05, 0,1, 0,4% влаги и 2,0, 8,0, 20,0 мг/л масла; железа в высшем и 1-м сортах должно быть не более 2,0 мг/л. По ГОСТ 5.1185—72 в аттестованном продукте должно быть не менее 99,96%' NH3 и не более 0,04% влаги, 2 мг/л масла и 1,0 мг/л железа.
Аммиак очень хорошо растворяется в воде: 1 объем воды при
И при парциальном давлении NH3, равном атмосферному, растворяет 1176 объем ов аммиака ("приведенных к нормальным условиям), а при 20° —702 объема. Пол. атмосферным давлением'максимальная концентрация NH3 в воде при 0° равна 46,7%, при 50°—
18,6%. Зависимость между растворимостью аммиака в воде, давлением его над раствором и температурой показана на рис. 412.
|
Nh, no3 |
|
NH3 Ю |
|
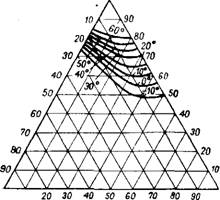
Рис. 413. Диаграмма растворимости в системе NH4NO3—NH3—Н20. |
|
Ся содержание не более 8 г/л С02 и 0,01 ejл меди. |
|
So |
|
X Z § 40 S А I ?0 З I § |
|
Нго |
Аммиачную воду (аммиак водный технический, ГОСТ 9—67) производят двух марок: А — для удобрения сельскохозяйственных культур и Б — для промышленности. Каждая марка имеет 1 и 2 сорт. Для 1 сорта установлено содержание не менее 25%, для 2 сорта — 22% NH3. Содержание нелетучего остатка установлено только для марки Б (не более 0,2% в 1 сорте и 0,4% во 2 сорте). В продукте марки А допускает
|
.0" .10° 20° |
—' |
||||||
|
Ж 40° £0° 80° 100° |
,—'» |
||||||
|
Га |
|
0,5 1,0 1,5 Давление NH3, am |
Рис. 412. Изотермы растворимости аммиака в воде.
Вследствие относительно небольшого давления пара над аммиачной водой ее хранят и транспортируют в стальных цистернах или закрытых резервуарах, рассчитанных на давление 1,5—2 ат.
Твердые аммиакаты представляют собой комплексные кристаллические соединения, образующиеся при взаимодействии некоторых твердых солей (или их водных растворов) с жидким или газообразным аммиаком. Состав аммиакатов, полученных на основе аммиачной селитры, соответствует формуле NH4N03-rtNH3-mH20; аммиакаты на основе кальциевой и аммиачной селитры имеют следующий состав: Са^ОзЬ-яМ^МОз-яМНз-ягНгО. Твердый нитрат аммония при температуре от —15 до +25° энергично поглощает газообразный аммиак и переходит в жидкое состояние — образуется так называемая жидкость Дайверса. При —10° ее состав отвечает формуле NH4N03-2NH3. С повышением температуры происходит выделение аммиака и при 28° образуется твердая соль NH4N03-NH3, которая легко теряет аммиак. Жидкие аммиакаты—, светлые жидкости (допускается желтоватая окраска), плотность* их зависит от состава и колеблется в пределах 0,9—1,25 г/См3. Да
вление пара над аммиакатами значительно ниже, чем над жидким аммиаком.
|
На рис. 413 и 41460'62. Растворимость Со (nhjJJ |
|
NH |
|
Нго |
|
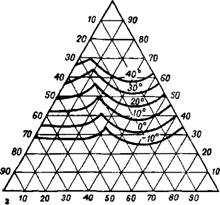
Рис. 414. Диаграмма растворимости в системе CO(NH2)2-NH3— Н2О. |
Растворимость некоторых азотнокислых солей в воде, в аммиачной воде и в жидком аммиаке приведена в табл. 105.
|
Таблица 105 Растворимость азотнокислых солей в разных растворителях
|
|
Растворимости аммиачной селитрычи карбамида в аммиаке и |
Аммиачнои воде показаны в системе CO(NH2)2— —NH4NO3—NH3—Н20 при 0 и 30° представлена на рис. 415бз. В этой си - NH3
Стеме при
= 0,4
NH3 + н? о в твердой фазе образуется комплекс CO(NH2)2- •0,11NH3, а при отноше -
NH3 г г* НИИ NH3 4- Н20 =°'5 К0М" Плекс имеет состав СО (NH2) 2 • 0,25NH3.
Температура высаливания аммиакатов понижается с увеличением содержания в них аммиака и уменьшением содержания воды. Аммиакат состава 55,14% NH4NO3, 25,69% NH3 и 18,97% Н20 имеет температуру высаливания —27,5°. Введение в аммиакат CO(NH2)2 или Ca(NOs)2 также приводит к понижению темпера - Туры высаливания 64~67.
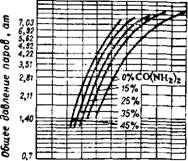
На рис. 416 и 417 показано изменение плотности аммиакатов в зависимости.,, от концентрации соли и аммиака, а на рис. 418 и
419 — зависимость общего давления пара над аммиакатами от содержания соли, аммиака и воды в растворе.
Производство аммиакатов, содержащих помимо карбамида карбонат аммония, позволяет с наибольшей простотой утилизировать отходящие газы цеха карбамида. О равновесиях в системе (ЫН4)2СОз—CO(NHo)2—
|
20 30 40 50 ео 70 NH4NO3, % |
|
Рис. 415. Растворимость в системе CO(NH2)2— NH4NO3—NH3— Н20 при 0 и 30°. Nh3 Числа на кривых — отношения------------------------ |
|
. 30% |
|||||||||
|
/ |
Л* / 10% |
||||||||
|
V |
/ |
/0% |
|||||||
|
7 |
|||||||||
|
|
|||||||||
|
|
|
•о Е О Б О £ |
|
U U2 М 1,0 0,9 0,8 V «6 |
|
О 10 20 30 40 50 60 70 80 30 100 NHj, вес. °/о |
|
Рис. 417. Плотность в системе CO(NH2)2—NH3—Н20 при 15°. |
|
* |
|||||||||
|
S* |
|||||||||
|
Ч> |
|||||||||
|
4 |
|||||||||
|
£ |
|||||||||
|
4г |
|||||||||
|
О. |
|||||||||
|
1,3 '.2 1.1 1,0 0.5 0.8 0,7 0,6 |
|
0 10 20 30 40 50 60 70 80 30 100 |
|
Nh3 ,бес.% I |
|
Рис. 416. Плотность в системе NH4N03—NH3—Н20 при 15°. |
|
Данные о некоторых свойствах аммиакатов, применяемых в США, приведены в табл. 106. В табл. 107 и 108 приведены составь! |
—NH4NO3—Н20 см.68. При добавлении к таким аммиакатам микроэлементов (соединений В, Со, Nh3+H2O ' Mo, Zn, Си) в количестве до 4% давление паров NH3 + CO2 над растворами понижается, а температуры кристаллизации повышаются е9.
Аммиакатов, имеющих достаточно низкую температуру выделения твердой фазы. Жидкие комплексные удобрения производятся двумя способами: 1) нейтрализацией фосфорной кислоты аммиаком С последующим смешением полученного раствора с КС1 или К2СО3,
|
—1—|—j—^—1— |
|||||
|
1/ Jsjr L |
|||||
|
A//V1 |
|||||
|
1 1 /Y// 1 1 1 ■"" |
|||||
|
JU/f- 15% |
|||||
|
ШМ1№4° |
|||||
|
Fffff~j[~-eox |
|||||
|
Ж '4^70% |
|||||
|
О 10 20 30 40 50 ео 70 SO 30 100 NH3, вес. % Рис. 418. Общее давление пара иад системой NH4NO3—NH3—Н20 при 20°. |
Или другими солями, вводимыми для получения заданного соотношения питательных веществ (горячий способ); 2) смешением предварительно полученных растворов фосфатов или полифосфатов аммония с другими солями — твердыми или растворенными (холодный способ).
|
0 10 20 30 40 50 Ео 70 Во So too NH3, Бес.7° Рис. 419. Общее давление пара над системой CO(NH2)2—NH3—Н20 при 20°. |
ТАБЛИЦА 106
|
Жидкие азотные удобрения, применяемые в США
|
|
ТАБЛИЦА 107 Составы аммиакатов иа основе нитрата аммония и карбамида
|
Большое значение имеет взаимная растворимость компонентов при различных условиях, так как одним из основных требований, предъявляемых к жидким комплексным удобрениям, является — низкая температура кристаллизации солей во избежание затруднений при их использовании70-71.
В системе NH4H2P04—NH4N03— KCI—Н20 72 в диапазоне весовых отношений NH4H2P04 : NH4N03 от 0,5 до 2,66 и общей концентрации солей в насыщенном растворе 25, 28, 30, 32 и 34% увеличение содержания КС1 в смеси солей до 25—35% приводит к понижению температуры начала кристаллизации от 25—35 до 2—10°. Дальнейшее увеличение содержания КС1 в смеси приводит к повышению этой температуры. Стабильный насыщенный раствор, в котором отношение KCI : NH4H2P04: NH4N03 = 35 : 32,5 : 32,5, при 24,5° имеет общую концентрацию солей 34%- Наиболее низкая температура начала кристаллизации, равная 1,5°, наблюдается при отношении KCI : NH4H2P04: NH4N03=46,5 : 26,75 : 26,75 и общей концентрации их в насыщенном растворе 28%. С повышением температуры содержание питательных веществ в растворе увеличивается, а с уменьшением отношения N : Р2О5, т. е. при увеличении в смеси доли Р2О5, не изменяется. Так, например, содержание питательных веществ в растворе при отношении N : P2Os: К20 = 1 : 1 : 1 составляет около 17% при 15° и 19% при 25°, а для отношения N : Р2О5: КгО = 1 : 2 : 1 при 15°—16,5%, при 25°-18,9%.
В системе NH4H2P04—NH4NO3-CO (NH2)2—Н20 72'73 в интервале температур от —7 до 50° и весовых отношений NH4H2P04: : NH4NO3 от 0,5 до 4 при общей концентрации солей в насыщенном растворе 30, 35, 37 и 40% повышение содержания карбамида в Смеси сухих солей от 5 до 65% приводит к увеличению концентрации насыщенного раствора. В указанном диапазоне концентраций и температур наиболее низкая температура выделения твердой фазы (от 0 до —7°) наблюдается при общем содержании в системе 30—35% солей и 50% карбамида в сухой массе солей. Понижение температуры кристаллизации растворов от 30 до 10° при повышении содержания в них солей может быть достигнуто либо при одном и том же отношении NH4H2P04: NH4NO3 за счет увеличения содержания карбамида в общей массе солей, либо при одном и том же содержании карбамида за счет изменения отношения NH4H2P04 : : NH4N03 от 1 до 4 и более.
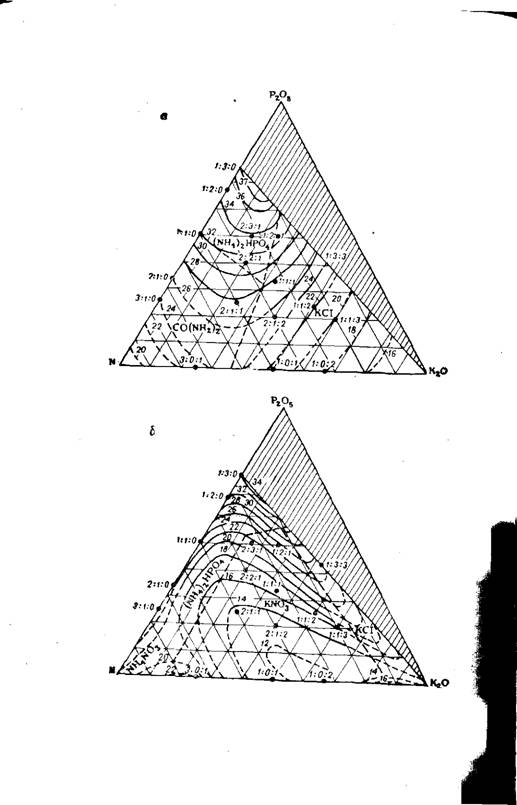
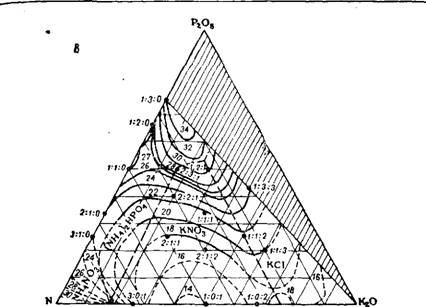
О совместной растворимости компонентов жидких комплексных удобрений, приготовленных на основе термической фосфорной кислоты см. 74~77. На рис. 420 представлены изотермы многокомпонентных систем, позволяющих определить возможную концентрацию питательных веществ в растворе в зависимости от заданного соотношения N : Р2О5: К20, а также какой солью насыщен раствор и какая твердая фаза будет из него выделяться при охлаждении ниже 0°. Например, при соотношении N ; Р205 ; КгО = 1 : 1 : 1, можно приготовить жидкое комплексное удобрение из карбамида, фосфорной кислоты, аммиака, хлористого калия и воды с общим содержанием питательных веществ 28% (рис. 420, а); при замене карбамида нитратом аммония — 17% (рис. 420,6); при одновременном применении карбамида и нитрата аммония — 22% (рис. 420, в).
На рис. 421 представлена зависимость температуры кристаллизации жидких комплексных удобрений от концентрации питательных веществ 74.
На основе полифосфорных кислот 78-81 при их аммонизации газообразным аммиаком с добавлением воды или аммиачной водой получаются жидкие комплексные удобрения с соотношением, N : Р205 = 1:3. Содержание питательных веществ в них при концентрации исходной полифосфорной кислоты 74—83% Р2Об составляет 42—48%, что на много превышает концентрацию питательных веществ в жидких комплексных удобрениях, полученных на основе термической или экстракционной фосфорной кислоты. Соотношение питательных веществ в удобрении может быть вырав - йено растворением в них карбамида или добавлением смеси растворов карбамида и нитрата аммония.
|
|
|
Рис. 420. Изотермы многокомпонентных систем при 0° (заштрихована область кислых растворов): А —система карбамид— аммиак — фосфорная кислота —хлориетый калий - вода (NH3 : Р04 = 1,6); б —система нитрат аммония — аммиак — фосфорная кислота — хлористый калий —вода; в —система карбамид — нитрат аммония — фосфорная кислота — хлористый калий —вода. |
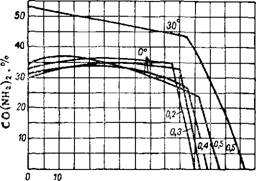
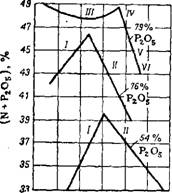
На диаграмме (рис. 422) показана растворимость фосфатов и полифосфатов аммония 80-Р2, полученных на основе ортофосфорной кислоты (54% Р2О5) и полифосфорных кислот (76 и 79% Р2О5). С повышением концентрации исходной фосфорной кислоты увеличивается концентрация питательных веществ в жидких удобрениях, соответствующая определенной степени аммонизации кислот.
ТАБЛИЦА 109
Составы двойных жидких комплексных удобрений
Марки
Соотношение питательных веществ из ортофосфорной кислоты (52-54»/. Р205) из полнфосфорной кислоты (78—79% Р2О5)
|
4:1:0 3: 1: 0 2:1:0 1:1:0 1:2:0 1:3:0 |
|
24- 6-0 24- 8-0 22-11-0 19-19-0 15-30-0 12-36-0 |
|
16- 4-0 18- 6-0 16- 8-0 13-13-0 9-18-0 8-24-0 |
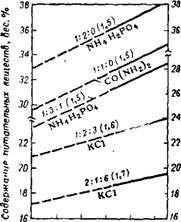
В табл. 109 приведены составы двойных жидких комплексных удобрений, которые могут быть получены на основе ортофосфорной и полифосфорной кислот 80-83. В табл. 110 приведены составы тройных жидких комплексных удобрений с соотношением N : Р205; : К20 = 1 : 1 : 1 и 1 : 2 : 1, с температурой на'сыщения около 0°, которые могут быть получены на основе жидких комплексных удобре-
|
|
|
-12-8-4 0 4 Температура, °С |
|
В 10 |
|
Рис. 421. Зависимость температуры кристаллизации жидких комплексных удобрений от концентрации питательных веществ в системе карбамид — фосфаты аммония — фосфорная кислота — хлористый калий — вода (в скобках — молярные отношения NH3:H3P04 в кристаллизующихся солях). |
Вий состава 11—33—0 и 8—24—0, приготовленных путем аммони зации ортофосфорной кислоты74.
При аммонизации экстракционной фосфорной кислоты выде ляются осадки фосфатов железа и алюминия. При добавлении раствору КС1 последний взаимодействует с содержащейся в экс тракционной кислоте кремнефтористоводородной кислотой с обра зованием кремнефторида калия, который тоже выпадает в осадок
H2SiFe + 2КС1 + 2NH3 = K2SiF6 + 2NH4C1
|
0,28 0,29 0,30 0,31 0,32 0,33 0,34 N : Ра05 |
|
Рис. 422. Влияние концентрации Р205 и весового отношения N : Р205 на растворимость солей в аммонизированных растворах фосфорных кислот при 0°. Твердые фазы: I — NH4H2PO4; //-(nh4)2hp04; 111 - FNH4)3HP2O7-H20; /k-(nh4)5p3oi0 • н20; v-(nh4)2hp04 • 2нго; l-7-(nh4)4p207 • h20. |
Разработан оптимальный режим аммонизации фосфорной кис лоты и фильтрации осадка74. Однако при использовании экстрак
|
ТАБЛИЦА и» Составы тройных жидких комплексных удобрений
|
|
* Температура насыщения 6—7°. |
Ционной фосфорной кислоты, можно получить жидкие комплексные удобрения лишь с низкой концентрацией питательных веществ, около 24%, а для отделения осадка требуется фильтровальное оборудование, что снижает экономичность процесса83-88.