Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ХЛОРИД КАЛЬЦИЯ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Хлорид кальция СаС12 образует белые кристаллы кубической формы с плотностью 2,51 г/см3. Плавится при 772°. Сильно гигроскопичен, на воздухе расплывается. Равновесная относительная влажность воздуха над СаС12'2Н20 при 20° равна 22%, при 50°— 17%, а над СаС12-6Н20 при 10° —38%, при 20° — 32,3%, при 24,5° — 31%- Высушивание гранулированным хлоридом кальция при 25° позволяет понизить влажность газа до 0,14—0,25 г воды в 1 м3. Практическая влагоемкость хлорида кальция при 25° (поверхностная) :
Относительная влажность Газа, % .... 36 60 70 80 85 90 95 Влагоемкость, кг/кг 1,0 1,6 2,0 2,8 3,5 5,0 8,4
Сведения о растворимости и кристаллогидратах СаС12 даны в табл. 49 и на рис. 202. О вязкости водных растворов CaCfo см.
Температуры кипения растворов СаС12:
СаС12, %.......................................... 40,8 50 58 75
<к„п, °С............................................ 120 130 140 175
С аммиаком СаС12 образует двойные соединения СаС12-4ЫНз, CaCi2-8NH3.
При повышенных температурах СаС12 разлагается кислородом воздуха и парами воды по реакциям
CaCl2 + 0,502 ^Zt СаО + С12 СаС12 + Н20 СаО + 2НС1
А в присутствии Si02 или А120з идут реакции:
2СЕС12 + Si02 + 02 2СаО • Si02 + 2С12 ЗСаС12 + А!203+ 1,502 ЗСаО-А1203 + ЗС12
Заметное разложение СаС12 в сухом и влажном воздухе идет выше 830°, в присутствии БЮг —выше 720°, в присутствии А120з — выше 800°2.3.
|
ТАБЛИЦА 49 |
Растворимость СаС12 в воде
|
Концентрация СаС12 В растворе, % |
|
Температура, °С |
|
Твердые фазы |
6Н20
Лед + СаС12 ■ СаС12 • 6Н20 То же
СаС12 • 6H20+Ct-CaCl2 ■ 4Н20 СаС12 • 6Н20 + р-СаС12 • 4Н20 СаС12 • 6Н20 + V-CaCl2 • 4Н20 а-СаС12 • 4Н20
А-САС12 • 4Н20 + СаС12 • 2Н20 СаС12 • 2Н20
|
СаС12 • СаС12 • СаС!2 |
То же » »
СаС]2 • 2Н20 + СаСЬ • Н20
Н20
|
(мет), (мет.) |
Н20 + СаС12
Известен субхлорид кальция СаС12/устойчивый при температуре выше 800°, образующийся при нагревании СаСЬ с металлическим
|
J00 |
|
250 |
|
200 |
|
50 |
|
ВО 80 |
|
Го 4о СаС12, вес. % |
|
|
|
Рис. |
|
Го зо 40 CaClj, вес. % Растворимость в системе ICl2—Са(ОН)2—Н20. |
Кальцием. Субхлорид кальция окрашен в красно-фиолетовый цвет. Он может быть получен при комнатной температуре в Метастабильном состоянии при быстром, переохлаждении.
%J50 |
|
-50 |
|
Рис. 202. Растворимость енстеме СаС12—Н20. |
|
203. С |
£ 100
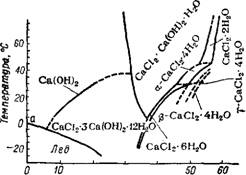
В системе СаС12—Са(ОН)2—Н20 (рис. 203) в интервале б—Уб" кристаллизуются 8 твердых фаз: Са(ОН)2, СаС12 • Са(ОН)2 • Н20,
СаС12-ЗСа(ОН)2-12Н20, СаС12-2Н20, а-, р - и уСаС12-4Н20 и СаС12-6Н20?. Гидрооксихлорид кальция СаС12 • ЗСа(ОН)2 • 12Н20" кристаллизуется в виде прозрачных игольчатых кристаллов ромбической сингонии. В воде и при температуре выше 50° разлагается с образованием раствора СаС!2 и Са(ОН)2.
В солянокислых растворах растворимость СаС]2 уменьшается и тем в большей степени, чем ниже температура. При 0° в растворе с содержанием 27,98% НС1 растворяется 9,1% СаС12 (вместо 37,30% в воде), при 15° и содержании в растворе 26,20% НС] растворяется 21,3% СаС12 (вместо 41,2% в воде). В системе НС!— СаС]2—Н20 при 15° кристаллизуются две твердые фазы: СаС]2-
2Н20 и СаС]2 ■ 6Н20, при 25° —три твердые фазы: СаС12-2Н20, СаС12-4Н20, СаС]2-бИгО. Хлорид кальция высаливает NaCl из его водных растворов, особенно при пониженных температурах. Растворимость NaCl в системе СаС12—NaC!—Н20 (при 0°) непрерывно уменьшается по мере растворения СаС12 (от 26,23% в воде до 0,62% в растворе, содержащем 34,87% СаС12). При более высоких температурах, помимо NaC!, кристаллизуются также СаС12-
6Н20 или СаС]2 • 2Н20; при —5, —23° кристаллизуются твердые фазы: лед, NaCl • 2Н20, NaC! и СаС12 • 6Н20.
В системе СаС12—NaCl—Н20 из метастабильных растворов при концентрации NaCl до 0,5 мол. % могут выделяться а-, р - и у-моди - фикации СаС12-4Н20. В системе СаС12—НС1—Н20 существуют, наряду со стабильными, также метастабильные области выделения всех трех модификаций тетрагидрата СаС]2 и СаС12-2Н20. Метастабильные растворы характеризуются большими значениями вязкости и плотности 5(О давлении пара в системах СаС12—NaCl— Н20, СаС12—КС!—Н20 и СаС12—НС1—Н20 см.6-7.
В системе СаС12—MgCl2—Н20 в интервале температур от 0 до 170° кристаллизуются MgCl2-6H20, CaCI2-6H20, 2MgCh • СаС12 •
12Н20, СаС12-4Н20 (стабильная и метастабильная), СаС12-2Н20, MgC!2 • 2СаС12 • 12Н20, MgCl2 • 2СаС!2 • 6Н20 и MgCl2-6H20. Наименьшую растворимость при 55° имеет инконгруэнтно растворяющаяся двойная соль MgC!2 • 2СаС12 • 12Н20. По сравнению с изотермой 25° ветвь кристаллизации этой соли при. 55° больше приблизительно в 5 раз8. В безводной системе СаС]2—MgC!2 эвтектической точке соответствуют 51% СаС12 и 611°.
В водной системе Са2+, Mg2+, К+ЦС1- между 18 и 93° с увеличением температуры возрастает поле кристаллизации СаС]2-
2MgC!2 • 12Н20, появляющееся при 22°, и уменьшаются поля кристаллизации СаС]2 • 6Н20 и MgC]2 • 6Н20. Увеличивается также поле кристаллизации СаС!2 • КС1 за счет полей СаС12 • 2Н20 и карналлита. При 92° начинает кристаллизоваться 2СаС!2- MgCI2-
6Н20, поле кристаллизации которого возрастает при дальнейшем повышении температуры за счет полей СаС12 • MgC!2 • 12Н20 и СаС12 • 2Н209.
ПРИМЕНЕНИЕ
Хлорид кальция используют в производстве хлорида бария, некоторых красителей, для коагуляции латекса, в химико-фармацевтической промышленности, при обработке сточных вод, в системах для кондиционирования воздуха, при экстракции масел и др.10. Ё связи с большой гигроскопичностью его часто применяют в качестве осушителя газов и жидкостей. Его применяют также для получения металлического кальция электролизом, для производства кальциевых сплавов и баббитов.
Низкие температуры замерзания водных растворов хлорида кальция позволяют применять его в качестве хладоносителя в холодильном деле и в качестве антифриза для двигателей внутреннего сгорания в авиации, автомобильном транспорте, для борьбы с гололедицей, для предотвращения смерзаемости угля и руд при транспортировании в зимнее время и др. Существенным недостатком его является сильное коррозирующее действие на металлы, которое уменьшается при введении в раствор хлорида кальция окислителей —хроматов или бихроматов 12. Коррозия уменьшается и в присутствии ионов магния. Раствор СаС12 - Ь MgCl2 также служит жидкостью с низкой температурой замерзания. Его приготовляют как из твердых солей, так и смешивая, например, конечный карналлитовый щелок (стр. 161) с предварительно упаренной дистиллерной жидкостью содового производства 13.
За рубежом масштабы применения хлорида кальция весьма велики вследствие использования его для обеспыливания грунтовых и щебеночных дорог и при строительстве дорог. Периодическое (3—4 раза за летний сезон) нанесение раствора СаС12 устраняет пылеобразование. При строительстве дорог СаС12 используют в качестве одного из компонентов цементо-грунта — подстилающего слоя дороги. При строительстве 1 км силикатированной дороги расходуют ~3т 75% раствора СаС12.
В присутствии СаС12 ускоряется твердение бетона и увеличивается морозостойкость строительных растворов. Некоторое распространение в последние годы хлорид кальция получил в качестве добавки к шихте при производстве кирпича-сырца на заводах с естественной сушкой.
Хлорид кальция можно применять для предотвращения пыле- ния угля, в частности для предотвращения появления взрывоопасной угольной пыли в шахтах, а также в качестве гербицида для уничтожения сорняков на железнодорожных путях.
Хлорид кальция может быть использован для мелиорации солонцовых почв с большей эффективностью, чем гипс. Возможно также использование его раствора в качестве тяжелой жидкости при углеобогащении.
24 М, Е. Позин
Хлорид кальция выпускают в виде раствора, плавленого продукта (порошкообразного, чешуйчатого или гранулированного), представляющего собой смесь двух - и четырехводного кристаллогидратов, и в виде кальцинированного, обезвоженного продукта (порошкообразного или гранулированного) (табл. 50).
ТАБЛИЦА 50
|
Требования к качеству хлорида кальция (содержание компонентов в %)
|
Кальцинированный и плавленый хлорид кальция упаковывают в металлические барабаны, в полиэтиленовые или бумажные пятислойные битумированные мешки. Предложено перевозить его в железнодорожных цистернах, загружаемых горячим концентрированным раствором СаС12, затвердевающим при естественном охлаждении. Для разгрузки в цистерну необходимо подать воду или разбавленный раствор в количестве, требующемся для получения стандартного раствора!4.
СЫРЬЕ
Сырьем для производства плавленого хлорида кальция служат промышленные отходы растворов хлорида кальция, получающиеся в больших количествах на содовых заводах, при производстве хлората калия и др.
Дистиллерная жидкость, получающаяся в производстве соды по аммиачному способу при регенерации аммиака по реакции 2NH4C1 + Са(ОН)2 = СаС|2 + 2Н20 + 2NH3
Имеет плотность 1,12—1,13 г/см3 и содержит 9,2—11,3% СаС12, 4,7—5% NaCl и небольшие количества растворенных гипса, гидроокиси кальция и аммиака в смеси с взвешенным осадком. Последний состоит из СаСОз, Са(ОН)2 и CaS04-2H^0; количество осадка равно 20—25 кг/м3. На каждую тонну производимой соды, выбра -
Получение плавленого СаСЬ из дистиллерной жидкости 743
Сывается в дистиллерной жидкости более 1 г СаС12 и 0,5—0,6 т NaCl.
В производстве бертолетовой соли после кристаллизации KClOg остается маточный щелок, содержащий 400—500 г/л СаСЬ, по 10— 20 г/л КСЮз и КС1 и незначительные количества других примесей. Этот щелок является отходом производства и выпускается в виде товарного продукта, применяемого для разных целей, в частности для производства хлорида бария (см. гл. XII). Путем его выпаривания получают твердый (плавленый) хлорид кальция.
Для производства хлорида кальция сырьем служат также соляная кислота и высококачественный известняк, содержащий малые количества примесей R2Os, MgO, Si02, S и P.
В некоторых случаях хлорид кальция (22—25% раствор) получают из хлормагниевого рассола, обрабатывая его гашеной известью и отделяя на фильтре осадок гидроокиси магния 15.
Хлорид кальция образуется при хлорировании окиси кальция выше 600°16, а также при хлорировании сульфата кальция в среде расплавленного СаС12 в присутствии восстановителя выше 800° 17>18. Эти способы получения СаС12 в промышленности не применяются.