Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Химические способы получения хлористого магния
Химическая переработка морской воды
|
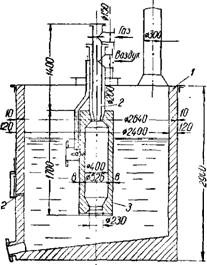
Рис. 87. Выпарной аппарат с погруженной горелкой (разрез): / — выпарной аппарат; 2 — горелка; 3 — каМера сгорания. |
Хлористый магний получают из морской воды также без ее предварительного концентрирования и садки NaCl, непосредственным осаждением известковым молоком гидроокиси магния,(стр. 287) и растворением ее в соляной кислоте. Осадок (кек),
содержащий ~25% Mg(OH)2, смешивают с разбавленным раствором MgCl2 и нейтрализуют соляной кислотой. Полученный раствор, содержащий ~15% MgCl2, выпаривают. Этот способ позволяет получать Mg(OH)2, а затем и хлористый магний, не содержащие соединений бора, которые не осаждаются при больших значениях рН. Хлористый магний, перерабатываемый на металлический магний, не должен содержать больше 0,001% бора.
Источником хлора для перевода суспензии Mg(OH)2 в MgCl2 может служить раствор СаС12 — дешевый отход содового производства. Суспензию Mg(OH)2 в растворе СаС12 подвергают76 карбонизации:
Mg(OH)2 + СаС12 + С02 = MgCl2 + СаС03 + Н20
После отделения осадка получается раствор, содержащий около 10% MgCI2 и некоторое количество NaCl. При выпаривании раствора до 35% MgCl2 основная часть NaCl выкристаллизовывается и отделяется.
Получение хлористого магния из доломита
Полностью обожженный доломит гасят водой при 95—100°. Полученную пульпу, содержащую ~11% твердой фазы, подвергают карбонизации при 60—40°. При этом карбонизуется только гидроокись кальция, переходящая в углекислый кальций77. Кар - бонизованную пульпу подвергают селективной нейтрализации соляной кислотой при рН = 7 — 8 во избежание растворения СаСОз. Соляную кислоту приливают медленно, чтобы скорость нейтрализации ОН- не превышала скорости растворения Mg(OH)2. После отделения осадка отстаиванием получаемый раствор содержит около 16% MgCl2. Часть этого раствора возвращают на взмучивание после первого отстаивания, а часть направляют на вторичное отстаивание, а затем на выпарку32.
Предложено78 подвергать карбонизации при температуре ниже 40° суспензию из доломитового молока, сульфата кальция и хлорида щелочного металла (при молярном отношении MgO : CaS04: : MCI = 1:1:1). К концу карбонизации суспензию нагревают до кипения. Образовавшийся СаСОз отделяют от раствора, затем из него выкристаллизовывают сульфат щелочного металла, а маточный раствор, содержащий MgCl2, выпаривают.
Для получения MgCl2, не содержащего СаС12, рекомендуют79 производить карбонизацию доломитового молока, полученного гашением обожженного доломита раствором NH4CI, взятым в количестве, необходимом для обменного разложения половины окислов доломита. При карбонизации в осадок выделяется основная двойная углекислая соль кальция и магния СаСОз• Mg(OH)2, а В растворе остается MgCl2. Осадок также обрабатывают раствором
NH4C1 для перевода Mg(OH)2 в MgCl2. Возможно использовать для регенерации аммиака в содовом производстве вместо известкового молока доломитовое молоко, с образованием при этом MgCb80'". При обработке жидкости теплообменника дистилляции доломитовым молоком вначале реагирует с NH4C1 гидроокись кальция. Гидроокись магния вступает в реакцию во вторую очередь и может прореагировать при 95° полностью лишь при отгонке аммиака. Без отгонки NH3 реакция между Mg(OH)2 и NH4C1 протекает лишь на 45—50%, идет медленно и зависит от активности окиси магния (стр. 287).
Хлористый магний из сульфатных растворов
Отбросный щелок в производстве сульфата калия, содержащий 2,9—3,2% К 5,5-6,5% Mg2+, 17—18% С1" и5-12% SOi", предложено перерабатывать следующим методом82. Вначале щелок выпаривают и кристаллизуют лангбейнит, причем удаляете^ до 80% SO4". Оставшийся S04~ осаждают хлористым кальцием, отделяют CaS04 и раствор выпаривают и выкристаллизовывают из него карналлит и галит. Полученный раствор хлористого магния направляют на выпарку.
В Техасе (США) хлористый магний, необходимый для производства металлического магния, получают из лангбейнитовой руды и из доломита83. Обменным разложением лангбейнита с КС1 выделяют K2SO4. Из оставшегося раствора, содержащего около 13% MgCla (при общем содержании солей — 30%), вакуум-кристаллизацией извлекают карналлит, а раствор MgCl2 концентрируют в аппаратах с погруженным горением, причем он окончательно очищается от КС1 и других солей. Обезвоженный хлористый магний направляют на электролиз, а выделяющийся при электролизе хлор перерабатывают в соляную кислоту, которую используют для нейтрализации бикарбоната магния, получаемого из доломита. Образовавшийся при этом раствор MgCl2 концентрируют и после обезвоживания также направляют на электролиз.