Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
СУЛЬФАТ МАРГАНЦА
Сульфат марганца получают способами, рассмотренными выше, из природной двуокиси марганца (стр. 767) и из бедных руд (стр. 761). В связи с возрастающей потребностью в сульфате марганца как микроудобрении и для переработки его в другие соединения изыскиваются и другие способы его производства. Многие из них также основываются на предварительном восстановительном обжиге природной руды, например а. ммиачный способ, в котором выщелачивание восстановленной руды производится сульфатом аммония 21 •105. Другие способы основаны на обработке серной кислотой марганцовой карбонатной руды 50'106.
Серную кислоту, образующуюся в результате побочной реакции окисления S02 в H2S04 под каталитическим влиянием ионов марганца, нейтрализуют добавкой к суспензии карбонатной руды (10—15% от начального количества руды). При этом облегчаются отстаивание и фильтрация пульпы. Очистка раствора достигается его подщелачиванием до рН = 7—8, причем железо, фосфор и другие примеси осаждаются. После отстаивания и фильтрации осадок с фильтра, промытый водой, направляют в отброс, промывные воды — на приготовление пульпы, а раствор MnS04 — на дальнейшую переработку.
Запатентован способ получения MnS04 из карбонатной руды обработкой ее разбавленной серной кислотой (отношение Мп : H2S04, равное 1 : 2,1, Ж : Т « 3) в присутствии катализатора KI107. Процесс ведут при рН = 2—3, температуре 80—90° и при 'вдувании воздуха почти до полного выщелачивания марганца. Затем горячую пульпу фильтруют, раствор MnS04 направляют на переработку, а осадок промывают холодной водой и промывную воду возвращают на разложение руды.
Растворение карбонатной руды ускоряется в присутствии окис - ной руды (пиролюзита) 108.
Когда сульфат марганца является промежуточным продуктом производства, его раствор перерабатывают электролизом, осаждением марганца в виде карбоната или гидроокиси и т. д. Термическая диссоциация твердого сульфата марганца позволяет регенерировать из него серу и окислы марганца. Добавка к обжигаемому сульфату марганца 5—10% угля ускоряет процесс его разложения. Приемлемые для практических целей скорости разложения MnS04 в атмосфере воздуха достигаются при 850°, азота — при
800°, причем твердые продукты обжига состоят почти целиком из МП3О4, а газовая фаза содержит серу в виде SO2 (содержание S03 меньше 3% от суммы S02 + SO3)109.
Выделение кристаллического сульфата марганца из его раствора осуществляется выпариванием и кристаллизацией или высаливанием концентрированной серной кислотой.
Ввиду того, что растворимость сульфата марганца с повышением температуры в интервале от 27 до 100° понижается, кристаллизация охлаждением концентрированного раствора оказывается
Невозможной. Изотермическая кристаллизация при выпарке из раствора воды, т. е. выпарка «на кристалл» несколько затруднена, потому что на греющих поверхностях выпарного аппарата нарастает толстый слой соли, сильно снижающий коэффициент теплопередачи Кроме того, при выпарке образуются чрезвычайно мелкие кристаллы MnS04 • Н2О, отделение которых на фильтре от маточного раствора идет крайне медленно.
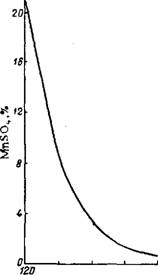
Для избежания этих трудностей кристаллизацию сульфата марганца можно осуществлять нагреванием раствора по. Растворимость сульфата марганца выше 100° резко снижается (рис. 210); в твердой фазе находится одноводная соль MnS04'H20. Если, например, исходный раствор содержит 20% MnS04, то при нагревании его до 160° в твердую фазу выделится 86%, а при 180° — 94% от общего количества MnS04.
Выделение сульфата марганца может быть осуществлено нагреванием раствора до 160° в автоклаве острым паром, имеющим давление 7—8 ат. Достаточно 15-минутной выдержки при этой температуре, чтобы в маточном растворе осталось 3,8% MnS04. Затем маточный раствор спускают через фильтр, находящийся внутри автоклава, и в автоклав загружают новую порцию свежего раствора. После двух - или трехкратной кристаллизации соль выгружают. Наиболее подходящим материалом для автоклава является медь или бронза.
|
140 160 160 Температура, "С |
|
Рис. 210. Растворимость MnS04 В воде при 120-200°. |
Маточный раствор от кристаллизации может быть употреблен для разбавления серной кислоты, идущей в производство ГАПа, вследствие чего конечный выход сульфата марганца будет бли - 8ок к 100%. Так как в исходном растворе сульфата марганца со
держится около 1% MgS04, то в маточном растворе будет накапливаться сульфат магния. Присутствие последнего благоприятствует кристаллизации MnS04 • Н20, так как понижает его растворимость. Часть маточного раствора должна периодически из цикла выводиться.
Растворимость сульфата марганца в присутствии серной кислоты сильно падает. Так, при 25° при содержании в растворе 40,8% H2S04 растворимость MnS04 составляет 3,8%, при 62% H2S04— 0,5%. При концентрации H2S04 ниже 62% твердой фазой является MnS04-H20, при более высокой концентрации — MnS04. При еще более высокой концентрации и низкой температуре в твердую фазу выделяется кислая соль MnS04 • H2S04 • Н20.
На основании этого Д. М. Корфом предложена следующая схема извлечения сульфата марганца из раствора. К раствору добавляют серную кислоту до концентрации 40% H2S04. При этом выпадает в осадок около 80% сульфата марганца. Отделенный осадок, содержащий до 40% маточного раствора, промывают раствором сульфата марганца. Растворы от промывки поступают на высаливание серной кислотой. Полученная соль содержит около 68% MnS04 и 0,3—0,6% H2S04. Недостатком этого способа является большой расход серной кислоты, примерно в 3 раза превышающий расход ее на производство ГАПа. Получающаяся после высаливания слабая серная кислота лишь частично может быть использована для производства ГАПа, что и затрудняет реализацию этого способа.