Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Разложение фосфата фосфорной кислотой (II стадия реакции)
После разложения основной массы фосфата серной кислотой оставшаяся непрореагировавшая его часть взаимодействует с Накопившейся в системе фосфорной кислотой (II стадия). Первая стадия — разложение фосфата серной кислотой, как указано было выше, протекает быстро вследствие большой активности раствора (высокой концентрации ионов водорода), а также расходования наиболее мелких частиц фосфата. Во второй стадии апатит разлагается водным раствором фосфорной кислоть^ в котором все больше накапливается монокальцийфосфата. По мере увеличения сте
пени нейтрализации фосфорной кислоты активность раствора уменьшается и скорость процесса замедляется И6-ш. Когда жидкая фаза становится насыщенной фосфатами кальция (моно - и дикальцийфосфатом), что совпадает с окончанием созревания суперфосфатной массы в камере, скорость разложения еще больше уменьшается. Это обусловлено, помимо уменьшения активности жидкой фазы, образованием на зернах непрореагировавшего фосфата плохо проницаемых корок, но уже не сульфата, а фосфатов кальция, кристаллизующихся из пересыщенных растворов системы СаО—Р2О5—Н2О118*. Образовавшаяся в I стадии корка сульфата кальция на зернах фосфата уже в самом начале II стадии создает дополнительное сопротивление диффузии фосфорной кислоты к реагирующей твердой поверхности. Помимо этого после завершения I стадии непрореагировавший фосфат состоит из относительно крупных частиц, что приводит к уменьшению поверхности контакта фаз. Тем не менее, в камере II стадия процесса протекает еще с достаточной скоростью вследствие высокой температуры и разложения фосфата мало нейтрализованными растворами фосфорной кислоты. Но в дальнейшем при дозревании суперфосфата на складе процесс идет очень медленно.
Режим разложения апатита фосфорной кислотой при созревании суперфосфата вплоть до окончания камерного процесса, определяется первоначальными условиями производства, т. е. концентрацией и нормой серной кислоты, температурой процесса и режимом смешения реагентов. Протекание процесса непосредственно в камере обычно не регулируется. В табл. 61 приведен типичный состав камерного суперфосфата в зависимости от метода производства 68.
|
Из апатитового концентрата |
|
19,9 |
16,7 |
11,9 |
14,5 |
70,6 |
83,9 |
|
20,3 |
17,15 |
12,2 |
13,2 |
71,8 |
84,5 |
|
20,7 |
17,8 |
12,2 |
12,7 |
69,8 |
86,0 |
|
Фосфорита Каратау (Чулактау) | 15,1 I 12,7 I 8,0 [ 12,0 I 64,0 I 84,0 |
ТАБЛИЦА 61
|
Состав камерного суперфосфата
Периодический. . Полунепрерывный Непрерывный. . . 1,98 1,94 1,90 |
Из
Периодический
^ ^Подробно о скорости разложения фосфатов фосфорной кислотой см.
Дальнейшее разложение фосфата протекает на складе, где имеется возможность в известной степени ускорять процесс. Это основано на изменении фазового состава фосфатного комплекса суперфосфата 43.
Фосфатный комплекс суперфосфата и его фазовый состав
Фосфатным комплексом называют систему, состоящую из твердых и растворенных фосфатов кальция, свободной фосфорной кислоты и воды, т. е. всех главных компонентов системы, за вычетом
|
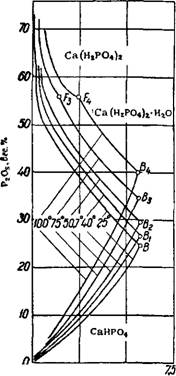
Рис. 218. Система СаО—Р205—Н20. |
|
2,5 5 СаО, бес. % |
Непрореагировавшего апатита, CaS04 и HF. Поэтому состав фосфатного комплекса определяется с помощью диаграммы равновесия в системе СаО—Р205—Н20 119"12s (рис. 218). Возможность применения этой диаграммы для определения фазового состава фосфатного комплекса суперфосфата, полученного из апатитового концентрата, обусловлена тем, что образовавшийся сульфат кальция (и стронция) находится в твердой фазе и уже не принимает участия в химических реакциях. Фтористые соединения частично улетучиваются, а частично образуют малорастворимые соединения — крем - нефториды, фторкомплексы алюминия и пр. Примесей других минералов в апатитовом концентрате всего 3%. Поэтому без большой погрешности II стадию процесса получения суперфосфата можно рассматривать как растворение в фосфорной кислоте гидро - ксилапатита Са5(Р04)3(0Н). При этом происходит постепенная нейтрализация фосфорной кислоты. Степень нейтрализации первого иона водорода фосфорной кислоты определяется отношением количества Р205, связанной с СаО в виде монокальцийфосфата, к общему содержанию Р205 в жидкой фазе. По окончании I стадии процесса степень нейтрализации равна нулю —жидкая фаза представлена свободной Н5Р04. Во II стадии фосфорная кислота реагирует с остальной частью фосфата, образуя раствор фосфорной кислоты и монокальцийфосфата, находящийся в равновесии с твердой фа
зой: моно - или дикальцийфосфатом. С увеличением степени разложения фосфата степень нейтрализации возрастает, с увеличением нормы серной кислоты она уменьшается.
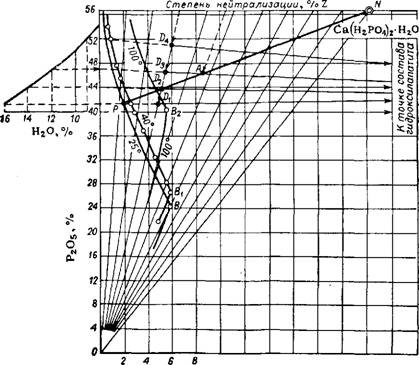
В нижней части рис. 219 приведены изотермы системы СаО—Р205—Н20 для 25, 40 и 100°. Пучок лучей, исходящих из точки начала координат диаграммы, представляет шкалу степени нейтрализации. Луч 100%-ной нейтрализации заканчивается в точке iV, отражающей состав монокальцийфосфата Са(Н2Р04)2- •Н20 (Р205—56,34% и СаО — 22,22%).
В верхней части рисунка дана зависимость степени нейтрализации от степени разложения апатитового концентрата при двух нормах серной кислоты (п), а слева второй вспомогательный график зависимости между концентрацией Р205 в жидкой фазе к началу I стадии процесса и конечной влажностью готового суперфосфата (при норме H2S04 72 вес. ч). На рис. 219 нанесены лучи растворения гидроксилапатита в фосфорной кислоте различной концентрации. Эти лучи направлены в точку состава Са5(Р04)3(0Н) (Р2О5 — 42,39% и СаО — 55,82%), находящуюся за пределами диаграммы. Точки составов фосфатного комплекса лежат на пересечении лучей растворения и степени нейтрализации. Например, при норме серной кислоты 72 вес. ч., коэффициенте разложения апатита 92% и влажности суперфосфата 12%, состав фосфатного комплекса изобразится точкой A (P20s — 46,2% и СаО—8,5%). Эта точка находится в поле кристаллизации Са (Н2Р04) 2 • Н20 при 25—100°; следовательно, фосфатный комплекс суперфосфата в приведенном примере состоит из жидкой фазы (раствор фосфорной кислоты и монокальцийфосфата) и монокальцийфосфата в твердой фазе. С помощью луча кристаллизации, проведенного из точки N Через точку А, подсчитывают, по правилу рычага, соотношение между количествами жидкой и твердой фаз в комплексе при различных температурах. Точки пересечения луча кристаллизации с изотермами (например, точка Р для 25°) определяют состав жидкой фазы при соответствующей температуре.
При норме серной кислоты 72 вес. ч. степень разложения апатита в камерном суперфосфате составляет в среднем 87% (точка С На рис. 219) и степень нейтрализации жидкой фазы равна 30%. При влажности суперфосфата 16, 14, 12 или 9% луч степени нейтрализации жидкой фазы суперфосфата пересечет соответствующие лучи растворения в точках Db D2, D3 или D4. Из положения этих точек можно заключить, что при влажности суперфосфата 16% фосфатный комплекс при 100° и выше совсем не содержит твердого монокальцийфосфата (точка Dx лежит в поле ненасыщенных растворов), а при влажности 14% содержит его очень мало (точка D2 лежит близко к 100°-ной изотерме). Чем меньше влажность суперфосфата, тем больше образуется кристаллического монокальцийфосфата в фосфатном комплексе камерного суперфосфата
|
Is 96 |
|
Рис. 219. Номограмма для определения фазового состава фосфатного комплекса суперфосфата (из апатитового концентрата). |
|
10 12 14 IS 18 20 22 24 26 СаО, % |
(см. положение точек D3 и D4 по отношению к 100°-ной изотерме). Охлажденный до 40—25° камерный суперфосфат содержит. в фосфатном комплексе твердый монокальцийфосфат при влажности продукта 16% и меньшей. Содержание влаги в свежеприготовленном суперфосфате из апатитового концентрата при применении 61—62%-ной серной кислоты (норма 70 вес. ч.) составляет в среднем 16%, а при 68,5%-ной кислоте 12%.
В табл. 62 приведены результаты расчетов43 по диаграмме рис. 219 (при норме серной кислоты 68 вес. ч. и влажности продукта 14%).
ТАБЛИЦА 62
Количество жидкой и твердой фаз в фосфатном комплексе и в суперфосфате
|
Коэффициент разложения, % |
Фосфатный комплекс |
Суперфосфат |
Состав твердой фазы фосфатного комплекса |
||
|
Твердая фаза, 70 |
Жидкая фаза, % |
Твердая фаза, % |
Жидкая фаза, °/о |
||
|
Температура |
25° |
||||
|
85 |
20,5 |
79,5 |
65,1 |
34,9 |
Монокальцийфосфат |
|
90 |
32,7 |
67,3 |
68,7 |
31,3 |
» |
|
95 |
43,2 |
56,8 |
72,1 |
27,9 |
» |
|
100 |
54,2 |
45,8 |
76,3 |
23,7 |
» |
|
Температура |
50° |
||||
|
85 |
17,0 |
83,0 |
63,6 |
36,4 |
Монокальцийфосфат |
|
90 |
29,5 |
70,5 |
67,2 |
32,8 |
» |
|
95 |
41,0 |
59,0 |
71,0 |
29,0 |
» |
|
100 |
50,7 |
49,3 |
74,5 |
25,5 |
Мои о - + дикальцийфосфат |
|
Температура 100° |
|||||
|
85 |
8,3 |
91,7 |
59,2 |
40,8 |
Монокальцийфосфат |
|
90 |
19,6 |
80,4 |
62,7 |
37уЗ |
Моио - + дикальцийфосфат |
|
95 |
31,4 |
68,6 |
66,4 |
33,6 |
То же |
|
100 |
25,4 |
74,6 |
61,5 |
38,5 |
» » |
С увеличением степени разложения фосфата и с уменьшением температуры количество твердой фазы в суперфосфате в большинстве случаев возрастает. Повышение нормы серной кислоты уменьшает количество твердой фазы. Особенно резко возрастает содержание твердой фазы в продукте с уменьшением влажности суперфосфата или с ростом концентрации исходной серной кислоты.