Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ПРОИЗВОДСТВО ФОСФОРНОЙ кислоты СЕРНОКИСЛОТНЫМ СПОСОБОМ
Фосфорная кислота является основным полупродуктом в производстве фосфорных и сложных концентрированных удобрений и других фосфорсодержащих соединений.
Один из распространенных способов ее получения — сернокислотный— заключается в разложении природных фосфатов серной кислотой и в отделении образующейся твердой фазы — сульфата кальция от раствора фосфорной кислоты. Он называется экстракционным, или мокрым, способом в отличие от термического (см. гл. XXVI).
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Фосфорной кислотой упрощенно называют ортофосфорную кислоту Н3РО4. Она изготовляется и применяется в виде водных растворов; концентрированные растворы имеют консистенцию густого сиропа. Безводная фосфорная кислота кристаллизуется в виде бесцветных призматических кристаллов ромбической системы, плавящихся при 42,35°; они легко расплываются на воздухе. При 284° н давлении 1 ат начинается дегидратация ортофосфорной кислоты и превращение ее в пирофосфорную H4P207 и метафосфор - ную НР03 кислоты.
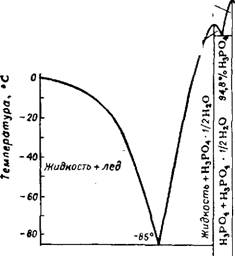
На рис. 233 изображена диаграмма растворимости в системе. Н3РО4—Н2О. Твердыми фазами являются: лед, Н3Р04 и Н3РО4 • 0,5Н20 (или 2Н3РО4 ■ Н20). В системе Р205—H20'-14 имеется твердая фаза Н4Р207 — пирофосфорная кислота (стр. 942).
Безводная ортофосфорная кислота Н3Р04 содержит 72,4 % Р2О5. При ее термической дегидратации или при взаимодействии с фосфорным ангидридом образуется полифосфорная кислота, содержащая больше 72,4% Р2О5 и состоящая из смеси разных фосфорных кислот: орто-, пиро - (Н4Р207), Триполи- (Н5Р3О.0}
Тетраполи- (НбР^з), мета - (НР03) и полиметафосфорной. Соотношение между этими кислотами зависит от общей концентрации Р2О5 в растворе, а при наличии в нем полимерных метафосфорных кислот с общей формулой (НРОз)п — и от времени (способа получения). Это объясняется тем, что гидратация и дегидратация метафосфорных кислот происходит
42>4 медленно.
Кислота с концентрацией 70—80% Р205 (что эквивалентно 96—110%- ной Н3РО4) называется суперфосфорной кислотой. Пиро - и триполифос - форная кислоты эквивалентны, соответственно, 110% - и 114%-ной Н3РО4. Суперфосфорная кислота с концентрацией 75,6% Р205 содержит 49% Р205 в виде ортофосфорной, 42% —в виде пирофос - форной, 8% в виде три - полифосфорной и 1% — в виде тетраполифосфор- ной кислот. При разбавлении суперфосфорной кислоты водой происходит значительное выделение тепла и полифосфорные кислоты быстро гидратируются до ортофосфорной. Плотность суперфосфорной кислоты 1,92—2 г/см3. Она имеет очень большую вязкость (400—1000 сл при 66°) и менее активно действует на металлы и сплавы, чем обычная ортофосфорная кислота. Температура замерзания суперфосфорной кислоты ~0°.
|
♦ 40 - |
|
Жидкость +Н3РО4 29,3' |
|
Жидкость + H3P04*J/2H20 у |
|
-юоь |
|
62,5% Н3Р04 Н3РО4 • T/2UzO + /Ied 91,6%Н3РОл |
|
20 40 60 80 Содержание Н3РО4, вес.% I________ I________ I________ О 20 40 60 Содержание Рг05, вес. 7« |
|
Ю0 |
|
Рис. 233. Диаграмма растворимости стеме Н3РО4—Н20. |
|
В си - |
В водных растворах фосфорная кислота ионизируется. Константы ионизации 0,1—0,01 н. фосфорной кислоты следующие:
|
Н3р04 н2ро; нроГ |
|
25 25° 18° |
|
10" 10" |
|
Прн прн прн |
|
Н+ + HPOJ - Н+ + POJ" |
/с, = 7,52 ■ К,- 6,31 •
К, = 2,2-10"
Теплота растворения 1 моль Н3РО4 в 1 моль воды составляет 1,741, в 20 моль — 4,998, в 100 моль — 5,269 кал/г-мол.
|
ТАБЛИЦА 68 Температуры кипения водных растворов фосфорной кислоты1,11
|
Вязкость 6>7 растворов Н3Р04 при 75° по отношению к воде (25°) при концентрации около 27% Н3Р04 равна 1,967, при 68% Н3Р04 — 9,506, при 88,2% Н3Р04—28,61, при 97,35% Н3Р04 — 59,24 сп.
Давление пара растворов фосфорной кислоты 8-12 приведено на рис. 234 (в паре только НгО), а температуры кипения в табл. 68.
Средняя теплоемкость13 (при 20—100°) водных растворов Н3РО4 с концентрацией от 0 до 60% определяется уравнением: С = 1,0109 — 0,00709л:, где х — концентрация Н3Р04, в %.
ПРИМЕНЕНИЕ
|
Рис. 234. Давление пара растворов' фосфорной кислоты. |
Фосфорная кислота, получаемая сернокислотным методом, применяется главным образом в производстве концентрированных удобрений (см. гл. XXVII, XXVIII, XXXIII). В США для этой цели использумт около 93% всей экстракционной фосфорной кислоты 15—21. В меньших количествах она потребляется для получения промышленных продуктов (см. гл. XXX). Производство фосфорной кислоты сернокислотным способом расширяется за последние годы во многих странах, так как увеличивается спрос на концентрированные удобрения и растет использование побочных продуктов (соединений урана, ванадия и фтора), выделяемых в процессе разложения фосфатов серной кислотой22-26. Имеет значение и более низкая стоимость экстракционной фосфорной кислоты по сравнению с термической (см. гл. XXVI).
Состав экстракционной фосфорной кислоты зависит от применяемого фосфатного сырья27-29 и условий ее производства. Кислота, получаемая из апатитового концентрата дигидратным способом (с выделением сульфата кальция в виде дигидрата или гипса CaS04-2H20), содержит 25—32% Р205, 1,8—2,8% S03, 0,8—1,1% Fe203, 0,5—1,0% А120з, 0,2—0,4% СаО, 1,5—1,8% фтора и имеет плотность 1,25—1,3 г/см3. При использовании фосфоритов, в состав которых входит значительное количество нерастворимых примесей (кремнезема, силикатов и других), образуется более разбавленная кислота с концентрацией 20—25% Р2Об вследствие необходимости применения для отмывки осадка большего количества воды. При наличии в фосфоритах соединений магния последние также переходят в кислоту, которая в этом случае содержит 1—3,5% MgO. Содержание других примесей колеблется в тех же пределах, что и в кислоте, полученной из апатитового концентрата. Во многих случаях получаемую разбавленную кислоту упаривают до концентрации 53—55% Р2О5, необходимой для производства концентрированных фосфорных и сложных удобрений.
Концентрированную экстракционную кислоту получают также без упарки полугидратным методом (с выделением сульфата кальция в виде полугидрата CaS04 • 0,5Н20) и она содержит 47—48% Р205, 0,9-1,1% Я203, 0,2—0,4% SOf, 0,2-0,7% фтора, 0,1-0,2% СаО. Ее применяют для получения кормовых фосфатов и удобрений.