Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Получение хлористого калия из карналлита
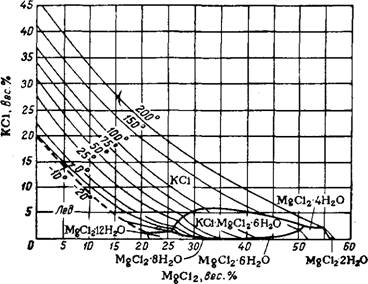
В системе KCI—MgCl2—Н20 карналлит КС1 • MgCl2 • 6Н20 стабилен в интервале температур от —21 до +167,5° (рис. 46). Он растворяется инконгруэнтно — при обработке ограниченным количеством воды в раствор переходит MgCI2, а КС1 остается в твердой фазе. При испарении раствора карналлита кристаллизуется сначала КС1, а затем карналлит с растворением ранее выпавшего КС1. Если до начала кристаллизации карналлита отделить выкристаллизовавшийся КС1, а оставшийся раствор продолжать выпаривать или охлаждать, то в обоих случаях будет кристаллизоваться карналлит.
Природный карналлит загрязнен примесями сильвина и галита. При переработке карналлита методами растворения и кристаллизации щелоки насыщены хлористым натрием, который выделяется вместе с КС1, загрязняя продукт. При кристаллизации КС1 из горячего раствора, насыщенного KCI и NaCl, он будет тем чище, чем меньше в растворе хлористого магния.
Все существующие методы переработки карналлита основаны на большей растворимости хлористого магния по сравнению с растворимостью хлористого калия и делятся на способы полного и Неполного растворения48'50-52. Первые способы заключаются в полном растворении карналлитовой руды горячим оборотным щелоком, в котором содержится значительное количество MgCl2 и мало КС1 (например, 280 г/л MgCl2, 40 г/л КС1 и 40 г/л NaCl). При охлаждении полученного раствора большая часть хлористого калия кристаллизуется (с примесью NaCl). Маточный раствор выпаривают и охлаждают; при этом кристаллизуется карналлит КС1 • MgCh • 6Н20, называемый, в отличие от прирбдного, искусственным. Его используют для получения магния, или для
В М. Е. Познн Извлечения КС1 тем же путем, как и из природного карналлита. В конечном щелоке содержится большое количество MgCl2.
Способы неполного растворения, при которых КС1 полностью не растворяется, а остается частично в шламе, называют также «шламовыми». Основными из них являются способы холодного разложения, растворения «на конечный щелок» и «конечным щелоком».
Холодное разложение карналлита ведут обработкой его водой или оборотным щелоком без нагревания, причем большая часть
|
Рис. 46. Растворимость в системе КС1—MgCl2—Н20. |
КС1 извлекается в виде тонкого шлама, взвешенного в жидкости. После удаления галитового отвала шламовый хлористый калий отделяют от щелока, из которого выпариванием и охлаждением кристаллизуют искусственный карналлит, присоединяемый к природному карналлиту, идущему на разложение. Остающийся раствор хлористого магния, содержащий мало примесей, перерабатывают на твердый плавленый хлористый магний (см. гл. IX).
Растворение «на конечный щелок» или горячее шламовое разложение заключается в обработке карналлитовой руды маточным щелоком при ~100°. При этом в раствор переходит весь MgCl2 и часть КС1 из карналлита, а остальная часть КС1 из разложенного карналлита выделяется в виде шламового хлористого калия. После отделения галитового отвала (в котором остается и находившийся в руде сильвин), а затем шламового хлористого каЛия, раствор охлаждают для кристаллизации возвращаемого в цикл искусственного карналлита, а затем выпаривают для получения плавленого хлористого магния. Преимуществом этого способа является возможность получения без выпарки конечного щелока, богатого хлористым магнием и бедного хлористым калием.
По способу растворения «конечным щелоком» шламовому разложению подвергают предварительно полученный из природного карналлита искусственный карналлит, мало загрязненный галитом и потому отделение шлама КС1 от NaCl не производят. Галитовый отвал отделяют в первой стадии, после горячей обработки природного карналлита оборотным маточным щелоком, перед кристаллизацией искусственного карналлита.
Имеется много вариантов этих схем.
Способы холодного разложения отличаются тем, что в них практически весь КС1 остается нерастворенным; в горячих же способах КС1 полностью или частично растворяется.
Использование способов холодного разложения, как и горячих способов неполного растворения карналлита, приводит к получению менее ценного продукта, загрязненного глинистыми и другими нерастворимыми примесями, содержащимися в сырье, однако вполне пригодного как удобрение. Использование этих способов оказывается целесообразным при наличии сравнительно чистого карналлита.
Наиболее распространены способы полного растворения карналлита, они дают возможность получать наиболее чистый продукт, но требуют примерно в 1,5 раза большего расхода тепла, чем способы холодного разложения и почти в 2 раза больше тепла, чем способ растворения «на конечный щелок». Поэтому в тех случаях, когда состав природного сырья допускает возможность их использования, способы неполного растворения карналлита являются более экономичными.
Сложность выделения хлористого калия из карналлита значительно удорожает технологический процесс по сравнению с переработкой сильвинита. Переработка карналлита на хлористый калий более экономична, если она производится с использованием других компонентов, входящих в состав природного карналлита, и в первую очередь хлористого магния с целью получения соединений магния, металлического магния, хлора, хлорпроизводных и др.53 ■ .
В СССР хлористый калий из карналлита не вырабатывают. Карналлитовую руду перерабатывают способом неполного (шламового) растворения на необходимый для получения металлического магния искусственный карналлит,- Отходом в производстве магния электролизом карналлита является калийная соль, содержащая 75—80% КС1; ее выпускают в качестве удобрения под названием «электролит».
При переработке карналлита применяют такую же аппаратуру, как и при переработке сильвинита. Растворение карналлита идет с большой скоростью, поэтому его ведут и в вертикальных растворителях; по-видимому, целесообразно вести его в трубах, совмещая этот процесс с гидротранспортом.