Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ПОЛУЧЕНИЕ МЕДНОГО КУПОРОСА СУЛЬФАТИЗИРУЮЩИМ ОБЖИГОМ БЕЛОГО МАТТА
Существенным недостатком способа получения медного купороса из белого матта путем его окислительного обжига и последующего растворения полученной окиси меди в серной кислоте является то, что основное количество серы, содержащейся в белом матте, не используется. Между тем за счет этой серы теоретически возможно было бы перевести в медный купорос 50% меди, находящейся в белом матте, и тем самым снизить в 2 раза расход серной кислоты при последующей обработке продукта обжига. С этой целью белый матт должен подвергаться не простому окислительному, а сульфатизирующему обжигу, т. е. длительной прокалке при сравнительно невысоких температурах (400—500°) при достаточном избытке кислорода. В этих условиях реакции
2S02 + 02 2S03 CuO + S03 CuS04
Смещены направо и 60—70% сульфидной серы переходят в сульфатную, что соответствует превращению 30—35% меди в сульфат меди. Для обработки продукта обжига расходуется в 1,5 раза меньше серной кислоты, чем при простом окислительном (не сульфати - зирующем) обжиге, а общее использование меди достигает 90%.
Механизм образования сульфата меди при сульфатизирующем окислении белого матта можно представить следующими элементарными реакциями Ч Часть сульфида непосредственно окисляется в сульфат:
( и.2 3 + 2,502 = Си S04 + CuO
Наряду с этим происходит окисление сульфида меди с образованием двуокиси серы и окиси меди:
Cu2S + 1,Б02 = Cu20 + S02 Cu20 + 0.602 2CuO
Окись меди далее реагирует с серным ангидридом, образующимся при каталитическом окислении S02 в присутствии содержащейся в белом матте окиси железа, а частично аульфатизируетоя по реакциям
CuO + S02 = CuS03 4CtiS03 = 3CuS04 + CuS
С последующим окислением образующегося CuS. Для успешной сульфатизации белого матта необходимо обеспечить достаточно
Высокую концентрацию кислорода в газовой фазе. Этого можно достигнуть или использованием обогащенного кислородом воздуха или применением добавок, обладающих высоким равновесным давлением кислорода в температурных условиях обжига.
|
400 500 600 700 Температура, "С |
|
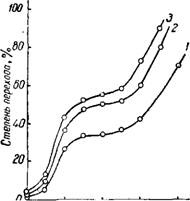
Рис. 192. Влияние температуры на переход Cu2S В CuS04 при разном содержании окиси меди в смеси. Содержание СиО в смеси (в %); 1 — 0; 2- 10; 3-25; 4-50. |
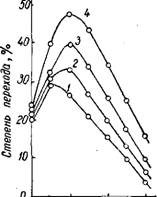
Степень перехода серы в газовую фазу в виде двуокиси серы значительно возрастает при добавке окиси меди (рис. 191) 53. Зависимость степени перехода сульфидной серы в сульфатную от температуры выражается кривой с максимумом (рис. 192), что объясняется разницей в скоростях образования и разложения сульфата
|
"400 500 600 700 600 Температура,°С Рис. 191. Степень перехода серы В газовую фазу при окислении сульфида меди в зависимости от Температуры: |
/ — без добавки СиО; 2 — при добавке К сульфиду меди 10% Си О; 3 — то же при 25% СиО. .
Меди (и промежуточных продуктов) при различных температурах. £тепень окисления сульфида меди при 450° в течение 60 мин в отсутствие добавки составляет 29,5%. С увеличением температуры выше 450° в этих условиях степень перехода сульфидной серы в сульфатную резко падает и при 750—800° практически равна нулю. В присутствии добавок окиси меди увеличивается степень перехода сульфидной серы в сульфатную, а температура, отвечающая максимуму сульфатообразования, сдвигается в сторону более высоких температур. При добавке 25% СиО в интервале 500—550° за 60 мин 35—40% сульфидной серы переходит в сульфатную, а общее количество окислившейся серы достигает 90—95% 53.
Наиболее интенсивно сульфатизирующий обжиг сульфидов и окислов меди идет в кипящем слое, особенно при предварительном мелком измельчении материала 54>55.
Изучена сульфагизация C112S крепкой серной кислотой. До 300° она идет по реакциям:
Cu2S + 2H2S04 = CuS + CuS04 + S02 + 2Н20 CuS + 2H2S04 = CuS04 + S02 + S + 2H20 S + 2H2S04 = 3S02 + 2H20
Наибольший выход CuS04 достигается при 200°. При высоких температурах частично улетучивается серная кислота и в результате взаимодействия CuS04 с Cu2S образуется Cu2S04, а затем Cu20 56.
Изучены условия превращения Cu2S в CuS04 путем автоклавного выщелачивания белого матта слабой серной кислотой в присутствии кислорода. При этом параллельно идут следующие реакции:
Cu2S + 2,502 + H2S04 = 2CuS04 + Н20 (1)
Cu2S + 02 + 2H2S04 = 2CuS04 + S + 2Н20 (2)
Скорость растворения Cu2S пропорциональна давлению кислорода в степени 0,5. Для преимущественного (на 93%) осуществления процесса по реакции (1), т. е. с полным использованием серы и с меньшим расходом серной кислоты, оптимальными условиями являются: давление кислорода ~4 ат, концентрация серной кислоты 0,01 моль/л, температура 140°57.
Аналогичным способом можно получать медный купорос из водной суспензии халькопиритного концентрата (Т: Ж = 1:3) с добавкой СаО или СаС03 для регулирования гидролиза образующегося сульфата железа и выделения H2S0458.