Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ОЧИСТКА ИОДА-СЫРЦА
Иод-сырец обычно содержит большее количество примесей органических веществ и минеральных солей, чем это допускается ГОСТ, и поэтому подвергается очистке. Для отделения водорастворимых солей лепешки иода промывают, для отделения остальных примесей иод сублимируют или обрабатывают сырец концентрированной серной кислотой.
|
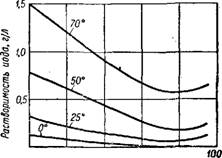
20 60 Кониентрзция H2SOt, Sec. % |
|
Рис. 74. Растворимость иода в сериой кислоте. |
Наиболее широко применяемый метод очистки — сублимацию осуществляют в стальных, чугунных или керамических ретортах, обогреваемых топочными газами. Пары иода кристаллизуются на стенках холодильников, представляющих собой систему керамических или асбоцементных труб, охлаждаемых воздухом. Для уменьшения влажности получающегося иода трубы-холодильники укладывают с небольшим наклоном, а в стыках труб оставляют отверстия для стока воды. Иногда иод-сырец перед сублимацией смешивают с 8— 12% негашеной извести. Для получения крупных кристал-
119
Лов, легко отделяемых от стенок холодильника 11а, температура паров иода в зоне конденсации ие должна быть выше температуры плавления иода (113,6°).
На некоторых заводах возгонку иода производят пропусканием перегретого водяного пара (ПО—120°) через слой иода-сырца. Пары иода и несконденсировавшиеся пары воды охлаждают в прямоточном холодильнике. Полученную пульпу, состоящую из кристаллов иода и воды, фильтруют через бязь и прессованные угольные плитки, а затем кристаллы иода отжимают на гидравлическом прессе. Расход пара 3,6 мгкал на 1 т иода.
Для очистки иода-сырца применяют также плавление его под слоем серной кислоты при 120—150° или промывку его 90—93% серной кислотой — при этом содержащиеся в сырце органические вещества обугливаются120-121. Использование более концентрированной кислоты не улучшает очистки, но увеличивает потери иода
из-за повышения его растворимости (рис. 74) т. Обработанный серной кислотой иод измельчают и промывают водой для удаления включений и серной кислоты. Потери иода составляют 2—3%, а расход серной кислоты 2—3 г на 1 г иода. Отработанную серную кислоту используют на других стадиях получения иода.
Для получения особо чистого иода123 иод-сырец возгоняют в вакууме или перекристаллизовывают его из раствора в четырех - хлористом углероде; захват примесей предотвращают с помощью стеклянной ткани.
ПОЛУЧЕНИЕ СОЛЕЙ ИОДА
Получение иодистых солей прямым взаимодействием иода с растворами гидроокисей в промышленности не применяется из-за трудности отделения от иодатов. Из диаграмм растворимости в сисяе-
20
|
О ю го зо 40 50 во то К!,% |
£
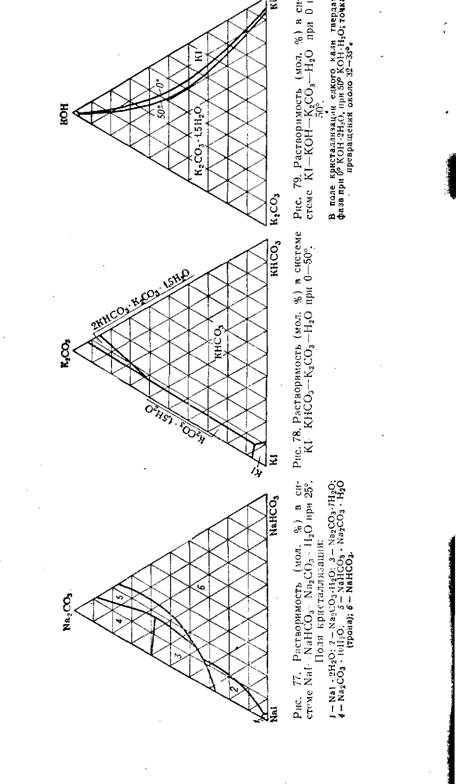
Мах KI—КЮз—Н20 и Nal—NaI03—Н20 (рис. 75 и 76) видно, что В чистом виде можно выделить только иодат калия или натрия124.
|
Рис. 76. Изотермы растворимости в системе Nal—NalOs—НгО. |
Иодиды же всегда будут загрязнены иодатами, и для удаления последних необходимо применять дополнительные операции.
По наиболее распространенному методу для получения иоди - дОВ 125,126 приготавливают раствор иодисто-иодного железа Fe3I8. Последний получают при взаимодействии железных стружек с
Иодом в присутствии воды: 3Fe + 4I2 = Fe3I8. Затем к раствору Fe3Is прибавляют растворы гидроокисей или карбонатов: Fe3I8 + 8iMOH = Fe304 + 8MI + 4Н20 Fe3I8 + 4М2С03 = Fe304 + 8MI + 4С02
Где М-К, Na, NH4.
Получение иодидов ведут в чугунных или стальных реакторах с мешалкой и паровой рубашкой. Раствор карбоната или гидроокиси нагревают до кипения, а затем медленно прибавляют раствор иоди - стоиодного железа. После 3—6-часового нагревания, с целью получения легко фильтрующего осадка Fe304, последний отделяют декантацией или фильтрованием, отжимают на фильтрпрессах и Промывают водой до практически полного извлечения иодидов. Первые промывные воды смешивают с основным раствором и выпаривают до получения насыщенного раствора, из которого выкристаллизовывают иодид. Кристаллы иодида центрифугируют, промывают и сушат при ~100°. При получении иодида аммония, последний частично разлагается и окрашивается иодом, а потому реакцию ведут при избытке аммиака в растворе, а окрашенные кристаллы промывают небольшим количеством спирта или отбеливают пропусканием через них паров аммиака. На некоторых за-4 водах вместо Fe3Is готовят раствор иодистого железа Feb и реакцию ведут по уравнению:
3FeI2 + I2 + 8МОН = Fe304 + 8MI+"4Н20
Иодиды также получают взаимодействием иодо-воздушной сме - си 1о°-105 (стр. 249) или иода 127 со щелочными растворами в присутствии перекиси водорода при 8—10° или в присутствии сероводорода:
I2 + 2МОН + Н202 = 2MI + 2Н20 + 02 ,
I2 + 2МОН + H2S = 2MI + 2Н30 + S
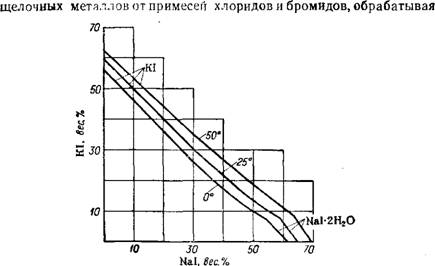
Выход иодида (в пересчете на иод) составляет 96—98%. Концентрации исходных растворов КОН, К2С03 и Na2C03, а также - оптимальные условия кристаллизации иодидов натрия и калия могут быть установлены с помощью диаграмм растворимости в системах Nal—Na2C03—NaHC03—Н20, KI—К2СО3—KHC08—Н20, KI—КОН—К2С03—Н20 (рис. 77—79) Иодиды натрия и калия высаливают карбонаты из растворов и в двойных и тройных эвто - нических точках в пределах температур 0—25° содержание Nal в солевой массе растворов составляет 98,3—99,3 мол. %, a KI— 87,7—91,1 мол.%. Для получения чистых иодидов карбонаты должны быть предварительно удалены из растворов добавкой Fe3I8 или HI. В системе KI—КОН—Н2С03—Н20 наибольшим высаливающим эффектом обладает КОН. Применяемые для получения KI поташ и едкое кали всегда содержат соединения натрия (1—5%),
Которые накапливаются в производственных растворах и загрязняют готовый продукт. Пути разделения KI и Nal могут быть выявлены с помощью диаграммы растворимости в системе KI-Nal—Н20 (рис. 80)129'130.
Перспективным является изготовление иодидов 125- isi—134 взаи. модействием иодистоводородной кислоты (получаемой при извлечении иода из рапы десорбцией воздухом, стр. 249) со щелочами, карбонатами или хлоридами:
МОН + HI = MI + Н20 М2С03 + 2HI = 2MI + Н20 + С02 MCl + HI = MI-fHCl
|
По последней реакции можно производить и очистку иодидов
Рис. 80. Растворимость в системе KI—Nal—Н20 при 0, 25 и 50°. |
Соли раствором HI при нагревании. Количество HI должно соответствовать —1,5 эквивалентам от содержащихся в солях Вг" и CI".
В лабораторных условиях разработан метод прямого получения иодида натрия реактивной квалификации из иод-углей,35. После промывки иод-угля пресной водой из него извлекают иод раствором щелочи или сульфитно-содовым раствором. Полученный концентрат-выпаривают досуха и прокаливают при 350—450° для удаления органических веществ. Остающийся плав обрабатывают небольшим количеством воды и получают раствор, содержащий 64—65% Nal, 0,2—0,3% NaCl, 0—1% NaBr и 0,03—0,05% Na2S04.
В этом растворе может содержаться и 0,02—0,03% нафтеновых кислот, если не прокаливать остаток после сульфитно-содовой обработки. Далее удаляют из раствора SCU карбонатом бария и добавляют иодистоводородную кислоту (150% от эквивалента Вг~+ + С1"). Нагреванием до кипения (128°) отгоняют смесь кислот (НС1 + НВг + Н1 + Н20), после чего остается чистый иодид натрия.
Иодат калия получают по реакциям 136.
6КС1 + 3I2 + 10HN03 = 6КЮ3 + 6НС1 + lONO + 2Н20 KIO3 • HIO3 + КОН = 2КЮ3 + Н20
Иодат калия может быть также получен раскристаллизацией смеси KI + KIO3.