Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Криолит
Для получения криолита в плавиковой кислоте вначале растворяют гидроокись алюминия:
А1(ОН)3 + 6HF = H3A1F6 + ЗН20
Раствор фторалюминиевой кислоты H3A1F6 нейтрализуют содой: 2H3A1F6 + 3Na2C03 = 2Na3AlF6 + 3C02 + 3H20
Образующийся криолит выделяется в осадок.
Фторид натрия, содержащийся в виде примеси в плавиковой кислоте, также превращается в криолит:
3NaF + H3A1F6 = Na3AlF6 + 3HF
При избытке соды примесь Na2SiF6 переходит в NaF: Na2SiFe + 2Na2C03 = 6NaF + 2С02 + Si02
Для получения чистого криолита стандартного качества (стр. 1108) необходимо, чтобы плавиковая кислота содержала малые количества примесей — H2SiF6, Na2SiF6 и H2S04. Обычно «чистая» плавиковая кислота, идущая на приготовление криолита, содержит до 25% HF, 0,7—0,8% H2SiF6 и около 1,5% H2S04. Примеси в криолит попадают также из гидроокиси алюминия, который по техническим условиям не должен содержать более 0,3% Si02, 0,6% Na20 и 0,1% Fe203.
Получение криолита осуществляют 188 в стальных резервуарах, футерованных угольными плитками и снабженных мешалками. Процесс ведут непрерывно в 3—4 соединенных последовательно и расположенных каскадом резервуарах. Кислоту и пульпу гидроокиси алюминия вводят через дозаторы в первый резервуар, содовый раствор — в третий. Гидроокись алюминия дозируют из расчета связывания 55% HF плавиковой кислоты. Нейтрализацию фторалюминиевой кислоты в третьем резервуаре ведут так, чтобы в маточном растворе осталось 2—3 г/л свободной HF во избежание перевода примеси Na2SiF6 в NaF и Si02 и перехода в осадок примеси железа, которое при меньшей кислотности выделяется вместе с криолитом в виде Fe(OH)3. Отстоявшийся криолит отфильтровывают и промывают водой на барабанном вакуум-фильтре. Снимаемую с фильтра пасту криолита, содержащую 15—20% влаги, высушивают в стальной барабанной сушилке при 130—140°. На производство 1 т криолита расходуют: 0,69—0,71 т HF в виде плавиковой кислоты, 0,29—0,30 т А1203 и 0,8—0,9 т Na2C03.
Для получения криолита могут быть использованы промывные воды и другие отбросные жидкости, содержащие NaF. При обработке их горячим свежеприготовленным раствором А1(ОН)3 в плавиковой кислоте 99% фтора осаждается в виде криолита, содержащего 90—98% Na3AlF6189.
Криолит предложено получать также обработкой смеси А1(ОН)3 и Na2C03 газообразным HF при 300° в горизонтальном вращающемся барабане 19°.
При приливании раствора хлористого алюминия к раствору поваренной соли и плавиковой кислоты образуется криолит и выделяется соляная кислота:
А1С13 + 6HF + 3NaCl - Na3AlFe + 6НС1
Этот метод применяют при переработке алюминиевых шлаков («алюминиевой золки») растворением их в соляной кислоте. Выделившуюся соляную кислоту возвращают в процесс.
Изучено191 образование криолита при взаимодействии каолинита с плавиковой кислотой и с кислыми растворами NaF. Процесс идет согласно уравнению:
Al2Si20,(0H)4 + 24F- + 14Н30+ - 2AlFjj- + 2SiFjj" + 23Н20
В нейтральном растворе (рН ~5) вместо кремнефторида образуется гидроокись кремния:
Al2Si205(0H)4 + 12F" + 6Н30+ = 2A1F|" + 2S1(0H)4 + 7HsO
По-видимому, и в кислых растворах коллоидная гидроокись кремния является промежуточной фазой при образовании кремнефторида.
Исследована возможность получения криолита борфтористово - дородным методом 192. Сначала получают раствор HBF4 обработкой CaF2 серной и избытком борной кислоты при 95° в присутствии Na2S04 для снижения растворимости CaS04. Оптимальная концентрация Н3В03 110—120 г/л. К отделенному от сульфата кальция раствору HBF4 добавляют гидроокись алюминия и соду, отделяют осадок криолита, а маточный раствор с избытком Н3В03 возвращают в цикл. Вследствие накопления примесей в циклическом процессе при 8-кратном обороте маточного раствора извлечение фтора снижается до 64—73%. Потери Н3В03 составляют 2—4% от веса получаемого криолита.
Применение вместо порошкообразного гранулированного криолита при электролитическом получении алюминия снижает потери фтора в этом процессе. Гранулирование производят на тарельчатом грануляторе из снимаемой с фильтра криолитовой пасты, влажность которой должна быть ~19%. Оптимальная температура последующего обезвоживания гранул во вращающейся барабанной печи ~600°193.
Фторид алюминия
Для получения фторида алюминия плавиковую кислоту нейтрализуют гидроокисью алюминия:
А1(ОН)3 + 3HF = A1F3 + ЗН20
Находящиеся в растворе примеси NaF и Na2SiF6 переходят в результате реакций
3NaF + AIF3 = Na3AlFe 3Na2SiFe + 4A1F3 = 2Na3AlFe + Al2(SiFe)3
В криолит, который выделяется в осадок вместе с A1F3. Так как образующийся по последней реакции Al2(SiFe)3 хорошо растворим, то он также взаимодействует с плавиковой кислотой и превращается в плохорастворимый A1F$:
AI2(SiFe)3 + 6HF = 2AIF3 + 3H2SiFe
В результате этих реакций содержащиеся в плавиковой кислоте соли натрия переходят в криолит, а взамен Na2SiF6 в растворе появляется эквивалентное количество H2SiF6.
Растворение гидроокиси алюминия производят в предварительно нагретой до 90—95 плавиковой кислоте. Массу перемешивают при этой температуре в реакторе с мешалкой в течение часа. Вследствие склонности фторида алюминия образовывать пересыщенные растворы кристаллизацию ведут также из горячих растворов при 90°, когда степень пересыщения минимальная. Продолжительность кристаллизации около 2,5 ч. Фторид алюминия выделяется в виде AIF3 • ЗН20. Так как растворимость его больше, чем криолита, то он кристаллизуется относительно медленнее, и кристаллы получаются крупнее. Для получения более крупных, быстрее осаждающихся кристаллов реакционную смесь нагревают и вводят в нее затравку—небольшое количество кристаллов (суспензии), полученных в предыдущей операции. Иногда затравку получают так: в реакционную смесь вводят струю холодной воды (небольшое количество); резкое охлаждение части раствора вызывает выделение некоторого количества мелких кристаллов, которые и служат затравкой.
Так как часть воды из реакционной смеси связывается при кристаллизации A1F3 • ЗН20, то пульпа значительно загустевает и осаж
дение кристаллов происходит медленно. Для ускорения процесса применяют плавиковую кислоту, содержащую не больше 9—10% HF. После некоторого охлаждения пульпы отстоявшиеся кристаллы отделяют от маточного раствора на фильтре, промывают и высушивают. На получение 1 т фторида алюминия расходуют: 0,8— 0,83 т HF в виде плавиковой кислоты и 0,71—0,72 т А1203.
Поступающая на сушку паста фторида алюминия содержит 25— 30% A1F3, 30—35% кристаллизационной воды и 35—40% маточного раствора. Свободная влага из маточного раствора при сушке удаляется в первую очередь. При нагревании до 300° A1F3 • ЗН2р теряет большую часть кристаллизационной воды и превращается в A1F3 • 0,5Н20. Дальнейшее удаление кристаллизационной воды происходит очень медленно при 350—400°. Однако при этом невозможно полностью удалить воду, и окончательное обезвоживание ведется при 500—550°. При этой температуре под действием имеющегося в прокалочной печи (сушилке) водяного пара происходит частичное разложение продукта и загрязнение его А1203 194,195:
2( A1F3 • 0,5Н20) + 2НаО = Al203 + 6HF
Предложено вести сушку в псевдоожиженном слое в две стадии — сначала
Сушка при 200—300°, когда разложение еще не велико, а затем, когда скорости гидролиза замедлена благодаря малому содержанию влаги, кратковременное досушивание при 600°. Таким путем можно получить продукт с влажностью меньше 1 % и содержанием фтора больше 66%, при потере фтора на обеих стадиях сушки 1,5—2% 196.
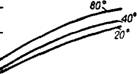
В маточном растворе после кристаллизации остается значительное количество фторида алюминия. Растворимость его в воде и слабокислых растворах невелика (рис. 328), но вследствие склонности к образованию пересыщенных растворов содержание A1F3 в маточном растворе составляет 50—60 г/л. Кроме того, в растворе остается до 15—30 г/л HF и немного других примесей — соединений железа, кремнезема, сульфатов. Маточный раствор используют для получения из содержащегося в нем A1F3 криолита путем внесения в него кристаллического NaF.
|
|
|
Л & < 1 |
|
12 3 4 Концентрация Hf 6 растворе, % |
|
Рис. 328. Растворимость фторида алюминии в слабых растворах HF. |
Предложено получать AlF3 из криолита или хиолита обработкой их при 200° (под давлением) смесью растворов алюминиевой соли (например, А1С13) и минеральной кислоты ш. Запатентованы способы получения фторида алюминия из железисто-глиноземной руды (боксита) обработкой ее стехиометрическим количеством плавиковой или кремнефтористоводородной кислоты или их смеси при
35—90°198. Описано получение A1F3 взаимодействием А1(ОН)3 с подогретым выше 70° газообразным фтористым водородом во взвешенном слое, разделенном на три зоны; реакция протекает в средней зоне при 400—650°199.
Запатентован способ получения фторида алюминия нагреванием в течение 2 ч при 80° смеси безводного А1С18 и NaF в среде ССЦ. Затем отделяют непрореагировавший ССЦ, твердый продукт промывают метанолом, потом водой и высушивают при 200° 20°.