Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
КАРБОНАТ БАРИЯ Карбонизация раствора сернистого бария
|
2.NH4NO3 |
|
2NHaC1 |
|
■13995 Ёа(Ы03)2 |
|
7439 5/35 2438 ВаС1г |
|
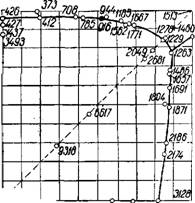
Рис. 140. Растворимость в водной системе BaCl2 + 2NH4N08-=Ba(N03)2 + + 2МН4С1 при 25°. (Цифрами отмечены моль Н20 на 100 моль солей.) |
Наиболее распространенный способ получения технического Углекислого бария основан на карбонизации раствора сернистого б%рия (160—170 г/л BaS) При 30—40° двуокисью углерода,
содержащейся в газах, отходящих из известково-обжигательных печей, из печей в производстве сернистого бария и др. В применяемых для этой цели печных газах не должно содержаться заметных количеств кислорода во избежание окисления сернистого бария, а содержание С02 желательно не ниже 20%.
Ввиду того, что сернистый барий в растворе гидролизован
2BaS + 2Н20 = Ва(ОН)2 + Ba(HS)2
При карбонизации идут две последовательные реакции. Вначале карбонизуется Ва(ОН)2:
Ва(ОН)2 + С02 = ВаС03 + Н20
При дальнейшей карбонизации выделяется сероводород по реакции:
Ba(HS)2 + С02 + Н20 = ВаСОз + 2H2S
Таким образом, процесс идет по суммарному уравнению: BaS + С02 + Н20 = ВаСОз + H,S
Печной газ проходит последовательно через 3—4 цилиндрических резервуара с коническим днищем, где барботирует через предварительно отстоявшийся от шлама раствор сернистого бария. Это обеспечивает хорошее использование содержащейся в газе двуокиси углерода. Вместе с С02 газ приносит в последующий карбонизатор H2S, Выделившийся в предыдущем по ходу газа аппарате. H2S Поглошается сульфидом бария с образованием гидросульфида:
BaS + H2S = Ba(HS)2
В дальнейшем гидросульфид бария карбонизуется. По окончании реакции в первом по ходу газа аппарате его отключают и дают отстояться образовавшемуся осадку ВаС03. Затем жидкость сливают и направляют на выщелачивание плава сернистого бария, а осадок промывают несколько раз горячей водой, отжимают на фильтрах (а иногда под прессом) и сушат.
Получаемый таким путем углекислый барий всегда, даже при хорошей промывке, содержит небольшое количество сульфидов и серы. С целью получения продукта, не содержащего серы, осажденный ВаСОз смешивают с водой, добавляют небольшие количества щелочей (NaOH, NH4OH, Na2C03, NaHC03 И т. п.) и нагревают до кипения. При этом образуются сульфиды, легко отмываемые от осадка горячей водой. Более полная очистка осадка ВаСОз от сульфидной серы достигается при нагревании его в слабых растворах щелочей до 140—150° в автоклавах. Общее содержание серы становится при этом ниже 0,2% в пересчете на BaSOi.
Осаждение ВаСОз из растворов BaS Производят также содой по реакции:
Ва(ОН)2 + Ba(HS)2 + 2Na2C03 = 2ВаС03 + 2Na2S + 2Н20
Для получения более чистого осадка следует к 15—16% раствору соды, нагретому до 70—80°, медленно приливать 11—15% раствор BaS, Не допуская полного израсходования соды (избыток Соды должен равняться 1—2%). Полученный осадок ВаС03 легко отстаивается и промывается.
Получение ВаС03 из нитратного щелока
Для производства ВаС03 используют, например, раствор, содержащий 140—160 г/л Ba(N03)2— осветленный нитратный щелок из производства азотнокислого бария. К щелоку, после контрольной фильтрации на вакуум-фильтре, добавляют раствор NaOH С концентрацией 500 г/л до свободной щелочности 1—2 г/л (в пересчете на NaOH). Подщелачивание ведут при 60—70° в резервуаре с змеевиками для подогрева паром и барботером для перемешивания раствора воздухом. Затем нитратный раствор обезвреживают (удаляют из него сернистые соединения), медленно добавляя раствор гипохлорита натрия (120 г/л активного хлора) до появления свободного активного хлора, определяемого пробой на иодо-, крахмальную бумажку. При этом идут следующие реакции;
BaS + 4МаС10 = BaS04 + 4МаС1 S + 3NaC10 + Н20 = H2S04 + 3NaCl H2S04 + Ва(М03)2 = BaS04 + 2НМ03
После отстаивания раствора от BaS04 И других примесей его приливают к перемешиваемому, подогретому до 80—90° раствору соды (200 г/л Na2C03). Конец реакции
Ba(N03)2 + Ма2СОэ = ВаСОэ + 2МаМ03
Устанавливают по щелочности реакционной смеси — около 0,5 г/л (в пересчете на ОН-). По окончании осаждения карбоната бария продолжают перемешивание при 85—90° в течение 10—15 мин, Затем дают осадку ВаС03 отстояться в течение 20—30 мин. Рас* твор NaN03 Декантируют и отправляют на выпаривание, а осадок промывают на вакуум-фильтре горячей водой (80—90°) от нитрата натрия и ионов хлора. Затем осадок разваривают при 80—90°, отфильтровывают, окончательно промывают, сушат и укупоривают. На 1 т продукта (в пересчете на 100% ВаС03) расходуют: 0,59— 0,6г кальцинированной соды (95% Na2C03), 2,4 г барита (100%), 0,675—0,71 г азотной кислоты (100%), 0,22—0,25 т едкого натра (Э2%), 0,02—0,025 г гипохлорита натрия (100% активного хлора).
Другие способы получения ВаС03
При небольших масштабах производства для осаждения углекислого бария используют производственные растворы хлористого бария, обрабатывая их содой:
ВаС12 + Ма2С03 = ВаС03 + 2NaCl
Обычно раствор содержит 180—200 г/л ВаС12. Его предвари-: тельно очищают от ионов кальция и железа обработкой раствором NaOH Или промывными водами, получаемыми при производстве гидроокиси бария, содержащими 30—40 г/л Ва(ОН)2. Для осаждения берут раствор соды, содержащий 180—200 г/л Na2C03. Процесс ведут так же, как и при осаждении ВаС03 из Ba(N03)2. Промывку осадка на фильтре горячей водой ведут до содержания - в нем С1" не больше 0,05%. На 1 г 100%-ного углекислого бария расходуется 1,276—1,29 г ВаС12 • 2Н20 (100%), 0,553—0,575 т кальцинированной соды (95%), 0,011т едкого натра (92%), 100— 120 квт-ч электроэнергии, ~3 мгкал пара, ~100м3 воды.
Существуют и другие способы получения ВаС03, например осаждение его из растворов BaS Или ВаС12 углекислым аммонием или разваривание BaS04 В концентрированном растворе углекислого калия под давлением 5 ат.
При перемешивании 12—15 мин суспензии BaS04 В 20% растворе Na2C03 (с небольшой добавкой NaOH) В автоклаве при 8— 10 ат и 200° выход ВаС03 достигает 90%103.
Возможно получение ВаС03 взаимодействием BaS04 И №2СОз в среде расплавленного NaCl104. '