Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ДЕГИДРАТИРОВАННЫЕ ФОСФАТЫ НАТРИЯ
При дегидратации ортофосфатов натрия образуются различные конденсированные фосфаты 2>66-78 со структурой аналогичной силикатам, так как координационное число как кремния, так и фосфора по отношению к кислороду всегда равно четырем. Один из четырех атомов кислорода связан с пятивалентным атомом фосфора двойной связью и поэтому не может быть связующим звеном между двумя атомами фосфора. В зависимости от строения конденсированные фосфаты относят к метафосфатам или полифосфатам.
Метафосфаты имеют общую формулу М„[РОз]„, например, при п, равном 3 или 4, три - или тетраметафосфаты. Структура ме - тафосфатов характеризуется образованием кольцеобразных анионов79, например, для триметафосфата Na3[P3Og]:
4p/0Na
С/ Хо NaO |
Р Р О^ Q/�Na
У солей с кольцеобразными анионами отношение заряда катионов к количеству атомов фосфора строго равно 1:1.
Известен двойной метафосфат натрия и кальция Na4CaP60ia с предполагаемым строением80:
°wONa °wONa
/ / О О 0 0
Na04| |у) О | |у>
NP Р—О—Са—О— Р Р^
,/)Na
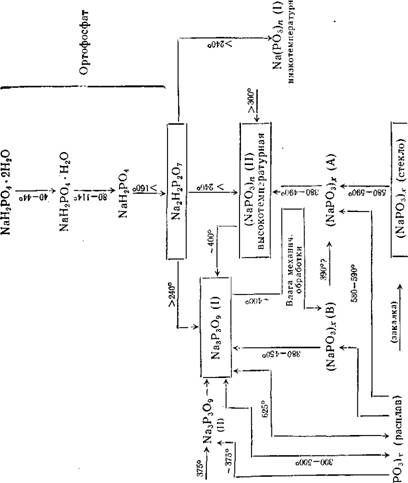
На рис. 310 схематически показаны условия образования различных продуктов и их превращений68 при нагревании на воздухе дигидрата однозамещенного фосфата натрия. Выше 160° образуется пирофосфат, который при температуре выше 240° переходит в стабильную форму триметафосфата Na3P309 и частично в соль Маддреля [низкотемпературную (NaP03)n(I) и высокотемпературную (NaP03)n(II) формы]. Соль Маддреля формы (NaP03)„(II) при температуре около 400° переходит необратимо в триметафосфат Na3P309(I). Последний при 625° образует расплав (ЫаР03)ж. При медленном охлаждении расплава получается триметафосфат как стабильной Ыа3РзОэ(1), так и нестабильных форм Na3P309(II) и Na3P309(III). При быстром охлаждении расплава метафосфата образуется стекловидная соль Грэма. Последняя ниже 600° переходит в стабильный триметафосфат, а в присутствии затравки в натриевую соль Курроля (NaP03)x(A). Под действием влаги или механической обработки из формы А соли Курроля образуется форма В, которая при 380—450° переходит в триметафосфат. Обе эти формы могут быть получены также из расплава метафосфата. Форма А соли Курроля при охлаждении переходит в (ЫаРОз)„(П).
Полифосфаты имеют общую формулу Mn+2P„03n+i или МпН2РпОзп+1, где п может быть равно от 1 до ~108. Полифосфаты характеризуются тем, что их анионы состоят из неразветвлен - ных цепей, представляющих собой (Р04) — тетраэдры, связанные
|
К Ч си К Is £ J5 Ч о S G § Й Oi О |
|
К ч о о. о. X А Ч О |
|
Са О в 2 4 S К о. Е - |
|
X Еч |
|
О ■в - О о. к С |
|
О а |
|
|
|
О |
|
Са о. |
|
S В |
|
О со |
|
О - е - 03 А, _ |
|
„FiSS-Wffi |
|
X Ч |
|
К 5 S А м Са к Я в <и а А. ч S К С в. К с » 3 А а СО О) X] <d О. я с g S3 Н Я Ч О о Е - о. в С[ <и Й 3 О, щ С я Й § щ о СГ w |
|
Я О. |
|
И ~ 2 в |
Друг с другом атомами кислорада. Пример триполифосфата с не- разветвленной цепью — Na5[P3Oi0]:
II II II
NaO—Р—О—Р—О—Р—ONa
I I
ONa ONa ONa
Отношение заряда катионов к количеству атомов фосфора приближается к 1 : 1 с возрастанием длины цепи.
Широко известный стекловидный фосфат, неправильно называемый гексаметафосфатом (соль Грзма), вследствие цепного строения относится к типу полифосфатов (а не метафосфатов, как считали ранее).
Конденсированные фосфаты, имеющие разветвленную цепь, содержат один или несколько агомов фосфора, которые связаны через атомы кислорода с тремя другими атомами фосфора, например:
II II II
МО—Р—О—Р—О— Р—ом
I I
I I
МО—Р—О—Р—О—Р—ОМ
II II II
ООО
Вследствие своей разветвленной структуры они получили название ячеистых фосфатов (изомета - и изополифосфаты). К ним относится и летучая модификация фосфорного ангидрида [Р40ю]п, где п может иметь значение от 1 до весьма большого числа. Изомета - и изополифосфаты имеют такой же состав, что и мета - и полифосфаты. Эти фосфаты при обычной температуре быстро гидролизуют - ся в нейтральном щелочном растворе с образованием нормальных полифосфатов. Гидролиз происходит в местах разветвления цепей, где все три связующие атома кислорода соединены с атомами фосфора ковалентной связью.
Среди метафосфатов наиболее известен триметафосфат натрия Na3[P309], Метафосфаты являются солями очень сильных кислот (их водные растворы имеют нейтральную реакцию). В воде хорошо растворимы только щелочные соли. Безводный триметафосфат натрия устойчив при нагревании почти до точки плавления. Остальные метафосфаты при высоких температурах переходят в смеси полифосфатов путем гидролитического расщепления кольцеобразных анионов. В нейтральном водном растворе метафосфаты устойчивы при комнатной температуре, а в кислой среде при температуре выше ~60° они быстро гидролизуются через промежуточные ступени до ортофосфата. В щелочных растворах они разлагаются до смеси полифосфатов (три - и тетрафосфатов).
Полифосфаты и относящаяся к этой группе не растворимая в воде соль Маддреля [NaP03]n • Н20 являются солями кислот, образующих ряд, представленный в табл. 83 67. Цепи полифосфорных кислот имеют у каждого атома фосфора сильнокислую группу ОН и, кроме того, на концах цепи по две слабокислых ОН-группы. Соответственно этому растворы полифосфатов, полученных из первичных ортофосфатов, дают слабокислую реакцию, а растворы их «нейтральных солей» — слабощелочную реакцию. Слабокислые, нейтральные и щелочные растворы полифосфатов при обычной температуре являются стойкими; выше 60°, особенно в кислой среде, они гидролиз уются.
Таблица 83
|
Полифосфорные кислоты Нп+2Рп03п+1
|
Наиболее важным свойством полифосфатов натрия, на котором основано их широкое практическое применение, является способность связывать кальций и магний, умягчая тем самым воду81-87. Эта способность полифосфатов объясняется тем, что они обладают свойствами ионообменников88. Триполифосфат Na5P8Oi0 с солями жесткости образует соль Ca2NaP3Oi0, выделяющуюся в осадок при достаточной концентрации ионов Са2+ в растворе. Он способен связать 10—11% кальция или 6,4% магния (от своего веса). Стеклообразные фосфаты могут связывать 12—18% кальция или 2,9— 3,8% магния.
Другим свойством дегидратированных фосфатов (особенно три - полифосфата) является способность пептизировать суспензии и снижать их вязкость, вследствие чего они используются при флотации руд89. Добавка во флотационную пульпу ~1 кг/т гексамета - фосфата натрия увеличивает содержание ценного компонента в концентрате при перечистке примерно в 2 раза90. В присутствии полифосфатов натрия органические поверхностно-активные вещества значительно улучшают свою моющую способность. В связи с указанными выше свойствами триполифосфат и стекловидный фосфат сейчас широко применяют для устранения солей жесткости из воды, идущей для питания силовых установок, и во всех других случаях, когда необходимо предотвратить выделение осадков. Стекловидные фосфаты используют непосредственно при стирке белья и поверхностной чистке одежды. Триполифосфат успешно применяют как составную часть (до 85%) большинства моющих смесей. Тетранатрийфосфат добавляют к обычному мылу. Дегидратированные фосфаты применяют как средство торможения коррозии металла 91'92, для удаления жира и масла из хлопка, шерсти и шелка, как катализаторы ё процессах дегидрирования, алкилирования и полимеризации углеводородов, как нефтеочистные агенты, для регулирования вязкости бурового шлама, в процессах флотации, как активные диспергаторы красок и минеральных суспензий (каолинов, известняка и др.), как эмульгаторы в производстве сыров, в гальванопластике и при электролизе, в производстве синтетического каучука, в кожевенной промышленности, при отбелке соломы, для стабилизации растворов пергидроля, для улучшения фильтруе - мости вискозных растворов, для промотирования роста кристаллов93 и др. Пирофосфат натрия используют как реагент при обогащении природных серных руд. Кислый пирофосфат натрия применяют преимущественно в качестве составной части хлебопекарных порошков. Тринатрийпирофосфат Na3HP207 вследствие нейтральной реакции (рН = 7) наиболее приемлем в производстве колбас и других мясных изделий.
Триполифосфат натрия должен отвечать требованиям, представленным в табл. 84.
|
ТАБЛИЦА 84 Требования к качеству триполифосфата натрия
|
Производство триполифосфата натрия и других дегидратированных фосфатов
Для производства триполифосфата натрия используют как термическую кислоту, так и экстракционную кислоту при условии ее очистки86. Фосфорную кислоту нейтрализуют содой до получения раствора с отношением 5Na20 : 3P20s: ЗН3Р04 + 2,5Na2C03 + гсН20 = 2Na2HP04 + NaH2P04 + (N + 2,5)HsO + 2,5С02
Раствор выпаривают, и смесь сухих солей подвергают дегидратации при 340—-400°. Это обеспечивает получение низкотемпературной модификации Na5P3Ojo, устойчивой ниже 450°, которая в отличие от высокотемпературной модификации, устойчивой выше 450°, не слеживается во влажной среде и не комкуется при растворении в воде94. Для стабилизации низкотемпературной формы триполифосфата предложено95 применять добавки небольших количеств (до 1%) карбамида, азотной кислоты, нитрата аммония и др. Эти добавки способствуют также более полному превращению орто - фосфатов в триполифосфат и придают белизну продукту.
Указывают96, что добавка к исподным веществам 1—2% NH4NO3 действует каталитически на образование Na5P3Oio, протекающее при более низкой температуре. В результате этого получается низкотемпературная модификация Na5P3Oio, отличающаяся хорошей растворимостью97.
Ортофосфаты NaH2P04 и Na2HP04 при прокаливании предварительно превращаются в пиро - и метафосфаты98. Например, 2Na2HP04 + NaH2P04 = Na4P207 + NaP03 + 2НаО
Образование промежуточных соединений протекает с максимальной скоростью при 185—220°. Триполифосфат натрия частично образуется при быстрой первичной дегидратации ортофосфатов до 230°. Основная же его масса получается по реакции между пиро - и метафосфатами:
Na4P207 + NaPOs = Na5P3O10
Она протекает с максимальной скоростью при 290—310° и идет с достаточной полнотой только при условии очень тесного контакта между частицами.
Дегидратация ортофосфатов с образованием триполифосфата завершается в течение 15—30 мин.
Выпаривание раствора ортофосфатов натрия с получением сухих солей (сушку) и дегидратацию (прокаливание) их осуществляют как раздельно, так и в одном совмещенном аппарате. Последний способ получил значительное распространение. Для раздельной сушки предварительно упаренного в трехкорпусном выпарном аппарате раствора применяют99 полые вращающиеся вальцы, обогреваемые паром давлением до 5—8 ат, или распылительные башни. Дегидратацию сухих фосфатов осуществляют во вращающихся барабанных печах. Последние могут быть использованы для совмещенной сушки исходного раствора и кальцинации ортофосфатов. В этом случае во избежание налипания материала на стенки барабана упаренный раствор, содержащий ~32% Рг05, смешивают с ретуром готового продукта86-10°-101 (в соотношении по весу 3 ч - 3,5 : 1 при влажности смеси 10—12%) или распыливают раствор на слой сухого материала 102.
Предложено 103 получать триполифосфат во вращающемся барабане, разделенном кольцевой перегородкой на две зоны: в первой раствор, вводимый в барабан посредством распыливающих форсунок, высушивается, а во второй протекают дальнейшие процессы. Барабан обогревается изнутри с помощью газовых или нефтяных горелок.
Более совершенными являются распылительные сушилки 104-107. При производительности завода 7500 г триполифосфата в год распылительная сушилка 108 представляет собой цилиндрическую башню диаметром 6,6 м и высотой 17 м. Раствор ортофосфатов подается под давлением и разбрызгивается в потоке горячих газов, поступающих в верхнюю часть башни с температурой 400—700° и уходящих с температурой 100—200°. Из сушилки продукт с влажностью менее 5% поступает для прокаливания во вращающуюся печь или в неподвижную печь, снабженную горизонтальными лопастными мешалками," служащими для передвижения материала. Прокаливание сухих ортофосфатов может быть также осуществлено & распылительной сушилке совместно с сушкой раствора. Перспективным представляется проведение сушки и дегидратации ортофосфатов в печи со взвешенным слоем 2> 109. Но это связано с трудностями регулирования гранулирования продукта, так как вследствие агломерации первоначальных частиц в крупные агрегаты происходит нарушение и затухание взвешивания слоя ио.
В СССР триполифосфат производят двумя способами: 1) в совмещенном процессе с применением сушильно-прокалочной распылительной печи и 2) с раздельной сушкой раствора в распылительной сушилке и прокаливанием сухих ортофосфатов в кальци - наторе специальной конструкции — турбокальцинаторе.
При совмещенном процессе111'112 сушка раствора, прокаливание сухих ортофосфатов и охлаждение продукта происходят в одном аппарате — сушильно-прокалочной печи.
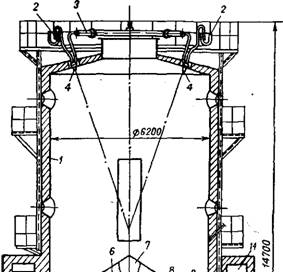
Сушильно-прокалочная печь (рис. 311) представляет собой цилиндрическую башню, футерованную изнутри огнеупорным кирпичом. В нижней части печь имеет две прокалочные и две холодильных тарелки; верхняя прокалочная тарелка изготовляется из чугуна или жаропрочной стали, а нижняя — из обычной стали, футерованной шамотным кирпичом, а холодильные — из обычной
Стали. Распыление раствора осуществляется пневматическими форсунками под давлением 5—7 ат. Горячие газы, полученные сжиганием газа или мазута с температурой 800—900°, поступают
|
|
|
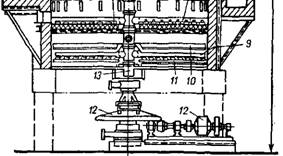
Рис. 311. Совмещенная сушильно-прокалочная печь: 1 — башня; 2 — желоб; 3 — коллектор для пара; 4 — форсунка; 5 и б — прокалочные полкн; 7 —конус; 8 —шлицы: 9 — скребки; 10 и 11 — полки охлаждения; 12 — приводной механизм; 13 — вал; 14 — боров. |
В нижнюю часть печи из кольцевого борова через шлицы. Основная масса газа выходит в полость между прокалочными полками, а часть газа поступает в зону над верхней тарелкой.
Сухой и частично прокаленный материал, оседающий на верхней тарелке, перемещается скребками к центру и ссыпается - на вторую прокалочную полку. Скребки и вал выполняются полыми;
Для их охлаждения через них продувают воздух. Со второй прока - лочной полки материал с температурой ~400° поступает на холодильные тарелки, по которым пропускают охлаждающую воду. На выходе из башни продукт имеет температуру 30—40 . Топочные газы выводятся с температурой 140—200°.
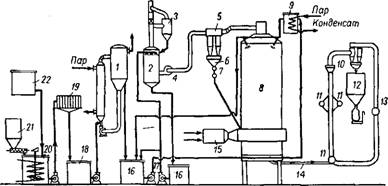
На рис. 312 показана схема производства триполифосфата натрия в совмещенном процессе с применением распылительной су - шильно-прокалочной печи. Исходный раствор перед сушкой упаривают в выпарном аппарате с принудительной циркуляцией. Упаренный до 60% - ной концентрации (~30—32% Рг05) раствор
|
Рис. 312. Схема производства триполифосфата натрия с применением совмещенной сушильно-прокалочной печи: / — выпарной аппарат; 2 — скруббер; 3 — брызгоуловитель; 4 — дымосос; 5 — циклон; 6 н /2 —бункеры; 7 —мнгалка; 8 — сушнльно-прокалочная печь; 9 — напорный бак; 10 — классификатор; ))—дробилка; 13 — вентилятор; 14 — шнек; 15 — топка; 16 — сборник; 17 — насос; 18 — сборник раствора; 19 — фильтр; 20 — реактор; 21 — бункер для соды; 22 — бак для фосфорной кислоты. |
Насосом подают через напорный бак в распределительный желоб печи, где происходит выпаривание и сушка раствора, дегидратация ортофосфатов и охлаждение триполифосфата. Отработанные газы вместе с пылью направляются в батарейный циклон для очистки от пыли. Уловленная пыль собирается в бункере, откуда она через две мигалки возвращается на первую прокалочную полку печи. Выходящие из циклона газы дополнительно очищаются от пыли в скруббере, орошаемом разбавленным раствором и, пройдя циклонный брызгоуловитель, выбрасываются в атмосферу.
Полученный в печи готовый продукт после грубого дробления пневмотранспортом подается в сепаратор, откуда крупные частицы поступают на дополнительное измельчение в мельницы тонкого помола. Мелкий порошковидный материал улавливается в циклонах и подается в бункер готового продукта.
Ю М. Е. Поз ни
Недостатками совмещенного процесса являются частое забивание тракта пылеочистки и трудности регулирования температурного и технологического режимов сушки и прокалки продукта. При резком повышении температуры в прокалочной зоне качество продукта снижается. В сушильно-прокалочных печах с комбинированным вводом (верхним и нижним) горячего газа 112-114 процесс сушки протекает более интенсивно. Однако полностью недостатки, присущие совмещенному осуществлению процесса, не устраняются.
Продукт более высокого качества образуется при раздельном получении смеси сухих солей и последующем их прокаливании в специально предназначенных для этого аппаратах. По этой схеме115 для сушки раствора применяется распылительная сушилка, обеспечивающая получение тонкодисперсного порошка, который легко и быстро дегидратируется.
Прокаливание тонкодисперсной смеси солей эквимолекулярного состава производится в турбокальцинаторе, представляющем собой цилиндрическую стационарную камеру, в которую вмонтировано большое количество вращающихся тарелок и турбин для интенсивного перемешивания горячих газов и обрабатываемого твердого материала. Этим достигается хороший контакт между продуктом и греющим газом и исключаются местные перегревы, ухудшающие качество продукта.
Помимо условий дегидратации качество продукта зависит от режима нейтрализации кислоты и ее состава. При отношении молярных концентраций в нейтрализованном растворе Na20 и P2Os меньше или больше 1,67 качество продукта снижается. Для точного поддержания этого отношения предпочитают вести нейтрализацию периодически или полунепрерывно; этим достигается более тонкая дозировка реагентов и корректировка состава конечного раствора. На заводе в РНР116 процесс осуществляется непрерывным путем. Нейтрализацию кислоты содой ведут в три стадии (в трех реакторах). В первом реакторе получают мононатрийфос - фат, во втором — динатрийфосфат и, наконец, в третьем реакторе раствор динатрийфосфата обрабатывают автоматически дозируемым количеством фосфорной кислоты до образования эквимолекулярной смеси NaH2P04 и 2Na2HP04.
Триполифосфат натрия (как и другие дегидратированные фосфаты), получаемый из экстракционной фосфорной кислоты, хуже по качеству, чем триполифосфат, полученный из термической кислоты. Это объясняется тем, что содержащиеся в экстракционной кислоте примеси не только разбавляют конечный продукт, но и действуют как каталитические пассиваторы на процесс дегидратации.
При использовании экстракционной фосфорной кислоты процесс осуществляют следующим образом 117. Кислоту, содержащую (в %): ~20 Р205) 0,4—0,6 S03 и 1,5—1,8 фтора, нейтрализуют содой до рН = 7. Выделяющийся шлам, состоящий в основном из фосфатов полуторных металлов и кремнефторида натрия, отделяют, а раствор упаривают в распылительной сушилке. При этом содержащиеся в растворе моно - и дифосфат натрия (в молярном отношении 2:1) дегидратируются при 400° за счет тепла отходящих газов. Продукт содержит: 54,3—55% Р205 (из них 53,2—54,3% в полиформе и 0,4—0,9% в ортоформе), 2,8—3,5% Na2S04 и 1—1,5% NaF.
В другом случае 118 используют экстракционную кислоту большей концентрации (~30% P2Os) и содержащую большее количество сульфатов (1,8—2,0% S03); ее предварительно очищают от SOt. Кислоту состава: 30,2%Р205, 1,8% S03, 0,2% СаО, 0,7% фтора, 0,4% хлора, 0,3% А1203> 0,3% MgO и 0,3% Fe203 обрабатывают вначале известняком, а затем концентрированным раствором соды. После отделения гипса и кремнефторида натрия к раствору добавляют ВаС03 и нейтрализуют его содой с последующей переработкой в конечный продукт.
Полученный в процессе очистки экстракционной фосфорной кислоты шлам, состоящий в основном из фосфатов железа и алюминия, используют в производстве гранулированного суперфосфата117. Комплексное удобрение предложено119 получать при смешении шлама с нитратом аммония и калийной солью.
Для получения из экстракционной кислоты триполифосфата такого же качества как из термической, необходима тонкая очистка ее от примесей. Особенно вредной примесью являются соединения фтора. Содержание основного вещества в продукте — триполи - фосфате натрия — обратно пропорционально содержанию фтора в кислоте.
Предварительное обесфторивание кислоты осаждением из нее кремнефторида натрия 120 соответствующим количеством соды приводит к осложнению последующих стадий процесса. Кислоту после отделения кремнефторида натрия подвергают дальнейшей нейтрализации содой до образования моно - и диортофосфатов натрия. Выделяющиеся при этом фосфаты полуторных окислов значительно хуже фильтруются, чем при одновременном соосаждении кремнефторида натрия. Кроме того, остаточное содержание фтора в кислоте достаточно велико в соответствии с растворимостью в ней кремнефторида натрия (например, ~0,5% Na2SiF6 в кислоте концентрации 22—24% Р2Об). В присутствии солей алюминия и железа содержание фтора в конечном нейтрализованном растворе увеличивается вследствие образования фторалюминатов и криолитов. Помимо этого при повышенной температуре кремнефторид натрия реагирует с содой:
Na2SiF6 + 4Na2C03 + 2Н20 = 6NaF + Si02 + 4NaHCO,
Образующийся фторид натрия обладает значительно большей растворимостью, чем кремнефторид.
Установлено121, что наименьшая растворимость фтористых соединений (0,04—0,05% фтора) наблюдается при нейтрализации содой экстракционной фосфорной кислоты до рН = 4,5—5,0. При исходной концентрации в кислоте 17—24% Р205 это соответствует полной нейтрализации первого и 20—30% второго ионов водорода Н3РО4. Одновременно происходит полное выделение в твердую фазу соединений полуторных окислов. Осуществляя нейтрализацию экстракционной фосфорной кислоты в две стадии с промежуточным отделением примесей, возможно получить - триполифосфат высокого качества.
Для очистки раствора от сульфат-иона обычно применяют карбонат бария.
Пищевые продукты можно получить из экстракционной кислоты, очищенной с помощью алифатических растворителей и активированного угля 122. Получаемая этим способом пищевая фосфорная кислота дешевле термической.
Указывают116, что при тщательной очистке фосфорной кислоты в условиях трехстадийной непрерывной нейтрализации экстракционной фосфорной кислоты с двухкратным отделением осадков (после нейтрализации и затем после упарки раствора) получаемый триполифосфат содержит: 91—93% Na5P3Oi0, 55—56,8% Р205, 3—4% Na2S04, 0,005% Fe и 0,003% As. Плотность его равна 0,5—0,75 г/см3, а рН 1%-ного раствора триполифосфата составляет 9,5—9,6.
Пищевой гексагидрат триполифосфата натрия 86-123 получают из технического продукта, растворяя его при 60—70° в воде. Полученный при этом 17—20%-ный раствор Na5P3Oi0 отделяют от нерастворимых примесей. Вакуум-кристаллизацией при 60° (с целью предотвращения гидролиза) выделяют из раствора кристаллы чистого Na5P3Oi0 • 6Н20, которые отфуговывают от маточной жидкости и высушивают.
Во избежание перехода триполифосфата в пиро - или ортофор - мы предложено 124 сушку гексагидрата Ыа5Р30ю • 6Н20 производить горячими газами, содержащими водяной пар при парциальном давлении последнего около 200 мм рт. ст. и относительной влажности менее 40%. Этого же можно достичь 125 путем перегрева гексагидрата при повышенном давлении с последующим высушиванием его при атмосферном давлении в распылительном аппарате или сушкой водяным паром 126, перегретым до 250—450°.
Стекловидный фосфат натрия (соль Грэма) получают нагреванием и расплавлением при 620—700° мононатрийфосфата с последующим очень быстрым охлаждением плава 127> 128. Для получения продукта в виде тонких чешуек расплав выливают между вращающимися охлаждаемыми вальцами. Продукт содержит ~69,6%
Р2О5. Его раствор имеет рН около 5,2. Свойства продукта (содержание основного вещества, устойчивость и степень полимеризации) зависят от температуры плавления и скорости кристаллизации плава. В периодических условиях не обеспечивается постоянство режимных параметров как при нейтрализации кислоты содой с получением мононатрийфосфата, так и при полимеризации и кристаллизации плава.
Представляет интерес разработанная в Ленниигипрохиме 129 непрерывная схема получения стекловидного фосфата. Нейтрали-, зацию фосфорной кислоты содой осуществляют непрерывным путем при автоматическом регулировании рН среды, температуры,, времени пребывания раствора в реакторе, сигнализации уровня в расходных емкостях. Плавление мононатрийфосфата и полимеризация осуществляется в отражательной печи непрерывного действия. Получаемый продукт отличается повышенной растворимостью и активностью.
Разработан (А. А. Соколовский) способ получения стекловидного фосфата натрия из суперфосфата через раствор мононатрийфосфата, получаемый обменным разложением монокальцийфосфата с сульфатом натрия. Процесс можно осуществить в шахтной печи с регулированием температуры в зонах испарения, прокаливания и полимеризации 130.
Описана131 установка для получения стекловидного фосфата расплавлением NaH2P04 при 800° в электрической печи с двумя угольными электродами, через которые пропускается переменный ток 200 в.
Предложено132 получение стекловидного фосфата во вращающейся трубчатой печи из смеси, состоящей из 0,5—1,5 моль NaH2P04, 1,5—0,5 моль КН2Р04 и 0,1—0,45 моль Na2HP04, которую нагревают до 430—480° и затем быстро охлаждают. В такой же печи возможно получение триметафосфата щелочных металлов. Мононатрийфосфат смешивают с 13—60% КН2Р04 и с ретурным триметафосфатом, и смесь нагревают до 360—420°.
Представляет интерес непосредственное получение мета- (и три - поли-) фосфата из фосфора и соды 133 в камерах для сжигания фосфора, минуя операции приготовления исходных растворов и их упаривание. При 600—700° образуются твердые продукты с отношением Na20 : Р205 от 1 : 1 до 1 :2, в том числе и 5 :3:
Р4>+ 502 + 0,5XNa2C03 = (0,5;TNa20) • 2Р205 + 0,5*С02
Пирофосфат натрия получают дегидратацией динатрийфосфата при 350—400°:
2Na2HP04 = Na4P207 + Н20
В присутствии небольших количеств NaH2P04 снижается температура и увеличивается скорость конденсации динатрийфосфата 1з4.
Скорость образования пирофосфата зависит также от молярного отношения Na20 : Р205135. Она имеет минимальную величину при 170° при отношении Na20 : Р205, равном 1,5, вследствие образования соли NaH2P04 • Na2HP04, устойчивой до температуры превращения ее в пирофосфат. Добавка ~1% NH4N03 к весу безводного NaHP04 ускоряет примерно в 2 раза реакцию образования пирофосфата при 300°136.
Пирофосфат натрия можно получать в такой же аппаратуре, как и триполифосфат137 с соответствующим изменением режима по нейтрализации кислоты, упарке раствора и температуре прокаливания. Для перехода с производства одного продукта на другой требуется ~4 ч. Термическую фосфорную кислоту (70—80%) нейтрализуют кальцинированной содой до рН = 8,8—9,0. Раствор кипятят для удаления С02, выпаривают до концентрации 48—50% Na2HP04 и смешивают с 3—4 вес. ч. оборотного продукта (до содержания влаги в смеси 10—12%). Смесь нагревается топочными газами до 360—400° во вращающемся барабане. Спекшиеся «частицы размером до 10 мм после охлаждения измельчают. Безводный пирофосфат натрия содержит 52—53,5% общей Р2О5, в том числе 50,5—52% в пиро-форме и 0,9% в орто-форме.
Аналогичным методом получают пирофосфат и из экстракционной фосфорной кислоты 138.
Пищевой пирофосфат натрия получают перекристаллизацией технического пирофосфата86. Водный раствор, содержащий ~22% Na4P207, полученный растворением технической соли в воде или оборотном маточном растворе, фильтруют при 70°. Из осветленного раствора охлаждением до 13—15° выделяют десятиводные кристаллы пирофосфата натрия.
Кислый пирофосфат натрия Na2H2P207 получают осторожной дегидратацией мононатрийфосфата при 225—250° или обработкой при более высокой температуре, но в течение очень короткого времени 139> 140:
2NaH2P04 = Na2H2P207 + Н20
Выше 250° образуется не растворимая в воде соль Маддреля, ниже 220° сильно снижается степень конверсии ортофосфата в пирофосфат. Готовый продукт содержит до 63,9% P2Os. Его раствор имеет рН около 4,2.
Тринатрийпирофосфат получают123-141 взаимодействием тетра - натрийфосфата с соляной кислотой:
Na4P207 + НС1 = Na3HP207 + NaCl
. Исходный технический пирофосфат натрия растворяют при 20—25° в воде и фильтруют нерастворимые примеси. Из осветленного раствора, содержащего 20—22% Na4P207, охлаждением до 10° выделяют Na4P207- ЮН20.
После отделения кристаллов на центрифуге их обрабатывают соляной кислотой концентрацией 35% НС1 при 35° в реакторе, снабженном мешалкой и рубашкой, в которую, по мере необходимости, подают пар или воду. В полученном растворе концентрация солей должна быть не более 35%. При охлаждении рассолом до 0—1% из него выделяют кристаллы Na3HP207 • 9Н20. Их отделяют центрифугированием от маточного раствора (хлористого натрия). В полученном продукте содержится: 31—33% Р2О5, 0,005—0,01% не растворимых в воде веществ, 0,5—0,6% хлоридов (в расчете на хлор), менее 0,15% S03, менее 0,01% Fe.