Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
АММИАЧНЫЙ способ улавливания и переработки фтористых газов
|
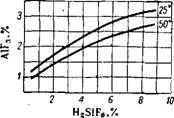
Рис. 338. Растворимость A1F3 В кремнефтористоводородной кислоте при 25 и 50°. |
Представляет интерес получение из отбросных фтористых газов или из продуктов их улавливания фтористого аммония, легко перерабатываемого в другие фтористые соединения 337>338.
Растворами фторида аммония можно пользоваться для получения почти всех ныне применяемых фтористых солей, причем полученные аммиачным методом они содержат меньшее количество примесей. Этот метод позволяет избежать затраты соды, применяемой для получения некоторых фтористых солей. Кроме того, при этом методе не имеет места частичный выход фтора в виде относительно1 менее ценного кремнефтористого натрия, являющегося побочным продуктом при получении фтористых солей сернокислотным разложением плавикового шпата. Это позволяет с успехом перерабатывать не только отходящие фтористые газы, но и низкосортный не - обогащенный шпат, содержащий 40—50% CaF2, с предварительным получением из него кремнефтористоводородной кислоты 339. Повышенное содержание кремнезема в шпате при этом не только не является нежелательным, но, наоборот, дает возможность увеличить выход побочного продукта — белой сажи.
При нейтрализации аммиаком или аммиачной водой кремнефтористоводородной кислоты, полученной из отходящих фтористых газов, а также неочищенной плавиковой кислоты, получающейся при кислотной переработке плавикового шпата, идут следующие реакции:
HF + NH3 = NH4F H2SiF6 + 2NH3 = (NH4)2SiF6 (NH4)2SiF6 + 4NH3 + (n + 2)H20 = 6NH4F + Si02 • nH20
При непосредственном улавливании фтористых газов аммиачной водой
SiF4 + 4NH4OH + aq = 4NH4F + Si02 • лН20
Четырехфтористый кремний легко поглощается практически полностью. При абсорбции SiF4 6—10% раствором аммиака образующаяся кремневая кислота хорошо отстаивается и сравнительно легко отделяется от жидкости. Более слабые или более крепкие растворы аммиака дают или хлопьевидный, трудно фильтрующий, или студневидный осадок 340. Лучшим вариантом является абсорбция фтористых газов 8—9%-ным раствором NH4F с последующей нейтрализацией образующегося кислого раствора [18—20% (NH4)2SiF6 + 2% H2SiF6] аммиаком или аммиачной водой 257.
Выделившийся осадок аморфной кремневой кислоты после промывки, сушки и разрыхления выпускается в виде белой сажи. После отделения осадка кремневой кислоты остаются весьма чистые растворы фторида аммония, которые и перерабатываются на различные фтористые соли.
Фторид аммоння хорошо растворим в воде. При нагревании сухой соли и ее растворов происходит диссоциация с выделением аммиака и образованием бифторида аммония согласно уравнению:
2NH4F = NH4F-HF + NH3
Кремнефторид аммония также хорошо растворим в воде и при взаимодействии с аммиаком разлагается согласно уравнению реакции, приведенному выше. Эта реакция обратима и подбором соот-_ ветствующих условий ее можно проводить практически до конца <как в одном, так и в другом направлении. При 15—20° и небольшом избытке аммиака (4—7 г[л) получаются почти чистые растворы фторида аммония, а кремнезем опять переходит в раствор.
Это позволяет перерабатывать на ценную белую сажу, обладающую хорошими адсорбционными свойствами, любой кремнеземистый материал. Процесс сводится к обработке кварцевого песка и других кремнеземистых материалов раствором фторида аммония при нагревании или предварительно полученным из него бифтори - дом аммония. При этом выделяется аммиак. Процесс идет через следующие промежуточные реакции:
2NH4F = NH4F.HF + NH3 4NH4F • HF + Si02 = 4NH4F + SiF4 + 2H20 SiF4 + 2NH4F = (NH4)2SiF6
Рекомендуются 257 следующие условия производства. Кварцевый песок, просеянный через сито 0,5 мм, промывают водой, потом слабой соляной кислотой (для удаления карбонатов и соединений полуторных окислов) и снова водой. Затем его обрабатывают при ■80° и перемешивании раствором бифторида аммония с концентрацией 30% (лучше более 50%). Получающийся раствор кремнефторида аммония отфильтровывают от неразложившегося остатка и насыщают при 15—20° до слабо щелочной реакции аммиаком, выделившимся в первой стадии процесса. При этом 8Юг выделяется •обратно в твердую фазу, но уже в виде геля, который после промывки и сушки суспензии в распылительной сушилке обладает ценными активными свойствами. Раствор фтористого аммония вновь возвращается в цикл.
Переработка раствора фторида аммония на фтористые соли осуществляется следующими способами.
Непосредственным выпариванием этого раствора до насыщенного состояния и последующей кристаллизацией может быть получен твердый фторид аммония. Так как при выпаривании идет ■частичная диссоциация NH4F с образованием кислой соли и удалением аммиака, то выделяющийся аммиак улавливают и возвращают в выпариваемый раствор к началу кристаллизации соли. Это •обеспечивает выделение в осадок средней соли, которую отделяют и высушивают при 35—40°. Маточный раствор возвращают на выпаривание. При выпаривании раствора NH*F без возврата NH3 получается плав, состоящий из смеси NH4HF2 (70—75%) и NH4F (16—20%), который при охлаждении на холодильных вальцах превращается в твердый чешуйчатый продукт — фторид-бифторид аммония. Он сильно гигроскопичен, на воздухе расплывается. Аппаратура для выпарки раствора NH4F изготовляется из стали ЭИ-44& или из графитопласта.
Криолит можно получить, прибавляя к нагретому раствору NH4F алюминат натрия, по реакции:
6NH4F + Al(ONa)3 = Na3AlF6 + 6NH3 +3H20
Выделяющийся аммиак улавливают и возвращают в цикл, а криолит отфильтровывают от маточного раствора и сушат. Изменяя модуль алюмината (т. е. отношение Na20 к А1203),' можно получать или криолит (3NaF-AlF3) или хиолит (5NaF-3AlF3).
Криолит может быть выделен и из кислого раствора NH4F (рН « 5,5), который смешивают без нагревания с раствором алюминиевой и натриевой соли:
12NH4F + 3Na2S04 + A12(S04)3 = 2Na3AlF6 + 6(NH4)2S04
Полученный криолит отфильтровывают, промывают и сушат - Из раствора (NH4)2S04 регенерируют аммиак281.
Фторид натрия можно осадить из растворов NH4F:
2NH4F + Na2C03 = 2NaF + 2NH3 + H20 + C02
2NH4F + Na2S04 = 2NaF + (NH4)2S04
NH4F +NaCl = NaF+ NH4C1
Наиболее прост первый вариант, так как в нем сразу регенерируется почти весь аммиак, который может быть возвращен в цикл. Однако применение для осаждения NaF относительно более дорогой соды и получение трудно используемого маточного раствора,, содержащего около 4% NaF, снижают ценность этого метода.
По второму варианту наряду с осадком NaF образуется раствор> сульфата аммония, содержащий до 40 г/л NaF. Избыток сульфата натрия не высаливает NaF, так как образуется двойная соль Na2S04 • 2NaF. Выделить оставшийся в растворе фтор можно в виде - криолита добавлением к раствору сульфата алюминия: 12NaF + A12(S04)3 = 2Na3AlF6 + 3Na2S04
Это усложняет производство фторида натрия, но позволяет получать криолит.
Наиболее целесообразным является третий вариант, так как избытком поваренной соли можно выделить из раствора почти весь фторид натрия, выход которого из раствора достигает 95% (при стехиометрическом количестве NaCl выход NaF 60%, при 25%-ном избытке выход 70% и при 100%-ном избытке выход 96%). Выход NaF возрастает также с увеличением содержания аммиака в растворе и достигает максимальной величины при 12% NH3. В этом; случае и при 50% избытке NaCl выход NaF ~90% 340. После отделения кристаллов NaF аммиак может быть регенерирован из;
Маточного раствора хлористого аммония обычным способом — обработкой известковым молоком при нагревании.
Фторид алюминия может быть получен нагреванием раствора - фторида аммония с гидроокисью алюминия в течение 6—8 ч. При этом осаждается крупнокристаллический, легко фильтрующий аммониевый криолит (NH4)3A1F6 или 3NH4F-A1F3. Так как в газовую фазу вследствие диссоциации NH4F удаляется аммиак и в растворе образуется бифторид аммония, то реакция, видимо, проходит по уравнению:
3NH4HF2 + А1(ОН)3 = (NH4)3A1F6 + ЗН20 .
Осадок отфильтровывают и прокаливают при 450—500°. При этой температуре происходит разложение комплексной соли с образованием A1F3. Выделившиеся газы (NH3 - Ь HF) могут быть уловлены и возвращены в производство.
Фторид алюминия получается при нагревании окиси алюминия ■с бифторидом аммония выше 130° по реакции
А120з + 3NH4HF2 = 2A1F3 + 3NH3 + 3H20
Которая идет в две стадии. Вначале с экзотермическим эффектом происходит нейтрализация кислого фторида аммония окисью алюминия
А1203 + 6NH4HF2 = 2A1F3 + 6NH4F + 3H20
Причем в газовую фазу выделяется водяной пар и лишь небольшое количество аммиака. При дальнейшем нагревании окись алюминия реагирует с фторидом аммония:
А1203 + 6NH4F = 2A1F3 + 6NH3 + 3H20
В качестве побочных промежуточных продуктов образуются аммониевый криолит (NH4)3A1F6 и комплексная соль NH4A1F4, которые выше 440° полностью разлагаются. При этом в газовую фазу удаляется и некоторое количество NH4F341.
Описан циклический способ производства A1F3 342. Вначале получают тетрафторборную кислоту HBF4 разложением плавикового шпата раствором, содержащим 216 г/л H2S04, 110 г/л Н3В03 и 50 г/л (NH4)2S04 при нагревании в течение 6 ч. После охлаждения и нейтрализации избытка серной кислоты известняком тетрафторборную кислоту отфильтровывают от осадка сульфата кальция и обрабатывают гидроокисью алюминия и аммиаком (или карбонатом аммония); при этом выделяется в осадок двойная соль NH4F-A1F3. Эту соль отделяют от раствора Н3В03, возвращаемого в цикл, и нагревают в смеси с А1203 или А1(ОН)3 до ~350° (по другим данным80, до 450—500°); образуется A1F3 и аммиак, который возвращают в процесс.
В отличие от 3NH4F-A1F3, устойчивого до 100°, который выделяется в осадок при введении раствора A1F3 в избыток раствора NH4F, образование NH4F-A1F3 происходит при введении рассчитанного количества NH3 в раствор А1(ОН)3 в плавиковой кислоте. Двойная соль NH4F-A1F3 может быть получена и обработкой раствора NH4F гидроокисью алюминия. Если к водной суспензии NH4F-A1F3, нагретой до 90°, добавлять постепенно NaF, образуется осадок Na3AlF6. Промытый криолит имеет примерный состав: 46% AlFs, 53,6% NaF, 0,5% А1203-ЗН20 343.
Получаемые из отходящих фтористых газов фторид и бифторид аммония могут служить полупродуктами для производства концентрированного фтористого водорода. Их можно разлагать серной кислотой по реакциям:
NH4F + H2S04 = NH4HSO4 + HF NH4HF2 + H2S04 = NH4HS04 + 2HF
По второй реакции расход аммиака и серной кислоты, а также количество побочного продукта — бисульфата аммония — в 2 раза меньше, чем по первой. При разложении кристаллического бифто - рида аммония 93—98%-ной серной кислотой при 200—250° выход HF составляет 93—96%, а содержание фтора в бисульфате аммония 0,5—1% 344'345. Безводный HF выделяется из твердых фторида или бифторида аммония при действии на них хлористым водородом; в твердой фазе остается хлорид аммония 346.
Большой интерес представляет термический метод, не требующий расхода реагентов и не дающий побочных продуктов или отходов. Он заключается в получении из фторидов аммония бифторида натрия и его термическом разложении 347. Раствор фторида аммония выпаривают, при этом получается бифторид аммония:
2NH4F = NH4HF2 + NH3
Аммиак вновь используется для получения NH4F из фтористых газов, а раствор бифторида аммония обрабатывают твердым NaF:
NH4HF2 + NaF = NaHFj + NH4F
Маточный раствор NH4F возвращается на получение бифторид». аммония, a NaHF2 разлагают при 300°:
NaHF2 = NaF + HF
Фторид натрия вновь используют для обработки NH4HF2 348.
Предложено также34Э-350 подвергать термическому разложению непосредственно NH4HF2. При этом вначале получают смесь HF и NH3, затем ее пропускают через никелевый катализатор при 700—800° для разложения NH3 на N2 и Н2. Из полученной смеси. 1 IF, N2 и Н2 конденсируют HF.
Аммиачный метод позволяет получать и осажденный, в частности весьма дисперсный и пористый фторид кальция 351-352. При нейтрализации полученной из отходящих фтористых газов (или другим путем) кремнефтористоводородной кислоты молотым мелом образуется осадок смеси CaF2 и Si02:
H2SiFe + ЗСаСОз = 3CaF2 + Si02 + Н20 + 3C02
Для освобождения от Si02 влажный осадок обрабатывают рас - ллавом фторид-бифторида аммония:
Si02 + 4NH4HF2 = (NH4)2SiF6 + 2NH4F + 2H20
Оставшийся CaF2 отфильтровывают, промывают и высушивают, а маточный раствор усредняют аммиаком для перехода кремнефторида во фторид аммония:
(NH4)2SiF6 + 4NH3 + 2Н20 = 6NH.,F + Si02
Выделившаяся двуокись кремния после промывки и сушки является побочным продуктом — белой сажей, а раствор NH4F и промывная вода упариваются. При этом получается возвращаемый в процесс плав фторид-бифторида аммония:
2NH4F = NH4HF2 + NH3
Аммиак улавливается водой и также снова используется. В этом процессе для получения легко отделяемого на фильтре осадка CaF2 + Si02 следует добавлять кремнефтористоводородную кислоту к меловой пульпе, тогда производительность фильтра достигает 500—700 кг/(м2-ч) сухого вещества. При обратном порядке смешения реагентов она резко уменьшается [до 30 кг/(м2-ц)]. Она значительно уменьшается [до 180 кг/(м2-ч)] и при использовании осажденного карбоната кальция. Степень обескремнивания осадка фторид-бифторидом аммония при 70° достигает 98%. Производительность фильтрации обескремненного CaF2 45—50 кг/(м2-ч), но она возрастает до 360 кг/(м2-ч) сухого вещества при использовании для получения смеси CaF2+Si02 осажденного карбоната кальция.
По другому варианту CaF2 можно изготовить по следующей схеме. Отходящие фтористые газы улавливают оборотным раствором NH4F, который затем нейтрализуют аммиаком. Осадок кремневой кислоты отделяют, промывают, высушивают и выпускают з виде белой еажи, а раствор NH4F упаривают для получения плава бифторида и фторида аммония; выделяющийся при этом ам - эшак возвращается в процесс. Плав вводится в меловую пульпу ^концентрация которой 1 : 3) для осаждения CaF2:
2NH4HF2 + СаСОз = CaF2 + 2MH4F + С02 + Н20
Осадок CaF2 отфильтровывают, промывают и высушивают. Раствор NH4F возвращается в процесс; промывная вода идет на приготовление меловой пульпы. При использовании для осаждения. CaF2 пульпы из осажденного карбоната кальция производительность фильтрации достигает 1300 кг/(м2-ч), а при работе с сепарированным мелом — всего 100 кг/ (м2 • ч). Содержание Si02 в готовом продукте 0,3—0,5%.
Вместо СаСОз для осаждения CaF2 из раствора NH4F можно - использовать СаО, а также CaS04. В последнем случае идет конверсия:
2NH4F + CaS04 = CaF2 + (NH4)2S04
При использовании фосфогипса степень конверсии по фтору достигает 95—97%, в продукте содержится 88—90% CaF2, ~6% CaS04, 0,5—0,6% Si02. Производительность фильтрации. ~ 150 кг/(м2- ч) сухого вещества; влажность осадка ~48%. Остающийся после отделения CaF2 раствор [20—22% (NH4)2S04] может - быть переработан в побочный продукт — сульфат аммония.
Фторид кальция может быть получен взаимодействием растворов NH4F и СаС12. Раствор NH4F (~135 г/л) с небольшой скоростью (в виде брызг) вводят в кипящий раствор СаС12 (60— 300 г/л), взятый с 5—25%-ным избытком по отношению к фториду и предварительно подкисленный соляной кислотой до содержания 0,05—0,25% НС1. Осадок отфильтровывают и промывают на центрифуге, сушат и размалывают образовавшиеся после сушкге комки 353
Фторид кальция, полученный из раствора NH4F осаждением' карбонатной суспензией состоит из плотных кристаллов размером 1,8—3,2 мк; при осаждении окисью кальция и хлористым кальцием- получаются пористые кристаллы с размером 0,01—0,1 мк 282.
Фторид магния также получают аммиачным способом 257>354. Он заключается в обработке кремнефтористоводородной кислогьг при 70—75° окисью магния (каустическим магнезитом) и в последующем отделении кремнегеля с помощью бифторида аммония.. При растворении MgO вначале образуется MgSiFe
MgO + H2SiFe = MgSiF6 + H20 который при дальнейшей нейтрализации гидролизуется: 3MgSiF6 + 2Н20 = 3MgF2 + Si02 + 2H2SiF6
В результате процесс идет по суммарной реакции: 3MgO + H2SiF6 = 3MgF2 + Si02 + H20
Для разделения твердых продуктов этой реакции — MgF2 it Si02 — их обрабатывают при 70—75° раствором фторид-бифторида аммония. При этом кремнегель растворяется:
4NH4HF2 + Si02 = (NH4)2SiF6 + 2NH4F + H^O
Присутствующая в растворе свободная H2SiF6 также превращается в кремнефторид аммония:
2H2SiF6 + 6NH4F + Si02 = 3(NH4)2SiF6 + 2Н20
Осадок MgF2 отделяют от раствора на фильтре, промывают, репульпируют в воде и высушивают в распылительной сушилке. При этом исключается последующий размол. Продукт содержит 83—85% MgF2 и 2—4% CaF2. Раствор, содержащий 16—18% (NH4)2SiF6 вновь перерабатывают в фторид-бифторид аммония.
При получении MgF2 описанным аммиачным Способом двойные фториды магния и аммония не образуются. Гидратированная соль (NH4)2MgF4-2H20 получается при взаимодействии MgF2 с концентрированным раствором NH4F. Эта соль при 110° дегидратируется, при 215° разлагается с выделением одной молекулы NH4F, а при 285° распадается на NH4F и MgF2. Безводные соли NH4MgF3 и (NH4)2MgF4 можно получить сплавлением MgF4 и NH4F (при ]80°) 35s.