Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Абсорбция и конденсация фтористого водорода
Абсорбция HF производится последовательно в нескольких свинцовых или пластмассовых башнях диаметром 2 м, высотой 6—8 м, заполненных коксом, угольными кольцами или деревянными рейками. Если используют стальные башни, то их гуммируют и футеруют в два слоя угольными блоками на бакелитовой замазке. Последняя башня орошается водой, и получаемая слабая кислота передается на орошение предыдущих башен противотоком газу. Из первой по ходу газа башни вытекает продукционная кислота. Для просасывания газов через систему за последней абсорбционной башней устанавливают гуммированный вентилятор. Такой вентилятор не может дать большого разрежения, и иногда, для уменьшения сопротивления системы, башни включают параллельно, попарно. С этой же целью иногда применяют полые башни, без насадки, в которых абсорбция идет на поверхности падающих капель жидкости. С газом, уходящим из абсорбционной установки, теряется менее 1 % фтора. Для обезвреживания этого газа его промывают раствором соды.
Кислота циркулирует с помощью эбонитовых насосов. Иногда ее охлаждают в змеевиковых холодильниках; это позволяет получать более концентрированную кислоту. Как видно из рис. 314 (стр. 1097), для получения стандартной плавиковой кислоты, содержащей 40% HF, при 25° требуется, чтобы концентрация HF в газе, поступающем на абсорбцию, была выше 7 мг/л, а при 50° — выше 30 мг/л.
Основное количество получаемой кислоты обычно сразу же перерабатывают на фтористые соли. В этом случае не стремятся получать концентрированную кислоту. Орошение башен водой регулируют таким образом, чтобы в продукционной кислоте содержалось 28—30% HF.
На получение 1 т 100%-иого HF в плавиковой кислоте расходуется: 2,55 т плавикового шпата (100% СаРг), 3,75 т серной кислоты (100% H2S04).
В абсорбционных башнях, помимо поглощения HF, происходит конденсация H2SiF6. Количество HgSiFe в «грязной» плавиковой кислоте, вытекающей из абсорбционной установки, зависит от содержания Si02 в плавиковом шпате и колеблется от 2 до 10%. Очистку плавиковой кислоты от H2SiF6, дающую побочный продукт— кремнефторид натрия, производят обработкой ее содой в стальных гуммированных чанах с лопастными мешалками. Образующийся по реакции
H2SiF6 + Na2C03 = Na2SiF6 + Н20 + С02
Плохорастворимый кремнефторид натрия выделяется в осадок, который отделяют отстаиванием или отфильтровывают на вакуум - фильтре и промывают водой. Промывную воду добавляют к плавиковой кислоте, идущей на переработку во фтористые соли.
Применение избытка соды для осаждения Na2SiF6 недопустимо, так как при этом нейтрализуется часть HF и получаемый NaF также осаждается, а содержащаяся в плавиковой кислоте серная кислота (0,5—1,5%) переводится в Na2S04:
2HF + Na2C03 = 2NaF + Н20 + С02 H2S04 + Na2C03 «= Na2S04 + H20 + C02
При применении же стехиометрического количества соды, требуемого для очистки от H2SiF6, эти реакции не имеют значения, так
Как растворимость Na2SiF6 меньше, чем растворимость NaF и Na2SC>4, и потому имеющаяся в растворе кремнефтористоводород - ная кислота осаждает NasSiFg из этих солей по реакциям: 2NaF + H2SiF6 = Na2SiF6 + 2HF Na2S04 + H2SiF6 = Na2SiF6 + H2S04
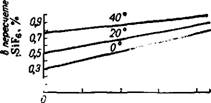
В очищенной кислоте содержится немного H2SO4, NaF и некоторое количества Na2SiF6, зависящее от концентрации HF и температуры (рис. 325)135; содержание Na2SiFe несколько больше соответствующего его растворимости.
Заводы, перерабатывающие плавиковую кислоту в криолит, «теряют» значительную часть фтора, выпуская его в виде кремнефторида или фторида натрия, получаемых в качестве побочных продуктов в процессе очистки «грязной» плавиковой кислоты. Чем меньше содержится Si02 в исходном плавиковом шпате, тем fg± меньше эти «потери». Впрочем, Kg получаемую при очистке пульпу £ кремнефторида натрия можно также переработать сначала в NaF, а затем взаимодействием NaF с A1F3 в криолит (стр. 1160)163. Рис -
Для получения плавиковой кислоты, не содержащей H2SiF6
Или Na2SiF6, предложено очищать печной газ от SiF4 до абсорбции HF. Очистка от SiF4 может быть осуществлена и сухим способом, при использовании в качестве поглотителей кислых фторидов калия, натрия или бария, образующих кремнефториды, стойкие при температуре газа, выходящего из печи94.
Предложен 164 способ очистки газообразного HF от SiF4 в процессе абсорбции. Для этого газ нагревают до 150—500° и затем направляют в абсорбер, где за счет вносимого газом тепла идет разделение н концентрирование получаемых кислот — из нижней части колонны отбирают концентрированный раствор H2SiF6, а из средней 25—38%-ную плавиковую кислоту. Уносимая газом вода конденсируется в дефлегматоре. Для очистки технической плавиковой кислоты от летучих примесей (H2S1F6, S02) рекомендуют 165 подвергать ее дистилляции, сопровождаемой продувкой воздухом или азотом под давлением 2,5 ат, при температуре в кубе 48°. Расход воздуха 25 кг на 1 кг HF, потери HF с отходящим газом 1%.
|
5 10 15 20 HP В очищенной кислоте, % |
|
325. Растворимость Na2SiFe В плавиковой кислоте. |
Описана166 опытно-промышленная установка для получения 80%-ной плавиковой кислоты двухступенчатой конденсацией HF из печного газа. В первой ступени конденсируются пары воды,
H2SO4, H2SiF6 и часть HF — конденсат отводится в виде «грязевой кислоты». Во второй ступени в трубчатом противоточном теплообменнике конденсируется кислота, содержащая 80% HF. Не- сконденсировавшаяся часть HF поступает на водную абсорбцию.