Общие положения теории кристаллизации
Кристаллизация расплавленного металла состоит из двух элементарных, одновременно протекающих процессов:
1) зарождения зародышей или центров кристаллизации;
2) роста кристаллитов из этих центров.
В зависимости от способов образования зародышей различают гомогенную или гетерогенную кристаллизацию. В чистом от примесей жидком металле при охлаждении зародыши образуются из наиболее крупных фазовых флуктуаций жидкой фазы, выделение которых связано с флуктуациями энергии (гомогенное зарождение). В технических металлах всегда имеются дисперсные включения примесей, на поверхности которых и происходит образование центров кристаллизации (гетерогенное зарождение).
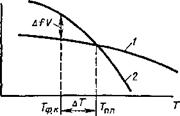
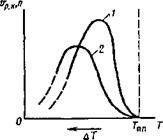
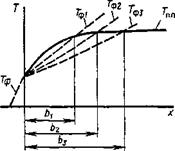
Движущая сила кристаллизации любого типа — разный характер изменения свободной энергии металла в жидком и твердом состояниях в зависимости от температуры (рис. 12.1). При температуре выше некоторой критической 7’пл меньшей свободной энергией обладает вещество в жидком состоянии, а при температуре ниже 7'пл энергетически более устойчиво твердое состояние металла.
Температура Гпл, при которой равновероятно как твердое, так и жидкое состояние,— равновесная или теоретическая температура кристаллизации. Затвердевание металла при этой температуре еще не происходит. Для кристаллизации необходимо образование зародышей и их рост в результате присоединения частиц контактирующей с ними жидкости. Это достигается при температуре ниже критической, т. е. при переохлаждении.
Температура Тфк> при которой практически начинается кристаллизация, называется фактической температурой кристаллизации.
Степенью переохлаждения АТ называют разность между теоретической и фактической температурами кристаллизации.
|
F |
|
Рис. 12.1. Зависимость свободной энергии твердого (/) и жидкого (2) металла от температуры |
Переохлаждение в чистых металлах называется термическим, в сплавах, где температура 7’пл уменьшается с повышением концентрации примеси, — концентрационным.
В результате кристаллизации освобождается некоторая энергия — теплота кристаллизации, численно равная скрытой теплоте плавления. Эта теплота отводится через границу раздела твердой и жидкой фаз в более холодное твердое тело.
|
|
|
Рис. 12.2. Изменение свободной |
|
~3г Гк= |
|
Af ' г Подставим значение г* в уравнение (12.3) и получим |
|
энергии в зависимости от размера * с 16 о3 ,1Г> сч зародыша «= (12.5) |
|
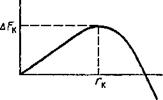
Из рис. 12.1 видно, что чем ниже температура Тфк, тем больше разность свободных энергий жидкого Рж и твердого Fk металла. Изменение свободной энергии на единицу объема V затвердевающего вещества будет равно A f = (F*-FK)/V. (12.1) При кристаллизации объема V свободная энергия системы уменьшается на величину AfV. Одиако при зарождении и росте кристаллов иа их границе с жидкостью возникает и увеличивается поверхностная энергия oS„ (о — поверхностное натяжение, S„ — суммарная площадь поверхности кристаллов). Общее изменение свободной энергии AF = oSB-AfV. (12.2) Термодинамическая система стремится к минимуму свободной энергии. Зародыш будет расти, если при этом AF, уменьшается, т. е. при условии AfV > oSn. Для зародыша сферической формы уравнение (12.2) можно записать в виде AF = 4nr2o — (4/3)nr3Af. (12.3) Изменение свободной энергии в зависимости от размера зародыша характеризуется кривой с максимумом (рис. 12.2), На первых стадиях рост зародыша приводит к увеличению свободной энергии и его существование будет неустойчивым. При определенном критическом размере зародыша гк изменение свободной энергии достигает максимума. Дальнейший рост кристаллического зародыша приводит к уменьшению AF и может продолжаться неограниченно. Зародыши критической величины, возникшие как флуктуационные образования, становятся центрами кристаллизации, из которых вырастают кристаллы. Значения гк и AFK можно рассчитать, используя выражение (12.3). Найдем частную производную лг d(AF)_ а-4л-2гк— Af •—л*3ri or З ы ^(АГ) п Из условия ■ ' = 0 находим гк: |
|
20 (12.4) |
Выразив значение Af из выражения (12.4) и подставив его в уравнение (12.5) для зародыша сферической формы, у которого sn = 4nr2K, получим
A FK=—os„. (12.6)
Выражение (12.6) показывает, что при образовании зародыша критического радиуса поверхностная энергия на границе кристалл — жидкость на '/з компенсируется энергией флуктуации AFK, а на 2/з — объемной свободной энергией.
Из уравнения (12.4) видно, что г« тем меньше, чем больше величина Af, которая растет с увеличением АТ (рис. 12.1).
Можно записать
Af = ATAs = ATQ/Tm. (12.7)
где As — изменение энтропии при затвердевании; Q — скрытая теплота затвердевания единицы объема. Следовательно,
L. (12.8)
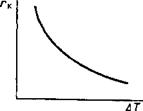
Из уравнения (12.8) видно, что критический размер зародыша уменьшается с увеличением степени переохлаждения (рис. 12.3). При этом создаются условия для образования большего числа зародышей. Увеличение переохлаждения, как следует из анализа уравнений (12.5) и (12.7), приведет также к уменьшению AF к-
Подставив значение Af, выраженное согласно (12.7), в выражение (12.5), получим
A (12.9)
Чем меньше критический радиус зародыша и чем меньше флуктуация энергии, требуемая для его образования,-тем больше вероятность образования зародышей wi (чцело возникающих зародышей).
Согласно статистическим представлениям термодинамики,
|
|
Ші =М, є-д^бП (12.10)
где &б — постоянная Больцмана.
Однако с увеличением переохлаждения процесс диффузии будет тормозиться, замедляя подход новых атомов из жидкости к кристаллу. Вероятность перехода атома из жидкой фазы в твердую при образовании зародыша
W2 = M2e ^бТ) (12.11) Рис. 12.3. Зависимость
. критического размера за-
где и — энергия активации самодиф - родыша от степени пере-
фузии. охлаждения
Вероятность w, определяющая общую скорость образования зародышей (число центров кристаллизации п), равна произведению вероятностей составляющих процессов
|
Рис 12 4 Влияние степени переохлаждения на условия образования зародышей |
w = wiw2 = M3e~{hFK + V)RHT) (12 12)
В формулах (12.10)...(12.12) М, Мг, Мз — постоянные коэффициенты, зависящие от свойств материала.
После подстановки значения AF* в выражение (12.12) получим зависимость числа центров кристаллизации п от температуры:
= Мзехр)--^.[У+4-ла(^)2]}. (12.13)
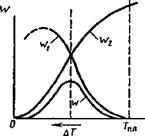
Таким образом, под влиянием двух противоположных тенденций при изменении температуры складываются оптимальные условия, при которых скорость образования зародышей кристаллизации максимальна (рис. 12.4).
W =
ГЕТЕРОГЕННАЯ КРИСТАЛЛИЗАЦИЯ И СКОРОСТЬ
КРИСТАЛЛИЗАЦИИ
Поверхность раздела между образующейся твердой и исчезающей жидкой фазами создает энергетический барьер при гомогенном возникновении зародышей, для преодоления которого необходима флуктуация энергии, равная AFK Поэтому энергетически более выгодно возникновение зародышей твердой фазы в кристаллизующейся жидкости преимущественно на готовых межфазных поверхностях. Такими поверхностями при гетерогенной кристаллизации могут быть поверхности твердых частиц, всегда существующие в технических расплавах.
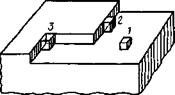
Наилучшие очаги гетерогенной кристаллизации — частицы или поверхности того же металла, что и расплав, например зерна основного металла, ограничивающие жидкую сварочную ваину. Оплавленные зерна основного металла становятся зародышевыми центрами кристаллизации, на которых, как на своеобразной подкладке, начинают расти первичные кристаллы шва (рис. 12.5). Растут кристаллы нормально к поверхности охлаждения в глубь жидкого металла ванны, в направлении, обратном отводу теплоты.
При наличии готовых межфазных поверхностей увеличивается вероятность гетерофазных флуктуаций. Это приводит к появлению плоских зародышей кристаллитов на межфазной поверхности. Энергетические условия образования плоских зародышей отличаются от условий возникновения трехмерных зародышей,
Рис 12 5 Схема роста кристалли - Рис 12 6 Схема образования плос-
тов в сварочной ванне кого зародыша
поэтому критическое состояние достигается при различных значениях переохлаждения.
Определим критический радиус плоского зародыша (рис. 12.6). При его возникновении на поверхности кристаллита площадь межфазной поверхности возрастает только на величину боковой поверхности зародыша.
Баланс свободной энергии при возникновении плоского зародыша аналогично (12.2) будет
AF = 2лгаа — лг2аД/. (12.14)
Аналогично рассмотренному выше случаю образования трехмерного зародыша критический радиус плоского зародыша
сг аТ„. 1
(12.15)
к Л/ Q ЛГ '
Критическое значение свободной энергии составит
» г - ЗССТЯ 1 n 3tC5 аТг, л мп і п.
^=-KT-TcS"=-IfQ-- <1216>
Таким образом, число центров поверхностных зародышей, образующихся вследствие флуктуации свободной энергии, с учетом процесса диффузии атомов будет равно
ж = М<ехр[__і_(и,+ "=.)], (,2.17)
где U і—энергия активации диффузии атомов к плоскому зародышу; М4 — постоянный коэффициент, зависящий от свойств металла.
Из сравнения энергетических условий образования трехмерных (гомогенное зарождение) и двумерных (гетерогенное зарождение) зародышей видно, что для образования плоского зародыша критического радиуса требуются меньшее переохлаждение и меньшая флуктуация свободной энергии, чем при гомогенной кристаллизации.
Линейная скорость роста грани кристалла ирк> на которой образуются плоские зародыши, определяется числом плоских центров кристаллизации, возникающих в единицу времени — формула (12 17). Из сравнения функциональных зависимостей
изменения числа центров кристаллизации (12.13) и линейной скорости роста кристаллов (12.17) от температуры видно, что интенсивности их изменения различны и зависят от степени переохлаждения (рис. 12.7). Несовпадение скорости образования центров кристаллизации и линейной скорости роста кристалла существенно влияет на структуру кристаллитов. Так как при малых АТ скорость роста кристалла растет быстрее, чем число центров кристаллизации, то при малом переохлаждении возникает крупнозернистая структура. Увеличение числа центров кристаллизации и замедление скорости роста будут способствовать измельчению кристаллитов.
|
Рис. 12.7. Зависимость линейной скорости роста кристалла пр к (кривая 1) и числа центров кристаллизации п (кривая 2) от степени переохлаждения |
Достигнув максимума, скорости зарождения и роста кристаллитов начинают снижаться, так как подвижность атомов с понижением температуры понижается.
Каталитическое влияние готовых поверхностей раздела фаз на возникновение зародышей зависит от действия факторов, усиливающих или ослабляющих этот эффект. На процесс гетерогенной кристаллизации влияет краевой угол между подложкой и находящимся на ней зародышем твердой фазы, так как от значения этого угла зависит соотношение поверхностных энергий между зародышем и сосуществующими фазами. Значение краевого угла определяется такими факторами, как близость структур кристаллических решеток подложки и твердой фазы зародыша, а также химическая природа поверхности подложки.
Большинство применяемых в промышленности металлов содержит достаточное количество нерастворимых примесей и гетерогенное зарождение центров кристаллизации в их расплавах происходит при переохлаждениях 1...10 К - Для интенсификации процессов гетерогенной кристаллизации, а также в целях регулирования размеров кристаллитов в расплав вводят модификаторы или катализаторы зарождения, стимулирующие образование зародышей. Эти вещества могут быть соединениями, нерастворимыми в расплаве и хорошо им смачивающимися, т. е. значения краевого угла с образующейся твердой фазой невелики, или химическими элементами, которые образуют с жидким расплавом соединения, способствующие зарождению центров кристаллизации.
Еще один фактор, влияющий на условия гетерогенной кристаллизации,— вид межфазной поверхности, разделяющей зародыш и твердую подложку. В реальных случаях она может быть выпуклой или вогнутой, что вызывает соответственно ослабление или усиление катализирующего влияния подложки.
Кроме того, на поверхности реальных тел, имеющих кристаллическое строение, на гранях растущего кристалла непрерывно возникают различные дефекты поверхности (ступени, выступы) в виде винтовых дислокаций или недостроенных атомных поверхностей. Кромки таких дефектов поверхности энергетически более выгодны для закрепления атомов, переходящих из жидкости в твердую фазу при кристаллизации. Так, на схеме, представленной на рис. 12.8, каждое из последующих положений атома 1, 2, 3 энергетически более выгодно и устойчиво. В случаях 2, 3 отпадает необходимость в образовании двумерных зародышей для начала формирования очередного слоя при идеально плоской грани, т. е. происходит беззародышевый рост кристалла, требующий очень малого переохлаждения (десятые доли кельвина).
|
Рис. 12.8. Схема кристаллизации при наличии дефектов поверхности |
Наличие зон с различной интенсивностью осаждения атомов при кристаллизации приводит к неравномерному росту кристалла в различных зонах. Вблизи выхода на поверхность винтовой дислокации возможен спиральный рост кристалла.
Вероятность образования двумерного зародыша существенно зависит от плотности упаковки атомов грани кристалла, на поверхности которой он образуется. Вероятность минимальна для граней с плотной упаковкой атомов, где поверхностная энергия также минимальна. На гранях же с менее плотной упаковкой, характеризующихся большей поверхностной энергией, зародыш образуется легче.
ОСОБЕННОСТИ КРИСТАЛЛИЗАЦИИ ЧИСТЫХ
МЕТАЛЛОВ И СПЛАВОВ
Рассмотрим направленную кристаллизацию, которая происходит при постоянном направлении отвода теплоты и определенном градиенте температур в жидкой и твердой фазах. Распределение температуры у межфазной поверхности определяется соотношением градиентов температуры в жидкой и твердой фазах, а также выделением при кристаллизации скрытой теплоты плавления. В результате ее выделения температурные градиенты снижаются в области жидкой фазы и возрастают в твердой. Характер распределения температуры у межфазной поверхности определяет ее микрорельеф, а следовательно, и структуру металла, формирующуюся в процессе кристаллизации.
При кристаллизации чистых металлов вследствие флуктуации появляются выступы на межфазной поверхности. Выступы образуются в результате преимущественного развития плоскостей кристалла с высокой плотностью упаковки атомов вследствие
интенсивного образования плоских зародышей на гранях с малой плотностью упаковки.
|
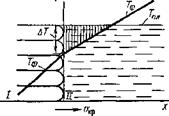
Рис. 12.9. Распределение температур перед фронтом кристаллизации чистого металла: Гф — фактическая температура; ТПЛ — равновесная температура кристаллизации; окр — скорость кристаллизации; / — твердая фаза; // — расплав |
При отсутствии переохлаждения появившийся выступ оказывается в зоне с температурой выше 7'пл, что приводит к уменьшению скорости кристаллизации. Фронт кристаллизации выпрямляется, сохраняя плоское очертание.
При наличии термического переохлаждения АТ (рис. 12.9) выступы, образовавшиеся на межфазной поверхности, попадают в зону переохлаждения. Скорость их кристаллизации увеличивается, и они прорастают вперед. Плоский фронт теряет устойчивость, искривляется, на нем появляются ячеистые выступы. В момент выделения скрытой теплоты плавления процесс роста кристалла приостанавливается, возможно даже его оплавление. Кристаллизация приобретает прерывистый характер.
Сочетание рассмотренных выше процессов, степень переохлаждения расплава перед фронтом кристаллизации могут существенно влиять на его искривление и, таким образом, приводить к формированию различных типов первичной структуры.
В кристаллизации сплавов существенную роль играют диффузионные процессы и степень переохлаждения.
Процесс образования и роста зародыша сопровождается разделительной диффузией в жидкой фазе (на межфазной границе), выравнивающей диффузией в твердой фазе, а в ряде случаев и конвективными потоками в жидкости, также выравнивающими ее состав.
При умеренном переохлаждении образование зародыша в сплаве происходит в условиях установления равновесной разности концентраций примеси в твердой и жидкой фазах (в соответствии с диаграммой состояния).
Вследствие разности концентраций растворенного элемента в твердой и окружающей ее жидкой фазе равновесие может нарушаться в результате диффузионных процессов. Растворенный элемент будет перемещаться в глубь жидкости, а соответствующая часть атомов основного металла для восстановления равновесия перейдет из жидкой фазы в твердую, что приведет к дальнейшему развитию кристаллизации. Такую кристаллизацию называют избирательной или диффузионной.
Если диффузия в жидкой или твердой фазе завершится не полностью (при ускоренном охлаждении расплава), то кристаллизацию называют неравновесной.
В условиях, когда не успевает пройти диффузия в твердой
фазе, среднее содержание примеси в твердой фазе меньше, чем равновесное.
При значительном переохлаждении (очень большие скорости охлаждения) механизм кристаллизации сплава иной. Твердая фаза интенсивно растет в результате присоединения любых атомов, находящихся с ней в контакте: и атомов примеси, и атомов металла. Такую кристаллизацию называют бездиффузионной.
Еще одна особенность кристаллизации сплавов — влияние градиента концентрации растворенного элемента в слое переохлажденного расплава, контактирующего с твердой фазой, на температуру Т„„. При кристаллизации сплавов происходит диффузионное перераспределение примесей между жидкой и твердой фазами. Переохлаждение, связанное с перераспределением примесей, принято называть концентрационным переохлаждением.
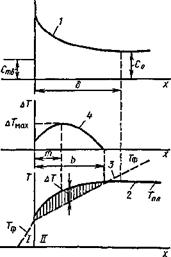
Увеличение концентрации примеси перед фронтом кристаллизации приводит к снижению температуры ликвидуса. При этом возникает область концентрационного переохлаждения АТ (рис. 12.10), поскольку из-за изменения состава 1 этого слоя меняется и температура кристаллизации 2. Фактическая температура 3 расплава, зависящая от сложившихся температурных условий кристаллизации, может быть ниже равновесной температуры 2, что вызывает переохлаждение 4 и обеспечивает возможность кристаллизации.
|
с;и
Рис. 12.10. Параметры концентрационного переохлаждения (/ — твердая фаза, II — расплав) |
Протяженность участка концентрационного уплотнения б зависит от скорости кристаллизации и интенсивности протекания диффузионных процессов в жидкой фазе:
6 = £>ж/щР, (12.18)
где D* — коэффициент диффузии примеси в жидкости; окр — скорость кристаллизации.
Концентрационное переохлаждение 4 характеризуется протяженностью зоны Ь, максимальным значением АГшах и расстоянием m от фронта кристаллизации до участка максимального переохлаждения и возрастает с понижением градиента фактических температур grad 7ф = дТф/дх, а также с увеличением концентрации примеси перед фронтом кристаллизации. Концентрация примеси будет возрастать с увеличением скорости кристаллизации. Таким образом, в случае сварки концентрационное переохлаждение металла шва определяется режимом
сварки (градиентом температур и скоростью кристаллизации, зависящей от скорости сварки), условиями теплоотвода из сварочной ванны, составом сплава и его теплофизическими свойствами. Влияние градиента температур и скорости кристаллизации на концентрационное переохлаждение обобщает критерий концентрационного переохлаждения
ф = grad Гф/^Окр (12.19)
ТИПЫ ПЕРВИЧНОЙ СТРУКТУРЫ
ПРИ КРИСТАЛЛИЗАЦИИ
Под первичной структурой (субструктурой) понимают структуру металла, образующуюся в процессе первичной кристаллизации, т. е. при переходе расплавленного металла из жидкого в твердое состояние.
Вторичная структура образуется в результате физико-химических процессов и структурных превращений в твердом состоянии.
Тип первичной микроструктуры сплава зависит от формы роста кристаллов, определяемой видом фронта кристаллизации и характером концентрационного переохлаждения перед этим фронтом.
Рассмотрим три возможных случая кристаллизации сплава при различной протяженности зоны концентрационного переохлаждения Ь, и Ь3 (рис. 12.11), вызванной различными распределениями температуры в жидкой фазе 7фі, Тф2, Тф3 (критерии концентрационного переохлаждения соответственно Фь Ф2, Фз). Условием, определяющим характер роста кристалла и формирование первичной структуры, будет соотношение двух параметров: Ф и ACo/k (А—экспериментально определяемая постоянная для данного Со, зависящая от теплофизических свойств, k — коэффициент распределения). При малой протяженности зоны концентрационного переохлаждения Ь Ф] >
|
Рис 12 11 Влияние градиента тем пературы перед фронтом кристалли задии на концентрационное пере охлаждение |
> ACo/k. В этом случае будет образовываться ячеистая первичная структура (рис. 12.12, а). Эта структура состоит из ряда параллельных элементов, имеющих форму стержней и ориентированных в направлении кристаллизации. Стержни в поперечном сечении имеют форму шестиугольников. Верхняя свободная поверхность кристаллов, обладающих такой структурой, волнистая.
При средней протяженности зоны концентрационного переохлаждения Ь2, когда Ф2 « ACo/k, образуется ячеисто-дендритная
|
Рис 12 12 Типы первичной структуры |
первичная структура (рис. 12.12,6). Отдельная ячейка, оказавшись впереди своих соседей, начинает быстрее расти и развиваться. По мере развития этого процесса выступ превращается в иглу, на игле образуются ветви, а эти ветви, в свою очередь, служат основой для следующих ветвей. Образуется ветвистая дендритная структура.
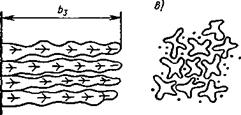
Если протяженность зоны концентрационного переохлаждения Ьз достаточно велика и переохлаждение больше некоторой критической величины, при которой еще происходит образование ячеистой структуры, то на всех ячейках начинают образовываться ветви и они превращаются в дендриты. Условием образования дендритной первичной структуры (рис. 12.12, в) будет Фз < ЛСо/fe. Дендриты сплавов имеют субструктуру, напоминающую ячеистую. Образование такой структуры на дендритах, растущих в расплаве, содержащем примеси, связано с тем, что растущая ветвь дендрита отталкивает атомы примеси так же, как и плоский фронт кристаллизации. Скопление примесей и концентрационное переохлаждение приводят к образованию ячеек на ветвях дендритов. С увеличением переохлаждения размеры дендритов и их разветвленность возрастают.
Таким образом, вероятность образования разветвленной дендритной структуры повышается с уменьшением градиента температуры grad Тф в жидкости перед фронтом кристаллизации, с увеличением скорости кристаллизации пкр и содержания примеси Со, а также с уменьшением коэффициента распределения примеси k.