Химические реакции при твердении цементов
При твердении цемента происходят реакции гидратации, гидролиза и обменного взаимодействия, протекающие при затворении цемента водой в жидкой фазе или па поверхности твердых частиц цемента. Большинство реакций сопровождается выделением тепла. Продукты реакции — твердые вещества либо квазитвердые, частично растворимы в воде и образуются в условиях постоянного уменьшения массы воды в процессе твердения.
Изучение химических реакций, протекающих при взаимодействии заводского цементного клинкера с водой, связано с большими трудностями. Клинкер состоит из минералов, в различной степени модифицированных твердыми растворами, застывшей жидкой фазы, стекла и т. п., и поэтому условия его твердения иные, чем у отдельных синтезированных в лабораторных условиях минералов. Кроме того, вода в процессе взаимодействия с цементом насыщается переходящими в раствор известью, гипсом и щелочами, наличие и концентрация которых в жидкой фазе твердеющего цемента существенно влияет на состав гидратных новообразований. При этом наблюдается взаимовлияние отдельных реакций, происходящих при твердении.
При гидратации индивидуальных синтетических минералов — силикатов кальция было установлено, что реакция C3S с водой приводит к образованию C3S2HX, на пограничной поверхности возникает пленка толщиной в несколько молекул. При комнатной температуре реакция C3S с водой стехиометрически описывается уравнением:
2(3 Ca0-Si02) +6н0о = 3Ca0-2Si0A-3H,0 + ЗСа(ОН)2.
При гидратации портландцемента в нормальных условиях образующиеся гидросиликаты кальция имеют переменный состав, в значительной степени близки к аморфным веществам и не образуют полной кристаллической структуры, которая возникает при твердении цемента в условиях повышенных температуры и давления. Они могут быть отнесены к полукристаллическим слабозакристаллизованным соединениям. К полукристаллическим слабозакристаллизованным относят также соединения, дающие на порошкограммах более трех линий, в которых отсутствует нормальный трехмерный порядок, характерный для кристаллических объектов.
Относительно хорошо образованные кристаллические гидросиликаты могут быть обозначены (по Тейлору): С —s — Н (I), если C/S = 0,8—1,5; С — S — Н (II), если C/S>1,5; в некоторых работах гидросиликаты С — S — Н (I) обозначаются С — S — Н (В), поскольку имеют тот же состав, но отличаются меньшей степенью закристаллизованности. Образующийся в цемент - Ном камне гидроксид кальция (СН) может быть отне-
Сен к веществам с полной кристаллической структурой, которую можно наблюдать в оптический микроскоп.
М. М. Сычев [138] рассматривает гидратацию клинкерных минералов как процесс, при котором происходит разрыв ионных связей между тетраэдрами Si04, мостиковыми ионами кальция и кислородом, в том числе разрыв более ковалентных связей Si — О в тетраэдрах. При этом связи Са—О—Si рвутся при про - тонизации, а связи Si — О — Si в результате комплек- сообразования с ОН - ионами и повышения координационного числа Si до 5—6 при более высоком значении рН.
Состав, структура и другие физико-химические характеристики гидросиликатов кальция (ГСК) изучались Н. В. Беловым, Е. Н. Беловой, В. В. Тимашевым, М. М. Сычевым, X. Ф. У. Тейлором, Г. J1. Калоусеком [8, 135, 137, 138, 140]. Исследованиями в этой области занимались также В. В. Илюхин, В. А. Кузнецов, А. Н. Jlo - бачев, В. С. Бакшутов [34]. ГСК различаются по основности (Ca0:Si02), содержанию воды, характеру кристаллизации и другим показателям. Некоторые гид - рос'иликаты кальция синтезированы при различных температурах при атмосферном и повышенном давлении, другие встречаются в природе. Гидросиликаты кальция относятся к волластонитовой — ксонотлитовой, тобер - моритовой, гиролитовой группам; выделена также группа высокоосновных ГСК-
X. Ф. У. Тейлор отмечает, что С — S — Н-фаза не подобна тобермориту, а является гелем с характерной слабой закристаллизованностью [140]. По представлениям М. М. Сычева, образование С — S — Н-фазы является результатом перестройки слоя минерала,, откуда выщелочен избыточный кальций и через который происходит диффузия ионов Са2+ и ОН~ в сторону жидкости. Это положение теперь дополнено представлениями Тейлора о возможности существования промежуточного слоя под слоем новообразований и названного слоем Тейлора. Это гелеобразиый слой с низкой основностью, чем, видимо, объясняется наличие внешних и внутренних продуктов гидратации, различающихся по основности. В гелеподобном (квазитвердом) слое Тейлора выделяют зоны реакции растворения, гидро - ксилирования и растворения на границе раздела слоя Тейлора и водной среды. Состав и морфология фазы
С — S — Н, образующейся в пространстве, занятом вначале соответственно цементным зерном и водой, различны во внешних и внутренних частях зерна.
Как «внутренний» продукт, так и «внешний», содержащий больше Са2+, образуются вследствие хемо - сорбции ионов Са++ наружной или внутренней поверхностью слоя Тейлора. Количество «внешнего» С — S — Н крайне мало по сравнению с содержанием «внутреннего» С — S — Н. Показано, что в первые минуты гидратации происходит конгруэнтное растворение минералов и затем осаждение из раствора С — S — Н - фазы на поверхности алита. Полагают также, что С — S — Н-фаза содержит большое количество примесных атомов; благодаря своей аморфности и чрезвычайно развитой удельной поверхности она отличается высокой диссоциативностыо.
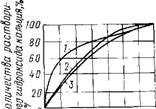
Поскольку жидкая фаза твердеющей системы (рис. 7) быстро и полно насыщается оксидом кальция, полагают, что вначале образуется гидросиликат кальция C2SH2, который по мере выделения извести в твердую фазу переходит в CSH(B) (рис. 8). Этому способствует также переход в раствор щелочей, снижающих в нем концентрацию извести. Гидратация |3-C2S в указанных выше условиях идет по приведенной выше схеме, но при меньшем выделении извести.
|
16 32 Hi И Время, сут |
|
98 112 |
|
Рис. 7. Скорость растворимости извести при гидратации силикатов кальция |
|
1— 3Ca0Si02; 2 — |5-2Ca0-Si02; 3 — V-Ca0-Si02 |
Под электронным микроскопом внешний слой С—S—Н-фазы имеет вид рыхлой фольги или весьма тонких волокон, порядка нескольких молекулярных слоев (рис. 9, 10). Удельная поверхность их довольно высока и в зависимости от степени слипания составляет примерно 250—350 м2/г. Можно заметить в этом сходство с некоторыми глинистыми минералами. Способность к обратимой отдаче воды указывает па то, что вода находится между слоями кристаллической решетки, плотность которой в зависимости от содержания воды может меняться. Считают, что это одна из важнейших Причин, от которых зависят многие строительно-тех-
|
Рис. 9. Электронная стереомикро - фотография реплики с поверхности скола камня C^S, гидратироваино- го 7 сут (по данным J] Шпыно - вой) |
|
Рис. 10. Электронная стереомикро - фотография с поверхности камня Сз5, гидратированного 6 лет (по данным Л. Шпыновой) |
|
Рис. 11. Электронная стереомикро - фэтография реплики с поверхности камня С А, гидратированного 6 мес (по данным Л. Шпыновой) |
Нические свойства портландцемента и, в частности, ус'адка и набухание.
Гидратация Са3А с водой протекает с большой скоростью при значительном выделении тепла. Вначале при температуре до 25°С образуется C3AHU_12 в виде гексагональных пластинок. Однако считают, что это соединение является гетерогенной эквимолекулярной смесью С4АН12 и C2AHg.
Гидроалюминаты общего состава С4АНХ в зависимости от температуры и влажности среды могут иметь следующее содержание воды: С4АН19—С4АН13—С4АНИ— С4АН7. По мере повышения температуры гексагональные гидроалюминаты кальция оказываются неустойчивыми и постепенно превращаются в стабильные кубические кристаллы С3АН6. При затворении С3А ледяной водой и охлаждении твердеющей системы образуется С4АН13 и АН3. При температуре затворения 21°С реакция протекает по схеме:
3 СаО - А1203 - г 6 НгО = ЗСа0-А1208-6Н,0
С3АН6 является единственным устойчивым соединением из всех гидроалюминатов кальция. Другие гидроалюминаты кальция медленно при нормальной температуре и весьма быстро при повышенных температурах переходят в кубические кристаллы С3АН6 (рис. 11). Такая перекристаллизация влияет на структуру и соответственно на прочность цементного камня; при высоком содержании в нем гидроалюминатов кальция возможно значительнее снижение прочности.
При гидратации С3А в присутствии некоторых соединений не исключено появление комплексных новообразований:
3 СаО-AJ203-3 CaS04-3J Н20, 3 СаО ■ А1203 ■ CaS04 ■ 12 Н20, 3 СаО - AJ203-CaCJ2- (10 — 12) Н,0, ЗСа0-А1203-Са (N03)2-ЮН20, 3 СаО - А1203 (Са, Mg)C03- JIH20.
С4АН13 можно рассматривать также как ЗСаО - •А1203-Са(0Н)2 - 12Н20.
Гидратация алюмоферритов кальция исследована применительно к наиболее часто встречающемуся в клинкере C4AF; его гидратация также зависит от температуры среды и содержания в растворе извести. В условиях гидратации портландцемента, т. е. насыщенного известью раствора при нормальной температуре, взаимодействие его с водой стехиометрически описывается следующим уравнением:
4 CaO-Al203-Fe203 + 2 Са (ОН)2 + 10 Н20 =
= ЗСа0-А1203-6На0 + 3Ca0-Fe203-6H20.
В результате образуются весьма устойчивые смешанные кристаллы С3(А, F)H6. При низкой температуре, примерно около 0°С, в насыщенном известью растворе образуется С4(А, F) Н13, гексагональные кристаллы кото рого также постепенно переходят в С3(А, F)Hg. Важным свойством алюмоферритов кальция является способность образовывать при гидратации ряд твердых растворов между гидроферритами и гидроалюминатами кальция, что благоприятно влияет, в частности, на коррозиеустойчивость портландцемента.
Гидратация содержащихся в клинкере свободной извести, а также периклаза (несвязанной MgO) протекает медленно с образованием гидроксида кальция и бру-' сита — Mg(OH)2. При крупных кристаллах свободной извести или периклаза становится особо заметным увеличение объема этих гидратных новообразований, что может вызвать существенные напряжения в цементном камне, нарушающие его структуру. Допустимое содержание СаОсвоб в нормально обожженном клинкере не должно превышать 1% ив отдельных случаях при тонком измельчении цемента — 2%. Валовое содержание оксида магния в клинкере ограничено по ГОСТ — 5%.
При взаимодействии с водой щелочных соединений силиката и алюмината кальция (К20-23Са0- 12Si02 и Na20-8Ca0-ЗА1203) щелочи переходят в раствор. Гидратация клинкерной жидкости, застывшей при охлаждении в стекловидном состоянии, приводит к образованию твердых растворов вида С3(А, F)H6. В их составе в качестве изоморфных компонентов находятся силикатные образования типа природных минералов группы гранатов — c3fs3 и СзАБз, в которых произошло замещение 6Н20 на 3Si02. Образующиеся при этом гидратные соединения называются гидрогранатами (рис. 12) и имеют состав ЗСаО(А1, Fe)203-Si02(6— —2х)Н20, причем при нормальной температуре «*»' может быть равен 0,5—0,7,
|
|
|
Рис. 12. Кристаллы гидрогранатов |
|
««W 6f<« ° ^ о| |
Рис. 13, Кристаллы Гидросульфоалюмина - та кальция
Сульфат кальция (гипс), вводимый в портландцемент при его помоле для регулирования сроков схватывания, при затворснии портландцемента водой переходит в раствор и в процессе гидратации образует (рис. 13) гидросульфоалюминат кальция ЗСаО - Al203-3CaS04- •31Н20. Известен также моносульфогидроалюминат кальция ЗСа0-А1203^3504-121^20. Первое соединение по структуре кристаллов и оптической характеристике соответствует природному минералу эттрингиту. Высокосульфатная его форма имеет игольчатую структуру кристаллов, часто в виде сферолитов, — низкосульфатная характеризуется гексагональными пластинками, которые также могут иметь вид сферолитов [75].
В насыщенном растворе гипса и извести вначале образуется высокосульфатная форма гидросульфоалюмина - та кальция; после израсходования всего гипса по мнению ряда ученых начинает появляться низкосульфатная форма. Ее считают также твердым раствором гипса с ЗСа0-А1203-Са(0Н)2-12Н20(С4АН13). Однако эта точка зрения встречает возражения. Гидросульфоалюминат кальция устойчив при определенной концентрации извести глинозема и серного ангидрида. Несмотря на существование природного эттрингита, что свидетельствует об устойчивости, многие экспериментальные данные указывают на возможность его поверхностного разложения под действием углекислоты; его метастабильность проявляется при повышении температуры примерно до 363 к.
В цементном камне образуется также гидросульфофер - рит кальция — 3Ca0-Fe203-3CaS04-31H20, а также его твердый раствор состава ЗСаО-(А1, Fe)203-3CaS04- •31Н20. При гидратации цемента эти соединения возникают очень быстро, причем играют большую роль в процессах формирования цементного камня. В. В. Ти - машев отмечает, что скорость реакции гидратации цемента зависит от скорости диффузии молекул воды и Растворенных ионов через слой продуктов реакции, располагающихся в виде оболочки на негидратированной поверхности частиц. Для определения скорости гидратации пользуются различными уравнениями [20].