Основы производства растворимых порошков
В своем применении проходят стадию получения жидкого стекла, т. е. стадию растворения. Вопросы, связанные с непосредственным применением сухих безводных силикатов натрия (молотая силикат-глыба), главным образом в качестве связующих для изготовления строительных изделий и жаростойких бетонов, изложены в монографии [57].
Как известно, отношение к растворению в воде силикат-глыбы при обычных условиях сильно меняется с возрастанием модуля - Высокощелочные силикаты, соответствующие ортосиликату 2Na20-Si02, хорошо кристаллизуются при охлаждении расплавов и не образуют стекол. Кристаллы ортосиликата натрия обладают островной структурой по кремнезему и не имеют силоксановЫ" связей. При взаимодействии с водой высокая щелочность в реакционной зоне препятствует образованию полимерных ионов, поэтому ортосиликат натрия растворяется практически конгруэнтно, очень легко. Образующийся раствор слишком низкого модУ-"*[3] аходит ограниченное техническое применение. Порошок во влаж - оМ воздухе хорошо поглощает СОг из атмосферы. Используется, к добавка к более высокомодульным системам.
Большее применение находит силикат натрия 3Na20-2Si02 модулем 2/3. Он производится в безводной форме кристаллизацией в массе расплава соответствующего состава при охлаждении.
Наибольшем количестве выпускается безводный метасиликат [атрия. Более щелочные силикаты, чем ЫагЭЮз, получают сплав - [ением дешевого метасиликата с соответствующей щелочью. Это асается и ортосиликата и 3Na20-2Si02. Все три силиката раство - яются в воде, хотя скорость растворения с возрастанием мо- уля падает. Механизм растворения, по всей вероятности, явится общим для всех силикатов. В зависимости от содержания [елочи меняется роль отдельных стадий. Растворение, естествен - 1о, сопровождается более или менее глубоким гидролизом силикат - ых ионов в зависимости от количества взятой воды. Скорость гид-
Юнцентрации силиката. Из образовавшихся растворов могут быть ыделены те или иные кристаллические гидросиликаты с помощью атравок в соответствии с фазовой диаграммой при той или той температуре. Легче всего выделяются гидросиликаты <a3HSi04- ГСН26 при растворении ортосиликатов натрия или Na20-2Si02. Процесс растворения протекает по схеме набухания гвердой фазы, сопровождающегося химическими реакциями, как
Обнаруживается. Поэтому производство в качестве товарных родуктов растворяющихся порошков безводных стекол или без - ;здных кристаллических силикатов с модулем выше 1 нецелесооб - азно. Все низкомодульные силикаты хорошо поглощают СОг влагу, способны слипаться и слеживаться при длительном хра - ении. При очень быстром охлаждении расплав метасиликата нат - 'ня способен застывать в виде стекла. Однако, по мнению Вейла '3], необходимые для этой операции усилия не оправдываются акими-либо существенными изменениями свойств продукта. Ди - "ликат натрия ИагБігОб, образующийся гидротермальным путем Ри температуре выше 200 °С из богатых кремнеземом растворов •ІИ медленным охлаждением расплавов соответствующего соста - а> не используется в качестве водорастворимого силиката. Напорот, в связи с очень малой скоростью его растворения в воде °3можно провести его отделение от метасиликата, который за ма - время растворяется полностью.
Все сказанное о высокощелочных силикатах натрия в основні •праведливо и для аналогичных силикатов калия. Укажем толы :іа главные отличия. Безводные силикаты калия практичесмq образуются только из расплава. При этом ортосиликат калия мо>|]2оЖНЫМИ силикатными но получить сплавлением более кремнеземистых силикатов с п' ташом, но нельзя со щелочью. Добавление даже небольших кол честв воды к расплавам калиевых силикатов очень резко, на соті градусов, понижает температуру их кристаллизации. Низкомі дульные, вплоть до метасиликата калия, кристаллические продуі ты и стекла отличаются высокой гигроскопичностью, болыш склонностью к гидролизу. При растворении в воде они не образуі насыщенных растворов, но способны гидролизоваться до выпад| ния аморфного кремнезема. Иногда говорят о растворимої метасиликата калия, имея в виду резкое понижение скорости пі рехода в раствор при достижении некоторого значения концентр; ции силикатов калия, величина которого зависит от температурі Дисиликат калия, в отличие от натриевого, растворяется в boj быстрее метасиликата.
|
Гидрату трехзамещенного ортосиликата Na3HSi04 • 2Н20. Крист^ лические гидросиликаты калия неустойчивы по отношению к |
Скорость растворения силикатов натрия с модулем до 1 во] растает при увеличении в них содержания воды, т. е. если э' кислые ортосиликат натрия и их кристаллогидраты. Наиболее легко растворим Na2H2SiOi4• 8Н20, ближняя гидратация ионов
Іедопустимо, или увеличением температуры процесса выше 100 °С, в нем почти завершена межионные взаимодействия в кристалли-!Г0 для ВОДНых систем приводит к техническим осложнениям, ческой решетке слабы. Однако он настолько уже обводнен (массо - Полностью избавиться от силоксановых связей в твердой фазе
Вая доля воды составляет что имеет слишком низкую теи-птем образования гидратов ортосиликатов натрия можно только пературу плавления. Плавясь при 48 С, он не восстанавливает ' мо я 2. Однозамещенный ортосиликат натрия NaH3Si04 об- кристаллическои структуры после охлаждения. По этим причинам изуегся при осторожном обезвоживании кристаллогидратов дву - производят менее водный кристаллогидрат двузамещенного орто - аме1ценного ортосиликата Na2H2Si04-8H20 или Na2H2Si04-4H20. силиката натрия Na2H2Si04 • 4Н20, который часто называют пев-ц й помол в шаровой мельнице этих веществ со спиртами или тагидратом метасиликата. В нем в координационную связь иона ацетоном дает требуемый продукт. Из расплавов или растворов натрия с шестью атомами кислорода вступает не только кислород, дН0заме[ценный ортосиликат не кристаллизуется, так как высоко - молекул воды, но и кислород силикатных ионов. Это повышает 10д ые системы содержат в значительной концентрации полипрочность кристаллическои решетки, увеличивает температуру, ликатные ионы и ПОЛучить достаточную концентрацию ионов плавления до 72 °С и понижает давление насыщенного пар^;ного вида^ в данном случае H3SiOr, не удается. Стабилен при 25 °С до 10 мм рт. ст. Последнее делает кристаллы более устои - 3|aj. j gjQ д0 50 60 °С
Чивыми к выветриванию на воздухе. Прозрачные кристаллы * * известный способ увеличения скорости растворения Na2H2Si04-4H20 на воздухе быстро мутнеют, поглощая углеки ■ ых стеклообразных силикатов заключается в их
Лыи газ. При нагревании выше температуры плавления они пост ■ Ид ци[[ Умеренн0 г„драТированные стекла сохраняют хруп - пенно теряют воду, превращаясь в объемистую пористую массу, Г)сть и могут быть приготовлены в виде порошков. уже отмеча - хорошо растворимую в воде. )сь чт0 силикаты щелочных металлов смешиваются с водой,
Получают пентагидрат метасиликата упариванием одном®' принципе в самых разных соотношениях. Основная трудность дульных водных растворов до состава, соответствующего крис .аключается в гомогенизации системы. Уже при грануляции без- таллогидрату, с последующим охлаждением. Образовавшую ;0дных силикатов охлаждеНием расплавов в проточной воде на кристаллическую массу дробят. Силикат натрия с модулем М оВерхности гранул обра3уется частично гидратированный слой, в некоторых странах также производят кристаллизациеи в ма « , ТОлщина ег0 невелика.
В виде кристаллогидрата 3Na20 • 2Si02 • 5Н20, что отвечает Д» Поглощение влаги расплавами при атмосферном давлении
Незначительно. Для удержания влаги в расплаве тре-
0Оде :?сьма
|
176 |
|
12 |
|
177 |
|
Заказ 23 |
'■Ются высокие давления.
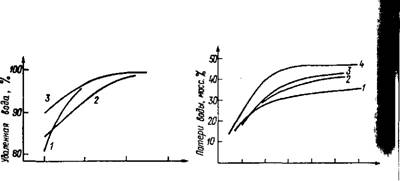
Рис. 67. Равновесные потери воды при сушке пленок силиката натрия в зависимости
От температуры [11] Модуль раствора: 1 — 2,9; 2 — 3,22; 3 — 3,75
Рис. 68. Кинетика сушки силикатных растворов в пленке прн 25 °С и относительной
Влажности 52% [11] / — Si02/Na20=2,9; 2 — Si02/Na20=3,22; 3 — 30% натриевого силиката 3,22+70% калиевого силиката 2,1; 4 — Si02/Na20=3,75
На рис. 67 приведены равновесные потери влаги силикатами натрия разных модулей при различных температурах, когда сушка производилась в пленке при атмосферном давлении. Уже при 500 °С вода практически не удерживается твердой фазой. Поэтому если расплав насыщался парами воды под давлением, а затем давление было снято при недостаточно охлажденном затвердевшем силикате, то он взрывается, освобождаясь от влаги, не соот ветствующей его равновесию при данной температуре. Термограм мы гидратированных стекол силиката натрия с модулем 3, содер жащих чуть меньше моля воды на моль кремнезема, показывают что стекла теряют основное количество влаги в диапазоне темпе ратур 130—150 °С [28]. Это означает, что давление пара над гид ратированным силикатом превысило атмосферное давление в этом диапазоне температур. По утверждению Вейла, насыщенным па ром 5 атм, температура которого около 150 °С, можно гидратиро - вать стеклообразные силикаты натрия; при этом образуются сухие хрупкие продукты гидратации. Сколько-нибудь существенно уве личивать давление насыщенного пара, повышая температуру пр° ведения процесса, нецелесообразно, а использование перегре того пара, очевидно, бессмысленно. Кинетика гидратации опреДе ляется также величиной поверхности раздела взаимодействуют^ - фаз, и скорость процесса будет замедляться по мере гидратации наружных слоев.
|
100 300 500 Температура, °С |
|
60 SO 120 ISO 180 Время, мин |
|
Рис. 68 |
|
Рис. 67 |
По данным [28], гидратация насыщенным паром при атмосферном давлении, т. е. при температуре 100 °С, порошке0 силиката натрия с модулем 3 и диаметром зерен 0,06 мм характе' ризуется величинами, приведенными в табл. 35.
Распределение влаги по глубине зерна при этом получается весьма неравномерным, хотя общее содержание воды достаточно велико. Наблюдения за процессами, происходящими в гидратиро - jaHHOM стекле, с помощью электронного микроскопа позволили отметить развитие кристаллизационных процессов [28]. Это свидетельствует о том, что спектр полисиликатных ионов в стекле сужался при гидратации и концентрация их отдельных видов повышалась, приводя к более упорядоченным системам. Известно, что при нагревании кристаллизационная вода теряется кристаллогидратами и гидратами в первую очередь, и только при более высоких температурах происходит дополнительная анионная поликонденсация и улетучивается вода из гидроксильных групп. Если этот процесс обратим, то при высоких температурах (выше 100 °С) с безводными силикатами может происходить обратная реакция: гидратационная вода идет в первую очередь на разрыв силоксановых связей. Тогда становится понятным развитие кристаллизационных процессов.
Стекла высокомодульных щелочных силикатов мало изменяют внешний вид, твердость, текучесть с увеличением содержания воды до 20%. Дальнейшее увеличение содержания гидратной воды понижает твердость, увеличивает эластичность гидратированных стекол и затем превращает их в густую вязкую массу. Поэтому увеличивать степень гидратации выше 20%, кроме специальных случаев, нецелесообразно. Эффект такой гидратации
|
Таблица 35. Зависимость степени гидратации стекла Na20-3Si02 паром при 100 °С от времени гидратации
|
Достаточно ощутим. Ниже приведены результаты опытов [13] по растворению безводных и гидратированных стекол в сопоставимых Условиях (гидратированные стекла содержат 17% Н20):
Нерастворимый остаток. %, при температуре 20 °С 100 °С
Безводное стекло Na20 • 2Si02 . . . Гидратированное стекло Na20-2Si02 Безводное стекло Na20-3Si02 . . . Гидратированное стекло Na20-3SiCb
Гидратация калиевых стекол с высоким модулем дает пример - "о такие же результаты. Однако наиболее легко растворимые высо - ^омодульные стекла получаются путем создания гидратированные полимеризации 10—100. При температуре ниже 80—90 °С потеря воды, видимо, не приводит к сколь-либо существенному образовав Нию силоксановых связей. Частицы коллоидного кремнезема и npoJ слойки частично обезвоженного раствора образуют общую стекловидную массу, сохраняющую структуру раствора. Распределение воды между коллоидными частицами и прослойками раствора' неравномерное. Прослойки гораздо более обводнены, чем коллоидные частицы, поэтому при растворении они переходят в жидкую фазу легко, а коллоидные частицы не изменяются существенно в процессе образования порошка и его последующего растворения. Иными словами, при низкотемпературной распылительной сушке полимерный состав раствора изменяется мало, вновь образующийся при растворении порошка раствор примерно воспроизводит исходный, и поэтому порошки сугубо аморфны. Использование вакуума при сушке более желательно, чем повышение температуры процесса.
На рис. 68 представлена кинетика сушки в пленке растворов силикатов натрия и калия разных модулей. Силикаты натрия легче теряют воду, чем силикаты калия. Особенно четко прослеживается зависимость скорости сушки от силикатного модуля. Чем модуль выше, тем легче сушка. Это указывает на то, что коллоидный кремнезем не удерживает воду в такой степени, как растворенный, и скорость сушки соответствует рассмотренной модели. Характерно, что высокомодульные растворы силикатов калия, не образующие каких-либо кристаллических соединений при температурах сушки, образуют такие же, как и натриевые, хорошо растворимые аморфные порошки, что указывает на сходство состояний силикатов в высушенных порошках. Практика показывает, что для сохранения способности порошков легко растворяться число молей воды, приходящихся на 1 моль силиката, с изменением модуля должно меняться. Чем выше силикатный модуль раствора, тем больше должно быть воды. Обычно в пределах модулей 2—3,7 число молей гидратной воды на 1 моль силиката находится в диа пазоне 2,5—4 для калиевых и натриевых систем.
Дах температурах, после чего проводился термогравиметрическии інализ и определялось количество щелочи и кремнезема, перешед - цих в раствор за то же время, что и в первом случае, и при тех же условиях. Результаты представлены в табл. 36.
Результаты растворения порошков, высушенных при 83 °С, шторы [55] считают подозрительными, хотя и воспроизводимыми, не находят им объяснения. Эндотермические минимумы на кри - !ых ДТА плавно смещались в сторону высоких температур с уве - шчением температуры сушки. Низкотемпературный минимум, на - шная с температуры 132 °С, был очень близок к температуре
|
Массовая доля |
|||
|
Температура сушки |
Воды, % |
Растворившейся щелочи |
Растворившегося кремнезема |
|
Таблица 36. Результаты сушки силиката натрия при разных температурах (59] |
СУшки, а второй минимум отличался от первого примерно на '00 °С. Рентгеновский анализ не обнаружил признаков кристалличности во всех полученных образцах, а ИК-спектры не дали *аких-либо характерных максимумов поглощения.
Работы по получению гидратированных растворимых высоко - }%ульных порошков были проведены в ЛТИ им. Ленсовета. еНтгеноаморфные порошки силиката натрия с модулем до 3,5 бы - 1к получены распылительной сушкой или сушкой в тонких слоях самым размеры сушильной камеры. Температура сохнущего мат риала на выходе сушилки, если содержание воды остается не ниже 17%, не поднимается выше 120 °С. Растворение порошков пр комнатной температуре при массовом отношении порошка и воді 1:3 дает жидкие стекла, по свойствам не отличающиеся от жидки$ стекол, полученных в производственных условиях растворениец силикат-глыбы.
Растворы силикатов калия при сушке требуют гораздо более осторожного обращения. Увеличение температуры до 90—100 при сушке в массе или в пленке приводит к образований гидрата тетрасиликата калия К2О • 4Si02 • Н20 (KHS12O5), что №дентифи - цируется рентгеноструктурным анализом. Эto соединение плох<| растворимо в воде, и порошок силиката калия образует молочного цвета суспензии. Количество KHSi2Os в порошке, полученном при высокой температуре, может достигать половины общей массы. Технологические свойства жидкого стекла при этом в значительной степени утрачиваются. Низкотемпературная сушка в пленке н« приводит к образованию видимых кристаллов KHSi2Os, жидкое стекло, содержащее 25% Si02, может слегка опалесцировать, hq порошок рентгеноаморфен. Распылительная сушка растворов силиката калия характерна малым временем процесса, что позволяет увеличивать температуру воздуха в зоне сушки без заметного образования плохорастворимого гидрата тетрасиликата калия. Скорость растворения калиевых гидратированных порошков гораздо больше, чем натриевых того же самого модуля. Калиевые порошки могут быть получены в области модулей 2—3,5. Они отличаются высокой гигроскопичностью. Калиевые порошки, высушенные до более низкой влажности, чем 15—16% Н20, заметно снижают качество получаемых из них жидких стекол. Поэтому: усреднение состава порошков по влажности в производстве недопустимо.
Силикаты четвертичного аммония, как упоминалось, обладают высокой устойчивостью по отношению к любой агрегации, особенно силикаты тетраэтоксиаммония, которые практически при любых высоких модулях, вплоть до золей, сохраняют способность раствО' ряться в воде после высушивания. Вследствие дороговизны
|
Плот |
|||
|
Вещество |
Ность, |
Силикат |
Способ производстве |
|
Г/см3 |
|
Кристаллические порошки силикатов, выпускаемые в США |
|
SiOj Ma20 2SiOj ' |
|
2,5 Ортосиликат натрия Силикат натрия с ыоду- Лем 0,66 |
|
Сплавление метасиликата натрия с каустической содой Охлаждение расплава Кристаллизация раствора стехиометрического состава при 72 °С |
Таблица 38. Порошки безводных стекол, выпускаемые в США
Текучесть (вязкость <105Па> при T, "С
3,22
|
Размягчение (вязкость <4- Ю'Пв) При /, °С |
|
Силикатный модуль |
|
Si02, % |
|
SiO; R20 • |
|
Силикат |
|
% |
|
Na Na К |
|
3,30 2,04 3,92 |
|
75,7 66,0 70,7 |
|
655 590 700 |
|
840 760 905 |
|
В заключение приведем, по данным [11], перечень коммер - іеских растворимых силикатов, производимых в США (табл. 37— Выпускаемый ранее гидратированный силикат натрия произ - •одился по ТУ 6-18-161—82 под названием «метасиликат натрия». Он отвечает формуле Na2Si03-9H20 и представляет собой мелкокристаллический порошок белого цвета с серым оттенком, плавит - (я при температуре 40—80 °С, легко растворим в воде. Массовая ^ля Na20 (общая щелочность в пересчете на Na20) в таком силикаты четвертичного аммония используют для создания вые"-іродукте составляет не менее 20,5; Si02 — более 19,0; Na2C03 комодульных порошков, относящихся к полисиликатам, где удель-'в пересчете на С02) —не более 1,2; полуторных оксидов ный вес органической составляющей невелик. '^ЬОз+РегОз) — не более 0,2. Общая влажность метасиликата Силикатам четвертичного аммония противопоказана высок"'іатрия не должна превышать 59%. Основная область применения температурная сушка, главным образом по причине их термИ" ;акого метасиликата натрия — производство синтетических мою - ческой неустойчивости. рИх средств. |
2,00 2,50
|
Таблица 39, Гидратированиые аыорфные порошки силикатов, выпускаемые в США
|