ОСНОВЫ АГЛОМЕРАЦИИ. ЖЕЛЕЗНЫХ РУД
Второй этап физико-химических превращений
Процессы второго этапа характеризуются высокой температурой и одновременным участием в реакциях твердой, жидкой и газообразной фаз.
Полученные в первом этапе процесса магнетит и твердый раствор магнетита в закиси железа служат начальной основой для образования жидких фаз.
Закись железа дает легкоплавкие соединения с Si02, из которых наибольшее значение для образования агломерата имеет фаялит-ортосиликат закиси железа 2FeO-Si02 с температурой плавления 1205° и две эвтектики с температурой плавления 1177—1178°. Кроме того, фаялит дает эвтектики с FeO и Si02. По исследованиям проф. Б. П. Селиванова, эвтектика с FeO содержит 73% FeO и 27% Si02 и имеет температуру плавления 1225°, а эвтектика фаялит—Si02 содержит 58% FeO и 42% Si02 н имеет температуру плавления 1130°.
Диаграмма плавкости системы FeO — Si02 представлена на рис. 38. Избыток окислов железа при охлаждении сплава (правая часть диаграммы) выпадает в виде вюстита. В левой части, до 1470°, из расплава выделяется кремнезем в виде кристобали - та, вследствие чего сплав обогащается закисью железа. Ниже 1470° кристобалит переходит в тридимит.
При образовании тройных сплавов FeO-Si02-CaO начальная температура плавления шихты значительно понижается.
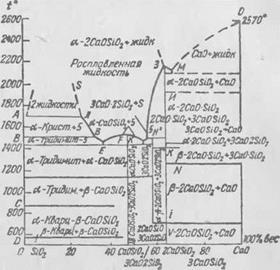
Наиболее низкую температуру плавления — около 1030° — имеет сплав с содержанием СаО, близким к 10%). — это почти на 200° ниже температуры плавления фаялита. Системы СаО — Si02 (рис. 39) и СаО—FeO—Si02 (рис. 40) представляет наибольший интерес для изучения превращений, происходящих при металлургических процессах.
Два компонента системы СаО и Si02 образуют соединения с температурой плавления: CaO-Si02—1544°; 2Ca0-Si02—
2130°; 3Ca0-2Si02— 1478°; соединение 3Ca0-Si02 образуется в твердой фазе при 1900°.
Система дает три эвтектики: (Si02+'CaO • Si02)—с температурой плавления 1438°; (СаО • Si02+3Ca0 • 2Si02)—с температурой плавления 1457° и (а 2СаО - Si02-HCaO)—с температурой плавления 2065°.
Большой интерес для агломерации представляет двухкальциевый силикат (Ca2Si04), существующий в трех модификациях а, Р, у. Температура плавления а-модификации 2130°, точка перехода а—>-Р 1420°. Переход р-.модификации в у-модификацию происходит при 675° с увеличением объема до 10%, что сопровождается превращением силиката в порошок. Это свойство у - модификации серьезно препятствует получению стойкого, выдерживающего продолжительное хранение офлюсованного известкового агломерата.
Для получения устойчивого агломерата необходимо предотвратить образование силиката 2Ca0-Si02 обеспечением условий образования тройных сплавов, не подверженных распаду.
Система СаО—Si02—FeO исследована недостаточно вследст вие трудности постановки экспериментальных работ. Имеющиеся сведения по исследованию этой системы приводятся на диаграмме рис. 40.
|
|
|
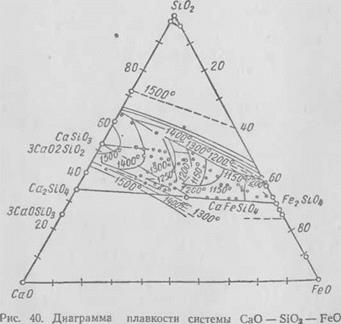
Система образует три известково-железистых силиката: мон - тичеллит СаО • FeO • SiCV, железистый окерманит 2CaO-FeO ■2Si02; метасиликаты: геденбергит СаО • FeO • 2Si02, однокальциевый силикат волластонит CaOSi02 и три ряда твердых растворов: два метасиликатных и один ортосиликатный. Твердые растворы ортосиликатов состоят из фаялита и монтичеллита. изменяясь в составе от чистого фаялита через монтичеллит Са FeO • Si02 до Ca2Si04.
Метасиликатные ряды твердых растворов волластонита включают в себя область от чистого волластонита (CaSi03) до 76% FeSi03; геденбергита — от собственно геденбергита до 80% FeSi03. Геденбергитовые твердые растворы при тем-пературах свыше 940—980° переходят в твердые растворы волластонита.
По исследованию Н. Константинова и Б. Селиванова, сплав с преобладающим количеством FeO ■ Si02 образует эвтектику, а при преобладании СаО ■ Si02 образуются однородные смешанные кристаллы. Наиболее низкая температура плавления (1030°) относится к сплаву с отношением Si02:FeO=l при содержании около 10% СаО.
Наблюдение за превращением модификации (J 2СаО • Si02 в форму у показывает, что наличие соединений железа до 45% не задерживает превращения, тогда как в системе Si02—А1203— СаО достаточно небольших количеств глинозема, чтобы задержать переход ортосиликата в у-форму.
Расплавы Si02—А1203—СаО склонны « образованию стекла, которое также препятствует переходу в у-модификацию.
Значительно понижается температура плавления при наличии в шихте А1203, т. е. в условиях образования оплава из четырех компонентов: FeO—Si02—СаО—А1203. Есть указания, что температура плавления эвтектического сплава при этом не превышает 1030—1050°.
Рассмотрение минеральных составляющих шихты позволяет наметить наиболее вероятные соединения между ними, являющиеся источником образования жидких фаз в условиях постепенно возрастающих температур.
Последовательность образования указанных соединений может быть и иной по сравнению с порядком расположения в табл. 23, за исключением образования твердого раствора Fe304 в FeO, который появляется до образования жидких фаз. Есть указания [9, 45], что при производстве офлюсованного агломерата при 1190—1230° образуются ферриты кальция; наиболее вероятно образование однокальциевого феррита СаО - Fe203.
По мере повышения температуры в химические реакции вовлекаются все большие массы твердых составляющих шихты и при определенных благоприятных условиях произойдет полное
|
Т а бли ца 23 Легкоплавкие соединения, образующиеся при агломерации руд
|
расплавление материала в зоне спекания. Оно может быть и не полным, например, при чрезмерно быстром перемещении зоны горения вследствие большой пористости шихты, при недостаточном расходе топлива, при наличии в шихте крупных кусков руды, успевающих прогреться до температур, обеспечивающих появление жидких фаз лишь на поверхности кусков и т. д. Отсюда понятна разница взглядов на природу агломерационного процесса, которая сводится к следующему: одни считают обязательным условием для агломерационного процесса полное сплавление руды и принимают, что все наблюдаемые в агломерате минералы являются минералами вторичного происхождения; по мнению других, руда в процессе спекания не претерпевает глубоких изменений, а происходит лишь поверхностное оплавление и склеивание зерен. Но, как видно из приведенного выше, при агломерации могут иметь место оба случая.
Обязательным условием для получения хорошего агломерата является образование жидких фаз. Количество последних зависит от состава руды, расхода топлива и воздушного режима процесса спекания.
По исследованиям проф. Б. П. Селиванова [46], влияние добавок Si02, AI2O3 и СаО на результаты спекания чистой окиси железа при нагревании в трубчатой печи дало следующие результаты. Нагрев чистой окиси железа от 1000 до 1100° сопровождается слабым уплотнением массы без признаков спекания. При 1200° имеет место заметное, однако непрочное спекание. Нагрев до 1300° вызывает полное спекание материала, но получающийся при этом агломерат имеет неудовлетворительную прочность.
Добавка к окиси железа 5% кремнекислота при 1100° обеспечивает прочное спекание. Увеличение содержания кремнезема до 10% не улучшает качества агломерата, а добазка его до 15% ухудшает качество агломерата. Кристаллическая окись кремния 9*
требует более высокой температуры для прочного спекания по сравнению с аморфной.
Спекание окиси железа с А1203 в количестве 5; 10 и 15% показало, что выше 1200° образуется агломерат небольшой прочности.
Ємесь из Fe203 и 5% СаО хорошо спекается уже при 1100°, а при 1200° сплавляется.
Действие окиси магния проявляется заметно при 10 и 15% добавки ее. В этих случаях заметное и прочное спекание наблюдается при 1200°.
Спекание Fe203 с МпО происходит вполне удовлетворительно при 1200°.
Проф. Б. П. Селиванов исследовал влияние водорода и углерода на качество спекания различных смесей, т. е. влияние газовой среды на результаты спекания.
Для смесей Fe203-Al203; Fe203-Ca0 и Fe203-MnO он отмечает отчетливое повышение прочности агломерата при спекании в восстановительной среде1 по сравнению со спеканием на воздухе. Водородная среда не отразилась на результатах спекания окиси железа с MgO.
В исследовании Гартмана [43] указывается, что в восстановительной среде спекание наступает при значительно более низких температурах по сравнению с обычной окислительной средой. Так, смесь СаО и Fe203, спекающаяся на воздухе при 660°, в атмосфере восстановителя размягчается уже при 520°, а смесь кремнезема и окиси железа размягчается с поверхности зерен при 390°. Начало спекания определяли изменением электропроводности. Гартман указывает на большое практическое значение восстановительной среды в промышленных условиях для повышения производительности агломерационных машин.
Сильнейшим плавнем для железной руды является окись кальция, один весовой процент который, по данным Б. П. Селиванова, образует четыре весовых процента жидкой фазы.
Температура образования железо-кальциевого силиката, по Селиванову, лежит в пределах 900—1000°.
Обстоятельный анализ условий образования жидких фаз при агломерации железных руд дал проф. С. Т. Ростовцев в своей работе по спеканию криворожских руд [6].
Исходя из того, что основными компонентами при агломерации являются Fe203 и Si02 как исходные и Fe304, FeO и Fe2Si04 как производные, С. Т. Ростовцев по содержанию Si02 в руде считает возможным определить приближенно степень развития жидких фаз в зоне спекания.
Расчеты, проведенные С. Т. Ростовцевым, .показали, что при агломерации руд, содержащих избыток кремнезема, повышенный расход топлива сопровождается подъемом температуры свыше 1400° и приводит к увеличению количества жидких фаз с 7,9 единиц до 14,3 единиц, т. е. почти вдвое, что резко изменяет и структуру агломерата.
При агломерации бртатых руд, содержащих мало кремнезема, развитие температур до 1500° также сопровождается почти удвоением жидких фаз, но общее количество их в три раза меньше, чем при спекании бедных руд при этой же температуре. Очевидно, что агломерат из богатых руд даже при избытке топлива будет иной структуры по сравнению с агломератом из руд, содержащих много кремнезема.