РЕНИЙ
Д. И. Менделеев в 1869 г. предсказал существование и свойства двух элементов VII группы - аналогов марганца, которые предварительно назвал "эка- марганец" и "дви-марганец". Они соответствуют известным в настоящее время элементам - технецию (порядковый номер 43) и рению (порядковый номер 75).
В последующие 53 года многие исследователи сообщали об открытии аналогов марганца, но без убедительных оснований. Теперь мы знаем, что поиски элемента №43 в природных соединениях не могли увенчаться успехом, так как он неустойчив. Лишь в 1937 г. этот элемент был получен искусственно Э. Сегре и К. Пёрье путем бомбардировки ядер молибдена дейтронами я назван технецием (от греческого "техно" - искусственный).
В 1922 г. немецкие химики Вальтер и Ида Ноддаки начали систематические поиски аналогов марганца в различных минералах. Из 1 кг колумбита они выделили 0,2 г продукта, обогащенного молибденом, вольфрамом, рутением и осмием. В этом продукте по характеристическим рентгеновским спектрам был обнаружен элемент с порядковым номером 75. О своем открытии Ноддаки сообщили в 1925 г. и назвали элемент рением. Позже, в 1927 г., Ноддаки установили, что в значительных концентрациях (до сотых долей процента) рений содержится в молибдените, из которого элемент был выделен в количествах, позволивших изучить химические свойства его соединений и получить металл.
Производство рения и его соединений в небольших количествах впервые воз - никло в Германии в 1930 г. на Мансфельдском заводе, где рений извлекали из печных настылей, образующихся при плавке медистых сланцев, содержащих примесь молибденита. В СССР производство рения возникло в 1948 г.
Свойства рения
Рений - тугоплавкий тяжелый металл, по внешнему виду похож на сталь. Некоторые физические свойства рения приведены ниже:
Атомный номер 75
Атомная масса 186,31
Тип и периоды решетки. . . . Гексагональная,
Плотноупакованная а = 0,276, с = 0,445 нм
TOC \o "1-3" \h \z Плотность, г/см3 21,0
Температура, °С:
Плавления ........ 3180±20
Кипения ~5900
Удельная теплоемкость средняя при
0-1200 °С, Дж/(г' °С) .... 0,153
Удельное электросопротивление
Р *10«, ОМ'см 19,8
О
20 С
Температура перехода в состояние
Сверхпроводимости, К. . . . 1,7
Работа выхода электронов, зВ 4,8 Сечение захвата тепловых нейтронов
П' 1024, см2 85
Твердость НВ отожженного металла, МПа 2000 Временное сопротивление (кованые и
Затем отожженные прутки) бв, МПа 1155
Модуль упругости Е, ГПа. . . 470
По температуре плавления рений занимает второе место среди металлов, уступая лишь вольфраму, а по плотности - четвертое (после осмия, иридия и платины). Удельное электросопротивление рения почти в 4 раза выше, чем вольфрама и молибдена.
В отличие от вольфрама рений пластичен в литом и рекристаллизованном состоянии и можеть быть деформирован на холоду. Вследствие высокого модуля упругости после небольшой деформации твердость рения сильно возрастает - проявляется сильный наклеп. Однако после отжига в защитной среде или в вакууме металл вновь приобретает пластичность.
Изделия из рения (в отличие от изделий из вольфрама) выдерживают многократные нагревы и охлаждения без потери прочности. Сварные швы нехрупкие. Прочность рения до 1200 °С выше, чем вольфрама, и значительно превосходит прочность молибдена.
Рений устойчив на воздухе при обычной температуре. Заметное окисление металла начинается при 300 °С и интенсивно протекает выше 600 ос с образованием высшего оксида Re207.
С водородом и азотом рений не реагирует вплоть до температуры плавления и не образует карбидон. Эвтектика в системе рений - углерод плавится при 2480 °С.
С фтором и хлором рений реагирует при нагревании, с бромом и иодом практически не взаимодействует. Рений устойчив в соляной и плавиковой кислотах
На холоду и при нагревании. В азотной кислоте, горячей концентрированной серной кислоте и перекиси водорода металл растворяется.
Рений стоек против действия расплавленных олова, цинка, серебра и меди, слегка разъедается алюминием н легко растворяется в жидких железе н никеле.
С тугонлавкимн металлами (вольфрамом, молибдене»!, танталом и ниобием) рений образует твердые растворы с предельным содержанием рения 30-50 % (по массе).
Свойства химических соединений
Наиболее характерны и устойчивы соединения рения высшей степени +7. Кроме того, известны соединения, отвечающие степеням окисления 6;5;4;3;2;1; а также -1.
Оксиды. Рений образует три устойчивых оксида: рениевый ангидрид, триоксид и диоксид.
Рениевый ангидрид Re207 образуется при окислении ренияокислородом. Цвет — светло-желтый, плавится при 297 °С, точка кипения 363 С. Растворяется в воде с образованием рениевой кислоты HRe04.
Триоксид рения Re03 - твердое вещество оранжево-красного цвета, образуется при неполном окислении порошка рения. В воде и разбавленных соляной и серной кислотах малорастворим. При температурах выше 400 °С обладает заметной летучестью.
Диоксид рения Re02 темно-бурое твердое вещество, получается восстановлением RejO; водородом при 300 °С. Диоксид нерастворим в воде, разбавленных соляной и серной кислотах. При нагревании в вакууме (выше 750 °С) диспро - порционирует с образованием Re207 и рения.
Рениевая кислота и ее соли - перреиаты. Рениевая кислота - сильная одноосновная кислота. В отличие от марганцевой кислоты, HRe04 — слабый окислитель. При взаимодействии с оксидами, карбонатами, щелочами она образует перренаты. К малорастворимым в воде относятся перренаты калия, таллия и рубидия, умеренно растворимы перренаты аммония и меди, хорошо растворимы в воде перреваты натрия, магния, кальция.
Хлориды рения. Наиболее изучены хлориды ReCl3 и ReCl3. Пентахлорид рения образуется при действии хлора на металлический рений при температуре выше 400 °С. Вещество темно-коричневого цвета. Плавится при 260 °С, точка кипения 330 °С. В воде разлагается с образованием HRe04 и Re02'xH20.
Трихлорид ReCl3 - красно-черное вещество, получается в результате термической диссоциации ReCl5 при температуре выше 200 °С. Температура плавЛения 730 °С, возгоняется при 500-550 °С
Известны два оксихлорида: ReOCl4 (температура плавления 30 °С, кипения 228 °С) и ReOjCl (жидкость, кипит при 130 °С).
Сульфиды рения. Известны два сульфида - RejS? и ReS2. Высший сульфид - темно-бурое вещество, осаждается сероводородом из кислых и щелочных растворов. Дисульфид рения ReS2 получается термическим разложением Re2Sy (выше 300 °С) или прямым взаимодействием рения с серой нри 850-1000 °С. ReS2 кристаллизуется в слоистой решетке, идентичной с решеткой молибденита. На воздухе при температуре выше 300 °С окисляется с образованием Re207.
Области применения рения
В настоящее время определились следующие эффективные области применения рения.
8-1325
Катализаторы. Рений и его соединения входят в состав катализаторов для ряда процессов в химической и нефтяной промышленности. Это наиболее масшатабная область применения рения. Наибольшее значение приобрели рений-содержащие катализаторы в крекинге нефти. Применение рениевых катализаторов позволило увеличить производительность установок, повысить выход легких фракций бензина, снизить зат-. раты на катализаторы путем замены большей части платины рением.
Электроосветительная и электровакуумная техника. В ряде ответственных случаев, когда необходимо обеспечить долговечность работы электроламп и электронных приборов (особенно в условиях динамической нагрузки), в этой области вместо вольфрама применяют рений или сплавы рения с вольфрамом и молибденом. Преимущества рения и его сплавов перед вольфрамом состоят в лучших прочностных характеристиках и сохранении пластичности в рекристаллизованном состоянии, меньшей склонности к испарению в вакууме в присутствии следов влаги (сопротивление водородно-водяному циклу), более высоком электросопротивлении. Из рения и сплавов вольфрама с рением (до 30% Re) изготовляют нити накала, керны катодов и подогревателей, сетки радиоламп. В электронных приборах используют также сплав Мо-50% Re, сочетающий высокую прочность с пластичностью.
Жаропрочные сплавы — одно из важных направлений использования рения. Сплавы рения с другими тугоплавкими металлами (вольфрамом, молибденом и танталом) наряду с жаропрочностью и тугоплавкостью отличаются пластичностю. Их используют в авиа - и космической технике (детали термоионных двигателей, носовые насадки ракет, части ракетных сопел, лопатки газовых турбин и др.).
Сплавы для термопар. Рений и его сплавы с вольфрамом и молибденом обладают высокой и стабильной термоэлектродвижущей силой (т. э.д. с.). В СССР широко используют термопары из сплавов (W—5 % Re) - (W - 20% Re). Т. э.д. с. этой термопары в пределах 0-2500 °С находится в линейной зависимости от температуры. При 2000 °С т. э.д. с. равна 30 мВ. Преимущество термопары — сохранение пластичности после длительного нагревания при высокой температуре.
Электроконганкты. Рений и его сплавы с вольфрамом. отличаются высокими износостойкостью и сопротивлением эле - 226 ктрокоррозии в условиях образования электрической дуги. Они более стойки, чем вольфрам, при эксплуатации в тропических условиях. Испытания контактов из сплавов W - 15-%Re в регуляторах напряжения и приборах зажигания двигателей показали их преимущества перед вольфрамом.
Приборостроение. Рений и его сплавы, отличающиеся высокой твердостью и износостойкостью, используют для изготовления деталей различных приборов, например опор для весов, осей геодезической аппаратуры, шарнирных опор, пружин. Испытания работы плоских пружин из рения при температуре 800 °С и многократных циклах нагрева показали отсутствие остаточной деформации и сохранение начальной твердости.
Масштабы производства рения в зарубежных странах в 1986 г. находились на уровне 8 т/год. Основные производители - США и Чили, в 1986 г. в США использовано 6,4 т рения.
2. СЫРЬЕВЫЕ ИСТОЧНИКИ РЕНИЯ
Рений - типичный рассеянный элемент. Содержание его в земной коре низкое - 10 7 % (по массе). Повышенные концентрации рения, имеющие промышленное значение, наблюдаются в сульфидах меди и особенно в молибдените.
Связь рения с молибденом обусловлена изоморфизмом MoS2 и ReS2. Содержание рения в молибденитах различных месторождений составляет от Ю-1 до 10"5%. Более богаты рением молибдениты медно-молибденовых месторождений, в частности медно-порфировых руд. Так, молибденитовые концентраты, получаемые при обогащении медно-порфировых руд СССР, содержат 0,02-0,17 % рения. Значительные ресурсы рения сосредоточены в некоторых месторождениях меди, относящихся к типу медистых песчаников и медистых сланцев. К этому типу относятся руды Джезказганского месторождения СССР. Более богаты рением руды с повышенным содержанием борнита CuFeS4. В полученных флотацией медных концентратах содержится 0,002-0,003 % Re. Предполагают, что рений находится в них в виде тонкодисперсного минерала CuReS4 - джезказганита.
Поведение рения при переработке молибденитовых концентратов
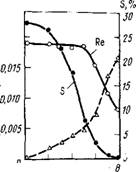
При окислительном обжиге молибденитовых концентратов, проводимом при 560-600 °С, содержащийся в концентрате рений образует оксид Re207, который уносится с газовым потоком (точка кипения Re207 363 °С). Степень возгонки рения зависит от условий обжига и минералогического состава концентрата. Так, при обжиге концентратов в многоподовых печах степень возгонки рения не выше 50-60 % Из рис.60
Рас.60. Изменение содержания серы, рения и степени окисления молибденита (пунктир) по подам восьмиподовой печи
Видно, что рений возгоняется с газами на 6-8 подах (при обжиге в 8-подовой печи), когда большая часть молибденита окислена. Это объясняется тем, что в присутствии MoS2 образуется малолетучий диоксид рения по реакции:
MoS2+2Re207 = 4Re02+ Mo02+2S02. (5.1)
Кроме того, неполный возгон рения может быть обусловлен частичным взаимодействием Re207 с кальцитом, а также оксидами железа и меди с образованием перренатов. Например, с кальцитом возможна реакция:
CaC03+Re207 = Ca(Re04)2+C02. (5.2)
Re, 7с
100 80
І
= 60 ? 40 20 О
Г 4 б
Номер пода
Советскими исследователями установлено, что наиболее полно рений возгоняется при обжиге молибденитовых концентратов в кипящем слое. Степень возгонки составляет 92-96 %. Это объясняется отсутствием при обжиге в печах
КС условий для образования низших оксидов рения и перре - натов. Эффективное улавливание рения из газовой фазы достигается в системах мокрого пылеулавливания, состоящих из скрубберов и мокрых электрофильтров. Рений в этом случае содержится в сернокислых растворах. Чтобы увеличить концентрацию рения, растворы многократно циркулируют. Из системы мокрого улавливания выводят растворы, содержащие, г/л: Re 0,2-0,8; Мо 5-12 и H2SO„ 80-150. Небольшая часть рения содержится в шламах.
В случае неполного возгона рения при обжиге концентрата рений, оставшийся в огарке, переходит в аммиачные или содовые растворы выщелачивания огарков и остается в маточных растворах после осаждения соединений молибдена.
При использовании вместо окислительного обжига разложения молибденита азотной кислотой (см. гл.1) рений переходит в азотно-сернокислые маточные растворы, которые содержат в зависимости от принятых режимов, г/л: H2S04 150-200; HN03 50-100; Мо 10-20; Re 0,02-0,1 (в зависимости от содержания в сырье).
Таким образом, источником получения рения при переработке молибденитовых концентратов могут служить сернокислые растворы мокрых систем пылеулавливания и маточные (сбросные) растворы после гидрометаллургической переработки огарков, а также азотно-сернокислые маточные растворы от разложения молибденита азотной кислотой.
V
Поведение рения в производстве меди
При плавке медных концетратов в отражательных или руд - нотермических электропечах с газами летит до 75 % рения, при продувке штейна в конвертерах весь содержащийся в них рений удаляется с газами. Если печные и конвертерные газы, содержащие SOz, направляются в производство серной кислоты, то рений концентрируется в промывной циркулирующей серной кислоте электрофильтров. В промывную кислоту переходит 45-80% рения, содержащегося в медных концентратах. Промывная кислота содержит 0,1-0,5 г/л рения и ~500г/л H2S04, а также примеси меди, цинка, железа, мышьяка и др. и служит основным источником получения рения при переработке медных концентратов.