Температура
Поскольку можно говорить о кинетике процесса агрегации, то уместно ожидать, что скорость гелеобразования возрастает с повышением температуры. Это не всегда имеет место в процессе флокуляцйи, когда образуются водородные связи с органическими молекулами, но при гелеобразовании наблюдается заметный температурный коэффициент скорости формирования силоксановых мостиковых связей между частицами. Была измерена энергия активации процесса гелеобразования в поликремневой кислоте, но, однако, имеется мало данных по превращению золей с известными размерами частиц в гели. Ниже рН 2, когда скорость реакции пропорциональна концентрации водородных ионов (HF оказывает каталитическое действие), энергия активации составляет около 9,5 ккал/моль. Согласно данным Пеннера [226], при рН 4,5, когда реакция катализируется гидроксил-ионами, энергия равна 16,1 ккал/моль. Броде, Браун и Хофф [227] определили близкое значение, равное
15.5 ккал/моль, при рН 5,5. При рН 8,5 они обнаружили более низкое значение 9,6. ккал/моль, тогда как при рН 10,5 в присутствии хлорида калия энергия активации составила
14.6 ккал/моль. Очевидно, что температурный коэффициент скорости гелеобразования должен также зависеть от изменяющихся констант диссоциации рассматриваемых веществ по мере возрастания температуры. Ранее выполненные исследования по механизму гелеобразования были обобщены Айлером [8].
Во многих исследованиях гелеобразования поликремневой кислоты, состоящей из очень небольших частиц, интерпретация результатов измерения осложнялась тем фактом, что с ростом температуры частицы увеличивались в размере. Существенные данные, относящиеся к энергии активации процесса агрегации частиц, могут быть получены только в том случае, когда частицы уже закончили свой рост и стабилизированы при более высокой температуре, чем предусматривалось в проводимых экспериментах. Кроме того, энергия активации зависит не только от вели
чины рН, определяющей заряд на частицах, но также и от изменения концентраций кремнезема и электролита. Следовательно, бессмысленно приводить данные для энергии активации гелеобразования, если только подобные переменные величины точно не определены.
Для деионизированного золя с частицами размером 14 нм (значение рН устанавливалось добавлением NaOH) энергия активации подсчитывалась из времени гелеобразования при 23 и 60°С. Ее значения оказались следующими:
Концен"рацня Si02, %
20 30 20 30
Очевидно, что рассматриваемые факторы оказываются сложными.
Теория прочности гелей
Коллоидный кремнезем находит многочисленные применения благодаря тому, что после высушивания он необратимо превращается в нерастворимый кремнезем. Его пригодность к использованию в качестве загустителя и связующего для неорганических волокон и порошков зависит от прочности геля, формирующегося около точек контакта между макроскопическими частицами веществ, подлежащих связыванию.
Настоящее обсуждение вопроса ограничивается гелями, полученными из дискретных частиц коллоидного кремнезема размером более чем 5 нм в диаметре. Не-сделано никаких попыток рассмотрения огромной по объему совокупности литературных данных, относящихся к гелям, полученным из поликремневых кислот посредством подкисления растворимых силикатов щелочных металлов. В том случае, когда в процессе участвуют поликремневые кислоты или частицы диаметром менее 5 нм, процесс гелеобразования оказывается гораздо более сложным и предусматривает конденсацию силанольных групп внутри частиц и циклизацию с образованием трехмерных силоксановых колец, что приводит к формированию зародышевых безводных частиц Si02.
|
РН |
Энергия активации; |
|
Ккал/моль |
|
|
5,5 |
10,7 |
|
5,5 |
7,6 |
|
3,0 |
16,4 |
|
3,0 |
11,9 |
Томас и Мак-Коркл [228] сформулировали основные положения теории образования геля из коллоидных частиц. Они показали, что теория Фервея—Овербека, описывающая взаимодействие двойных электрических слоев, окружающих две соседние сферические коллоидные частицы, приводит к объяснению
явления изотропной флокуляции. Новые коллоидные частицы могут более легко присоединяться к концам цепеобразного флокулированного осадка, т. е. в тех местах, где минимален энергетический барьер, обусловленный силами отталкивания. Это как раз тот тип агрегации, благодаря которому золь превращается в гель только в определенных точках контакта частиц путем формирования бесконечной сетки из цепочек коллоидных частиц, распространяющейся по всему объему золя (см. также гл. 3).
Превращение золя в высушенный гель происходит по следующим стадиям:
А) затвердевание золя вплоть до образования трехмерной сетки геля, состоящей из разветвленных цепочек кремнезема, в которой жидкость удерживается капиллярными силами;
Б) упрочнение связей между соседними частицами в точках контакта за счет коалесценции частиц;
В) усадка трехмерной кремнеземной сетки по мере испарения воды;
Г) развитие напряжений в кремнеземной сетке в процессе объемной усадки;
Д) появление трещин в высушенном геле кремнезема и образование из него отдельных кусочков.
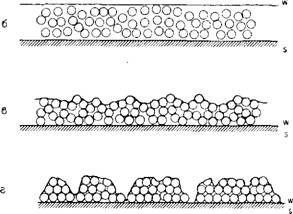
Как показано на рис. 4.15, усадка кремнеземного геля легко просматривается в том случае, когда тонкий слой золя высушивается на гладкой поверхности. На первом этапе формируется прозрачная, связанная с поверхностью пленка геля, а затем по мере высушивания пленка сжимается с разрывами, образующимися в направлении высушивания, так что получается непрочный волокнистый или похожий на волосы остаток кремнеземного геля. Частицы размером 100 нм могут образовывать ленточки геля шириной вплоть до 1 мм, а при использовании частиц еще большего размера остаются относительно большие тонкие пленки. Золь, состоящий из малых частиц, превращается в гель при более низкой концентрации кремнезема, и, следовательно, образовавшийся по мере испарения воды из пленки золя с данной концентрацией кремнезема гель сжимается более сильно и растрескивается на небольшие, относительно более твердые кусочки геля. Таким образом, получается некоторая определенная небольшая по толщине пленка геля, которая полностью покрывает поверхность - сплошным слоем. Хотя сам по себе золь кремнезема при высушивании может и не образовывать сплошной пленки, тем не менее он способен вести себя подобно прочному гелю и заполнять промежутки между большими по размеру частицами или волокнами. Подобным образом при нанесении на испытуемую подложку, например на поверхность стекла, золь с заданной концентрацией Si02
О о 0 о0 о о о o0g ООо0Оо
Oq? oo о о % оо°ооо00о ОО О О ОО О ОО о о
|
|
|
Рис. 4.15. Схема превращения испаряющейся пленки золя кремнезема в гель И высушивания геля (показано поперечное сечение системы). а — золь; б— начало агрегации частиц в концентрированном золе; в — сжатие геля под действием поверхностного натяжения; г — растрескивание геля в результате усадки; д — высушенные несвязанные между собой кусочки геля, w — поверхность воды, s — твердая Подложка. |
Может образовывать при высушивании хрупкое, не прилипающее к поверхности отложение относительно большой толщины, однако при высушивании очень тонкого слоя такого золя на чистой гидрофильной поверхности может получиться сплошная сцепленная с подложкой пленка, которая остается растянутой по поверхности в процессе ее высушивания. Если эта пленка достаточно тонка, например толщиной всего 1 мкм, то в том случае, когда золь, образующий пленку, был сконцентрирован почти до точки гелеобразования, окончательное высушивание пленки протекает настолько быстро, что частицы кремнезема оказываются в плотно упакованном состоянии, прежде чем успевает образоваться гель, и поэтому не происходит никакой усадки или растрескивания; кремнеземная пленка при данных условиях будет прочно сцеплена с поверхностью.
В щелочных золях небольшие добавки солей, таких, например, как сульфат натрия, ускоряют желатинирование при высушивании золя. Так как для получения более прочной структуры геля золь должен высушиваться вплоть до достижения возможно более высокой концентрации кремнезема, то очевидно, что в стабилизированных щелочью золях необходимо избегать присутствия электролитов. Так, например, Рейтер [229] утверждает, что при использовании в качестве связующего золя кремнезема, имеющего небольшие по размеру частицы при рН в пределах 8,5—9 и минимальном содержании электролита, электропроводность золя обусловливается только присутствием коллоидных частиц кремнезема и стабилизирующих систему противоионов, но не примесями электролита.
Виссер [222] рассмотрел роль поверхностного натяжения воды и шероховатости поверхности подложки при адгезии коллоидных частиц на гладких поверхностях.
Очевидно, трудно получить плотную прочно сцепленную с поверхностью пленку кремнезема, если использовать золь, состоящий из однородных по размеру частиц. Айлер [219] исходил в своем патенте из того факта, что когда золь с частицами диаметром 100 нм высушивается в виде тонкой пленки на поверхности, то пленка хотя и остается размягченной, но сжимается и растрескивается гораздо в меньшей степени по сравнению с пленкой, полученной из золя, состоящего из меньших по размеру частиц. Добавлением серий постепенно уменьшающихся по размеру частиц кремнезема получали смесь частиц разного размера, которая при высыхании превращалась в прочную и гладкую сплошную пленку. Использование только одного золя с частицами размером 100 нм приводило к формированию непрочной пленки, в которой относительный объем, занимаемый кремнеземом, составлял примерно 70 %. Вместе с тем смесь, состоящая из 74 % золя с частицами размером 100 нм, 11,9 °/о золя с частицами 22 нм, 2,3% золя с частицами 10 нм и 2,8 % золя с частицами размером 7 нм, давала прочную пленку, в которой относительный объем, занимаемый кремнеземом, был равен 80,4 %. В такой пленке не появлялись волосные трещины и не происходило ее растрескивания при высушивании, поскольку промежутки между частицами большего размера заполнялись частицами меньшего размера, и, следовательно, масса пленки не могла сжиматься в значительной степени под действием сил поверхностного натяжения (см. рис. 4.16). Декстер и Таннер [230] теоретически рассмотрели упаковку сферических частиц трех различных размеров.
Однородные по размеру коллоидные частицы полезно использовать при приготовлении гелей с однородными большими порами, но оказалось, что чем больше по размеру исходные коллоидные частицы, тем заметно менее прочными получаются гели. Однако Иетс [231] обнаружил, что добавлением относительно небольшого количества растворимого силиката для образования кремневой кислоты удается усилить связи между
Рис. 4.16. Схема формирования прочного плотного геля из смеси больших и малых частиц кремнезема.
Частицами и получить гораздо более прочные гели. Подобным же образом Сиппел [232] нашел, что прочный гель с большей пористостью можно приготовлять из золя, содержащего частицы двух различающихся размеров: 40 % частиц, больших по размеру, диаметром D и 60 % частиц диаметром 0,4—0,8D. Относительно низкая прочность гелей, приготовляемых из частиц большего размера, частично компенсируется тем, что большие частицы упаковываются более плотно. Белоцерковский с соавторами [233] наблюдал, что в ксерогелях эффективный диаметр пор имеет тенденцию сохраняться постоянным, тогда как размер частиц в исходном золе изменяется. Малые частицы могут стягивать пленку, сохраняя при этом поры вплоть до величины равной диаметру частиц или даже более, а большие частицы (превышающие 50—100 нм) становятся более плотно упакованными с сохранением пор размером меньше диаметра частиц.
Как было предложено Шоупом (см. лит. к гл. 2 [97, 96]), очень прочные покрытия могут, вероятно, приготовляться за счет использования жидкой смеси, способной формировать гель, состоящий из силиката калия, коллоидного кремнезема и схватывающего агента.