^Работы Хоббеля и Викера
Хоббель и Викер с сотрудниками [84] опубликовали серию статей, в которых наиболее глубоко и полно описано изучение полимеризации. В этих работах одновременно было применено несколько методов анализа и получения характеристик системы, что позволило прослеживать процесс начиная с его самых ранних стадий. Индивидуальные полимерные разновидности выделялись в виде триметилсилильных производных и характеризовались молекулярной массой и составом, что позволяло рассчитать характеристики исходной кремневой кислоты.
Наиболее ранние стадии полимеризации монокремневой кислоты происходят настолько быстро, что авторы вынуждены были изучать такую реакцию при —2°С и даже при —13°С для того, чтобы проследить за образованием и за исчезновением кремнеземных разновидностей с низкой молекулярной массой в 0,5 М и 1,56 М растворах. Ценным явилось применение ЯМР-спектроскопии с использованием изотопа кремния 29Si, что позволяло четко различать мономер как от смесей димер— тример, так и от циклического тетрамера и более высоких циклических разновидностей. Они наблюдали следующие отрицательные сдвиги сигнала по отношению к более высокому значению поля, измеренному на стандартных соединениях с известными структурами:
Кремневая кислота Область, млн-1
Мономер 73,0-73,5
Димер + линейный тример ~82
Циклический тетрамер 90,4—91,5
Высшие циклические разновидности 91,8—92,6
Разветвленные группы а 99—101
А Атом кремния связан через кислород с тремя другими атомами кремния.
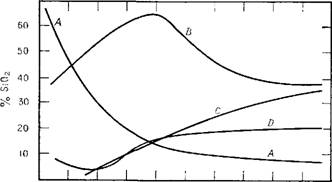
Метод ЯМР использовался в сочетании с усовершенствованными методами приготовления триметилсилильных производных промежуточных разновидностей кремнезема и четкого газохроматографического разделения с программированным нагреванием. Как показано на рис. 3.44, наиболее важным выводом явилось то, что полимеризация происходит в следующем порядке: прежде всего. образуется_дим. еЕд затем линейный три - мёр71Га~которыми следует циклический тетрамер, и далее полициклические полимеры и трехмерные полимерные разновидности. Полициклические соединения обнаруживались благодаря присутствию разветвленных групп.
К моменту времени, когда содержание небольших циклических полимеров в системе становилось максимальным, прибли-
|
70
Рис. 3.44. Ранние стадии полимеризации 0,5 Мл раствора монокремневой кислоты при —2°С и рН 2,0. (По данным Хоббеля и Викера [84].) А — мономер; В — скорее всего циклический тример, но может быть также димером или линейным тримером; С — циклический тетрамер; D — высшие поликремневые Кислоты. О 0 40 80 120 160 200 240 280 320 360 400 Время , мин |
Зительно 90 % мономера уже исчезало. При рН 1 даже при температуре — 15°С эти реакции протекали более быстро, и шло накопление высших полициклических кислот, а затем появлялись высокоразветвленные полимеры.
В тот же самый момент начиналась их дальнейшая конденсация с димером, тримером и тетрамером, вплоть до появления достаточно больших по размеру частиц кремнезема, действующих уже как зародыши для последующего роста частиц. Однако еще неизвестен механизм, по которому происходят внутренние перегруппировки с образованием плотной кремнеземной сердцевины частицы. Вероятно, такой механизм предусматривает разрыв и повторное образование новых силоксановых связей в объеме исходного полимера, причем в наибольшей мере происходит образование силоксановых групп, но исключается формирование силанольных групп. Такое превращение сопровождается некоторым сжатием частицы. Однако главным эффектом должно быть появление на поверхности большего числа групп SiOH и меньшего числа групп Si(OH)2. Одиночные силаноль - ные группы ионизированы более сильно, и, таким образом, более быстро происходит конденсация дополнительного количества мономера.
К тому моменту, когда на образование подобных зародышей израсходованы все самые небольшие олигомерные разновидности кремнезема, полученные коллоидные частицы приходят в состояние равновесной растворимости с мономером. Но если концентрация кремнезема составляет. более чем несколько тысяч частей на миллион (0,6 %, или 0,1 моль/л Si02), то частицы вскоре агрегируют в волокна или в разветвленные сетки микрогеля.
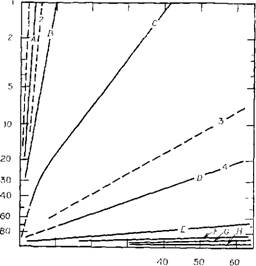
В своих более ранних исследованиях, выполненных при 25°С и наиболее стабильном рН 2,0, Хоббель и Викер получили основные сведения по полимеризации в 0,4 М растворе монокремневой кислоты (2,4 % Si02) при ее старении за время от 5 мин до 24 сут. Измерения были также выполнены при концентрациях растворов 0,084 М и 0,97 М. Полученные 'данные показали, что по мере развития процесса полимеризации способность кремнезема образовывать желтую кремнемолибдено - вую кислоту понижалась. Для каждого образца, взятого после определенного времени старения, измерялось процентное содержание кремнезема, еще не прореагировавшего с молибденовой кислотой, в зависимости от времени такой реакции вплоть до 80 мин. На основании этих данных для каждой стадии полимеризации подсчитывалась скорость реакции кНм мин-1 фракции с высокой молекулярной массой. Представленные на рис. 3.45 данные взяты из работы [84].
В течение 5 мин 40 % всего мономерного кремнезема поли - меризовалось в димер. Методом хроматографии было показано, что через 1 ч 40 % мономера и димера полимеризовалось с образованием циклотетракремневой кислоты, а также некоторого количества гексамерной формы кремневой кислоты и высших полимерных кислот. Через 4 ч приблизительно 50 % таких поли- тггерой",~впдаотк_до""тетрамера, превращалось в циклополикремне - вые кислоты при среднем значении константы скорости молиб- датной реакции 0,103 мин-1.
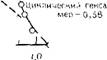
Как видно из рис. 3.46, наблюдается некоторый разрыв в соотношении между молекулряной массой и константой скорости реакции с молибденовой кислотой. Это позволяет отличать олигомеры от высших полимеров. Как будет показано ниже, такое изменение происходит на стадии, когда наблюдается «высокая молекулярная масса», т. е. основной вклад в систему дают коллоидные разновидности кремнезема.
|
Рис. 3.45. Скорость реакции поликремиевых кислот на различных стадиях полимеризации с молибденовой кислотой (по данным Хоббеля и Викера [84]). Концентрация S1O2 0,4 Мл, рН 2; температура 25 "С. Продолжительность полимеризации: 4 — 5 мии; В — 1 ч; С —4 ч; D — 1 сут; ІЗ — 3 сут; F — 5 сут, G —8 сут; Я—24 сут. Кривые для сравнения: / — мономер; 2 —димер; J — трехмерные полимеры; 4 — сдвоеи - иый цепочечный полимер (совпадает с кривой D). |
|
Юо Зо Время, мин |
|
10 - |
|
« Ю |
|
\ \ \ QКубический онтамер-0,52 |
|
Циклический тетрамер-0,6; |
|
^ Димер - 0,9 ..ГУІОНОМЄРТІ, 7 |
|
10 |
|
0,01 |
Ю
0,001
Рис. 3.46. Соотношение между молекулярной массой (Si02-*H20)п и константой скорости реакции с молибденовой кислотой кнм (по данным Хоббеля,- Викера и др. [84]). Кубический октамер и циклический гексамер не укладываются на прямую линию графика. Возможно, важным является то, что они не были обнаружены и при полимеризации в воде монокремневой кислоты.
23 Заказ № 200
Через 1 сут в системе наряду с высшим полимером оставалось 15 % низших полимеров, вплоть до тетрамера. Высший полимер имел константу скорости реакции 0,025 мин-1 и проявлялся на хроматограммах в виде полосы, положение которой менялось в зависимости от его молекулярной массы. Молекулярная масса полимерных разновидностей, определяемая на основании их триметилсилильных производных, составила 3440. Это соответствовало степени полимеризации, равной приблизительно 52 атомам кремния на одну полимерную молекулу, или же безводной частице Si02 с диаметром 1,65 нм.
Затем, по мере того как раствор подвергался старению в течение 1—8 сут, из поликремневых кислот получали триме- тилсилильные производные сложного эфира, в которых группы SiOH исходных кислот превращались в группы SiOSi (СН3)3. После удаления испарением и/или селективной экстракцией летучих олигомерных разновидностей производные поликремневых кислот с высокой молекулярной массой были проанализированы на содержание С, Н и Si, а их молекулярные щассы были определены в бензоле с помощью чувствительного к давлению паров прибора — осмометра. Молекулярная масса поликремневой кислоты подсчитывалась на основании молекулярной массы сложного эфира и коррелировалась с величиной константы скорости реакции с молибденовой кислотой. В течение интервалов времени от 8 до 42 сут (точка гелеобразования) молекулярная масса оценивалась только на основании значений константы скорости молибдатной реакции.
Авторы указали на отсутствие полимеров, состоящих из линейных цепочек, но, однако, остался открытым вопрос о природе высокополимерных разновидностей. Было сделано следующее предположение. В золе, подвергшемся старению в течение 1 сут, когда степень полимеризации достигала 52 атомов Si на одну молекулу полимера, полимер существовал в виде частиц кремнезема сферической формы. За время от 1 до 8 сут размер таких частиц увеличивался, а их число уменьшалось благодаря «созреванию по Оствальду». Затем в интервале 8— 42 сут продолжалось увеличение размера частиц по мере того, как они агрегировали в цепочки и сетки до тех пор, пока не образовывался гель.
В период «созревания по Оствальду» измеряли константы скорости реакции с молибдатом и оценивали молекулярную массу полимера. Величина константы скорости понижалась по мере увеличения размера частиц, однако в процессе агрегации она понижалась незначительно. Действительно, когда частицы связываются в цепочки, то лишь небольшая доля, поверхности теряется в местах контакта.
Таким образом, если эффективная молекулярная масса может повышаться до нескольких миллионов по мере увеличения размеров агрегатов, то молекулярная масса, подсчитанная из константы скорости молибдатной реакции, соответствует только размеру тех частиц, которые составляют цепочки и сетки. Следовательно, даже если молекулярная масса агрегатов вблизи точки гелеобразования приближалась к бесконечности, то молекулярная масса составляющих агрегаты частиц имела величину около 100 000, что соответствует степени полимеризации 1800.
В течение первых восьми суток процесса полимеризации измеряли молекулярную массу выделенных триметилсилильных производных высокополимерной фракции. Значения молекулярных масс рассчитывались по формуле
{SiO2-0,5x [OS і (СНз)з]х}«
Где х — отношение числа триметилсилильных групп к числу атомов кремния поликремневой кислоты и п степень полимеризации, определяемая с помощью осмометра.
Авторы представили доказательство, что все силанодьные группы превращались в триметилсилильные группы. Молекулярная масса поликремневой кислоты подсчитывалась по формуле
[SiO2-0,5.t-OHr]tf
В таблице 3.8 представлены значения х и п в зависимости от времени протекания процесса полимеризации. Из величины х подсчитывается число распределенных атомов кислорода, приходящихся на один атом кремния. Как было показано на рис. 3.44, отношение распределенных атомов кислорода к атомам кремния является функцией степени полимеризации, и эти значения находятся в разумном согласии со значениями, полученными Бечтольдом, Вестом и Плембеком [149].
Согласно формулам, рассмотренным в гл. 1, имеем
X = 2,\5d~l - l,53d~2 + 0,36d-3
Где d — эквивалентный диаметр безводной частицы Si02, содержащей п атомов кремния, нм.
П= 1 1,5йГ3 или d = 0,443я'/г
Тогда
Х = 4,85гг~,/з - 7,80n~Vi + 4,2п~1
Как показано в табл. 3.8, значения х рассчитывались при различных значениях п после старения золей в течение указанного числа суток.
При низкой степени полимеризации, равной 52, существует некоторое различие между отношением ОН : Si, равным 0,83,
|
Таблица 3.8 Значения п их, рассчитанные по данным Хоббеля и Викера [84]
|
|
А Экстраполированные значения. 6 Допускается, что полимерные образования представляют собой сферические кремнеземные частицы. в Получено из константы скорости реакции с молибдатом. Однако к этому моменту процесс агрегации уже начался, и фактическое значение молекулярной массы было гораздо большим. |
Подсчитанным по формуле для сферических частиц, и значением 0,65, подсчитанным из экспериментальных данных. Однако в дальнейшем, при обсуждении теории зародышеобразования, будет отмечено, что в соответствии с моделью, показанной на рис. 3.17, на той стадии, когда степень полимеризации равна 48 (т. е. частица уже сформирована и имеет сердцевину из S1O2), такая модель дает отношение ОН: Si, равное 0,66, а не 0,8, как это следует из формулы для сферической частицы! Возможно, что это чистая случайность, но, по-видимому, следует поддерживать ту точку зрения, когда вначале частицы кремнезема формируются на зародышах, представляющих собой трехмерный октамер или декамер (см. рис. 3.17).
После того как частицы увеличиваются в размере, их стехиометрия, как было постулировано, приближается к стехиометрии сферы. Таким образом, выше степени полимеризации 500 (размер безводной частицы БЮг составляет 3,5 нм) состав полимера очень близок к составу, подсчитанному для сферической частицы.
Скорость полимеризации. Увеличение степени полимеризации со временем достаточно хорошо выражается уравнением:
, 3000 г, п. , ^ 3000 - я
Или dn/dt = 0,023 (3000 — п)
Где п — степень полимеризации и t — время (примерно до 8 сут), сут. В момент времени, равный 8 сут (см. рис. 3.46), степень полимеризации составляет около 460, что соответствует диаметру частицы — 3,4 нм. После этого начинается процесс агрегации, и по мере развития этого процесса сетка микрогеля упрочняется и начинает более медленно реагировать с молибдатом. Экстраполированный предел п = 3000 соответствует размеру дискретных частиц (6,4 нм), которые должны реагировать с той же самой скоростью, что и скорость полимера микрогеля. Такой размер соответствует величине удельной поверхности 400—500 м2/г, что является вполне подходящим для геля. К тому же этот размер приближается к размеру, при котором растворимость кремнезема падает до значения 0,01—0,012 %.
В экспериментах Хоббеля и Викера отмечено, что константа кНм скорости реакции высокополимера с молибдатом близка к обратно пропорциональной зависимости от степени полимеризации п. Это приблизительное соотношение записывается как
|
|
Где п изменяется от 121 до 1260.
Можно предположить, что скорость реакции должна быть пропорциональна площади поверхности кремнезема и разности растворимостей между очень небольшими частицами и массивным кремнеземом. Можно показать, что эта разность изменяется обратно пропорционально квадрату радиуса частицы в рассматриваемой области размеров. Поскольку величина удельной поверхности обратно пропорциональна радиусу частицы, то скорость реакции должна в таком случае быть обратно пропорциональной радиусу частицы в кубе. Как отмечалось выше, это значение пропорционально степени полимеризации п.