Полисиликаты лития
Айлер [101] в 1954 г. обнаружил, что концентрированные устойчивые растворы с молярными отношениями Si02 : Li20 от 4:1 до 25 : 1 можно получать добавлением LiOH либо к раствору поликремневой кислоты, либо к суспензии геля кремнезема, либо к золю кремнезема, причем все реагенты должны быть свободны от ионов щелочных металлов или других катионов. Поскольку такие смеси сгущаются или же немедленно превращаются в гель, то подобный способ казался бесполезным до тех пор, пока не было обнаружено, что полученная масса самопроизвольно разжижается после выдерживания при комнатной температуре в течение нескольких часов (до суток). Если же с целью ускорения разжижения смеси нагревали до 80—100°С, то они оставались в желатинизированном состоянии. Жидкие составы содержали как ионную форму, так и коллоидный кремнезем.
Технические растворы полисиликата лития имеют следующие свойства [102]:
Полиснлнкат
S102, %
Li20, %
Молярное отношение
Si02: Li20 Вязкость. сП Плотность рН
Срок хранения при 24° С, мес
Поскольку составы во всем интервале отношений Si02 : Li20 от 4 : 1 до 25 : 1 растворимы и устойчивы, то такая предложенная Айлером система дает возможность изучать взаимосвязь между отношением содержания кремнезема к содержанию щелочи и природой присутствующих коллоидных разновидностей. Растворы полисиликата лития приготовляли смешиванием раствора поликремневой кислоты, полученного ионным обменом из силиката натрия с отношением Si02 : Na20 3,25 с раствором гидроксида лития. Эти смеси подвергали старению при 25°С в течение недели до получения прозрачных жидкостей в равновесном состоянии. Растворы содержали 10 % Si02 и имели отношения Si02 : Li20 в интервале от 3 : 1 до 10 : 1.
Такие растворы сравнивали между собой путем измерения скоростей образования желтой формы кремнемолибденовой кислоты. Процедура заключалась в мгновенном смешивании микроколичеств указанных растворов с раствором молибденовой кислоты при низких значениях рН. Для каждого образца отмечалась доля в процентах Р от полного содержания кремнезема, прореагировавшего при 25°С за определенное время /, равное 2,5; 5; 10; 15 и 20 мин. Рассматривался также раствор силиката натрия с молярным отношением Si02 : Na20 3,3 : 1,0. Было отмечено, что он реагирует с раствором молибденовой кислоты примерно таким же образом, как и раствор силиката лития с соответствующим отношением Si02 : Li20.
Принималось, что все растворы состояли в основном из мономерных силикат - и полисиликат-ионов с высокими молекулярными массами, причем полисиликатные ионы представляли собой очень небольшие заряженные коллоидные частицы. Так как мономерные ионы вступают в реакцию с молибдатом примерно в течение 2,5 мин, то в каждом случае отмечалась и доля в процентах Рт, относящаяся к мономерному кремнезему.
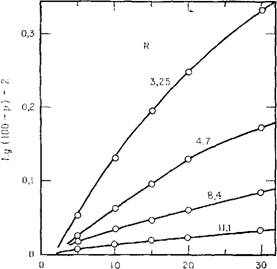
Следовательно, разность Р—Pmi или р, соответствовала процентному содержанию кремнезема в полимерном состоянии, который вступал в реакцию с молибдатом к моменту времени t. Изменение количества полимера в ходе реакции выражается следующим уравнением:
Lg 'V = kt (см. рис. 2. 4.)
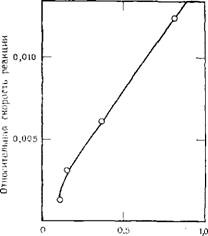
Графическая зависимость величины относительной скорости реакции k от величины (R—2)-1 (где R — молярное отношение Si02 : Li20) представлена на рис. 2.5. Разность R—2 берется потому, что коллоидные разновидности присутствуют только при отношении R, большем чем 2:1. Поскольку, как уже отмечалось, скорость рассматриваемой реакции является обрат-
|
(R ~2У' Рис. 2.5. Зависимость относительных скоростей реакции коллоидных разновидностей в растворах полисиликата лития с молибденовой кислотой от величины (R-2)-'. R — молярное отношение Si02 : ІЛ2О. |
|
Рис. 2.4. Ход реакции коллоидных разновидностей кремнезема с молибденовой кислотой в растворах полисиликата лития при различных отношениях Si02: Li20 (указаны на кривых). |
|
Время, мин |
Ной функцией от размера коллоидных частиц, то отсюда делается заключение, что размер коллоидных разновидностей равномерно и самопроизвольно должен возрастать пропорционально той степени, при которой отношение SiC>2 : Li20 превышает 2:1. Это по крайней мере справедливо для области отношений Si02 : Li20 от 3 : 1 до 10 : 1. При более высоких отношениях Si02 : Li20 размер частиц взаимосвязан с этими величинами в меньшей степени. Так, хорошо известно, что при отношениях Si02 : Li20, больших чем 25 : 1, стабилизация золей различающихся по размерам частиц почти не зависит от размера частиц.
Таким образом, полисиликатный раствор самопроизвольно достигает равновесия со смесью мономерных и коллоидных разновидностей, причем размер последних возрастает, когда отношение Si02 : Li20 больше, чем 2:1.
Были предложены многочисленные производственные технологические процессы. Например, был приготовлен полисиликат лития из 2,6 %-ного золя кремнезема [103]. Золь получали ионным обменом из силиката натрия с добавлением LiOH для достижения области отношений Si02 : Li20 от 2,5:1 до 8:1. Раствор затем концентрировали испарением в вакууме, что позволило повысить содержание кремнезема до 21 %. Как было указано автором, в растворе присутствовал в большей степени «кристаллоидный», чем коллоидный, кремнезем. Такой кремнезем получался вследствие того, что исходный золь, вероятно, содержал частицы кремнезема размером 1—2 нм.
Раствор полисиликата лития с молярным отношением Si02 : Li20 3,5 можно приготовить нагреванием тонкодисперсного аморфного кремнезема в растворе LiOH при молярном отношении 1,5 :1 [104]. Образующийся при повышенной температуре осадок после охлаждения разжижается до полисиликатного раствора с содержанием 23,4 % Si02. Очевидно, что силикат, выделяемый из горячего раствора, имеет более высокое отношение Si02 : Li20 по сравнению с отношением в оставшемся растворе [104]. Согласно Пэттону и Коксу [105], силикаты лития с молярными отношениями от 2 : 1 до 6,3 : 1 могут приготовляться аналогичным образом при 75—150°С с сохранением осадка в суспензии и с последующим охлаждением, для того чтобы оказать воздействие на весь раствор. Полисиликат можно также приготовлять растворением порошка кремния в растворе LiOH при 50—80°С в присутствии Си(ОН)2 в качестве катализатора [106].
Наличие некоторого количества силиката лития в растворах силиката натрия или силиката калия, очевидно, дает некоторые преимущества [107, 108].