Гидратированный аморфный кремнезем
Как будет показано, сильно гидратированные формы кремнезема, которые в общем случае стабильны вплоть до 60 °С, должны рассматриваться отдельно, поскольку их растворимость, по-видимому, отличается от растворимости безводных форм или форм, гидратированных только на поверхности.
Из сложных циклогексановых эфиров, имеющих формулы [(C6HiiOhSiO]4 и [C6HnOSiOi,5] ю, был приготовлен твердый, нерастворимый гидратированный аморфный кремнезем двух типов [107]. Первый представлял собой циклический тетрамер, второй имел объемную структуру, похожую на клетку, в которой каждый атом кремния связывается с одной эфирной группой. Путем удаления циклогексановых групп безводной кислотой HI получены чрезвычайно гигроскопичные белые аморфные порошки, состав которых соответствует формулам [(НО)г5Ю]х и [HOSiOil5]v.
Можно показать, что даже если вначале образуются молекулы кремневой кислоты с низкой молекулярной массой, процесс конденсации силанольных групп между соседними молекулами с образованием силоксановых связей и молекул воды будет происходить достаточно быстро. Однако молекулы воды удерживаются еще настолько прочно, что суммарный химический анализ дает те же самые результаты, хотя масса кремнезема сшивается поперечными связями и становится нерастворимой.
Природный опал может содержать 5,25—13,7 % воды,, которая удерживается внутри структуры и не испаряется [108]. Учитывая, что опал не адсорбирует газы и жидкости в достаточной степени, его можно считать в основном непористым кремнеземом.
Гидратированные в высокой степени гели кремнезема, прочно удерживающие воду при обычной температуре, могут быть получены в результате реакции кристаллогидратов силиката натрия с безводной кислотой. Выделяемая при этом в свободном состоянии кремневая кислота одновременно полимери - зуется до очень плотного состояния [109].
Для получения подобных гелей гидролизом этилсиликата в дистиллированной воде при 17°С предварительно готовили золи с содержанием около 0,5 % Si02. При стоянии в течение нескольких дней по мере образования агрегатов система становилась вязкой. Сформировавшийся осадок отфильтровывали, в результате чего получались влажный гель и избыточная вода при 15—17°С. Полное удаление следов НС1 из эфира замедляет гидролиз, и поэтому такое удаление даже нежелательно. К со
жалению, значение рН не регистрировалось, но оно, вероятно, было ниже 6, если присутствовали следы кислоты [110, 111], Для случая дегидратации влажного геля в вакууме при 11°С на графике зависимости содержания остаточной воды от давления пара в интервале 7—1 мм рт. ст. проявляются четкие ступеньки, соответствующие молярным отношениям воды к кремнезему, равным 2,5; 2,0; 1,5; 1,0 и 0,5.
Из значений давления пара воды на стадиях гидратации, соответствующих молярным отношениям 0,5; 1,0; 1,5 и 2,0, измеренным при различных температурах в интервале 35—60°С, выявлено [111] линейное соотношение между lg Р и Т~1 и подсчитана средняя теплота гидратации h, приходящаяся на 1 моль воды в области температур от Ті до Т2:
R — газовая постоянная;
Pk,, Pk2 — давление диссоциации гидрата при температуре Т\,
Ті,
Pw_ , Pw2— давление паров воды при Ті и Т2\ h составляла 1,2—1,5 ккал/моль Н20.
Выше упоминалось, что Гринберг [13] определил для реакции
S1O2 (тв. аморфн.) + мН20 (ж.) =Н45Ю4(водн.)
Значение Д# = 2,65±0,28 ккал/моль. Если допустить, что теплота растворения H4S1O4 незначительна и яг = 2, то АН в расчете на 1 моль воды равнялась бы 1,32 + 0,14 ккал/моль, что находится в согласии с приведенным значением, полученным Тиссеном и Корнером совершенно другим методом.
С образованием определенных гидратов в рассматриваемой системе, которая, как теперь известно, является аморфной, трудно согласиться. Более вероятно ступенчатое удаление монослоев адсорбированной воды с большой по величине поверхности кремнезема, если предположить, что удаление одного монослоя случайно совпадает с удалением 0,5 моля воды в расчете на 1 моль кремния. Если это так, то никакого образования воды за счет конденсации групп SiOH не следует учитывать и приведенное выше совпадение с данными Гринберга является случайным.
|
Г |
На основании современных сведений о подобной системе (более подробно рассмотренной в гл. 3) вполне можно считать, что золь, полученный гидролизом этилсиликата, содержит поликремневую кислоту или частицы кремнезема настолько малые, что значительная доля атомов кремния; удерживающих группы ОН, расположена на поверхности таких частиц.
Вначале эти частицы агрегируют в короткие цепочки, образуя очень открытую трехмерную кремнеземную сетку геля, заполняющую водную фазу. По мере удаления воды происходит постепенное сжатие этой сетки. Однако при нормальной температуре остается слой воды толщиной, вероятно, в несколько молекул, который связан водородной связью с силанольной поверхностью кремнезема. Таким образом, сформировавшийся гидратированный гель имеет более низкое давление водяного
|
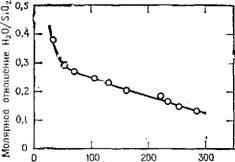
Температура, °С Рис. 1.3. Содержание связанной воды в гидрэтированном аморфном кремнеземе при повышении температуры в вакууме по данным [ПО]. |
Пара, чем давление насыщенных паров жидкой воды. Ступенчатое удаление воды, возможно, соответствует удалению последовательных слоев молекул Н20 с поверхности кремнезема. По мере ее удаления из пространства между частицами кремнезема структура геля сжимается, и частицы будут сближаться до тех пор, пока не удалится вся свободная вода и не придут в контакт силанольные поверхности кремнезема.
Как показано на рис. 1.3, такая стадия для рассматриваемого типа геля достигается в точке, имеющей молярное отношение H20/Si02, равное 0,275. Графическая зависимость содержания воды в этом геле от температуры приведена при давлении 2 мм рт. ст. [110]. Так как известно, что удаление воды в интервале температур 200—300°С включает дегидратацию силанольных групп, то, следовательно, линейный участок выше 70°С относится именно к этому процессу, тогда как ниже 70°С удаляется только адсорбированная вода. Таким образом, содержание силанольных групп при 70°С составляет около 0,27 моль Н20, или 0,54 групп ОН на 1 атом кремния.
Из этих данных можно оценить значение удельной поверхности кремнезема, учитывая, что площадь, приходящаяся на одну группу ОН, в случае высокогидроксилированной поверхности составляет около 12,5 А2:
0,54 • 6 • 1023 . 12,5 спп 2/ с-г> - = 690 м7г Si02
60- 1020
В случае когда вода адсорбируется на силанольной поверхности, на одну группу SiOH приходится одна молекула Н20. Следовательно, монослою воды соответствует молярное отношение - H20/Si02, равное 0,54. Рассмотрение ступенек на адсорбционных кривых [110] действительно показывает, что величина каждой ступеньки соответствует отношению H20/Si02 = 0,5.
Тем не менее необходимо признать, что, используя указанную теорию, трудно объяснить определенные отношения H20/Si02, равные 1,0 и 0,5, идентифицированные в гелях, приготовленных гидролизом сложных циклогексановых эфиров циклической тетракремневой кислоты [(HO)2SiO]4 и полициклического декамера [(HO)2Si2Os] 5 [107] или же [(HO)2SiO]x, полученного при гидролизе SiS2 [112].
С другой стороны, Де Буром было отмечено [113а], что удаление слоев воды с поверхности оксида алюминия происходит в виде отчетливо выраженных ступенек. Таким образом, отмеченное выше объяснение не является исключением, поскольку высокогидратированные гели, приготовленные при нейтральном или низких рН и при комнатной температуре, обычно имеют удельную поверхность в области 600—800 м2/г.