Адсорбция Si(OH)4 на кристаллическом кремнеземе
В 1955 г. было замечено, что, когда порошок кварца вводится в воду, концентрация растворенного кремнезема Si (ОН) 4 сначала быстро увеличивается, но затем повышается очень медленно. Это прослеживалось вплоть до образования на кристаллической поверхности какой-то формы кремнезема, которая составляла 16 % от величины монослоя на поверхности и могла быстро растворяться. Более того, после удаления этой формы с поверхности обработкой щелочью очищенная поверхность адсорбировала из раствора Si(OH)4, и на ней повторно образовывался такой же слой. Используя мономер Si(OH)4, содержащий радиоактивный изотоп 31Si, авторы обнаружили, что при
РН 9 происходит обмен мономера, находящегося в растворе, с мономером, адсорбированным на поверхности, но не с очищенной поверхностью кристалла, а при рН 5 никакого обмена не происходит [142, 143].
Штобер исследовал растворимость ряда модификаций кремнезема. Он развил теорию и вывел соответствующее уравнение для описания поведения адсорбированной монокремневой кислоты с учетом задержки в приближении к истинному состоянию равновесной растворимости [144].
Штобер предполагал, что взаимодействие Si(OH)4, находящегося в растворе, с поверхностью кремнезема должно включать следующие этапы:
1. Силоксановые связи Si—О—Si на поверхности разрываются в процессе гидролиза, образуя в среднем две связи на один поверхностный тетраэдр Si04 и одну адсорбированную на поверхности молекулу гидратированной кремневой кислоты.
2. Молекула Si (ОН) 4 десорбируется в раствор.
3. Мономер Si(OH)4 адсорбируется из раствора на поверхности, по мере того как достигается равновесие и происходит обратимый процесс, сопровождаемый конденсацией и увеличением Si02 на поверхности.
Штобер вывел следующие уравнения. Уравнение для адсорбции мономера Si(OH)4 имеет вид:
"■ads = {П+СЬс (1)
Nads — концентрация адсорбированного мономера Si (ОН) 4 на поверхности;
' п0 — поверхностная концентрация Si(OH)4 при заполнении всего монослоя;
С — концентрация кремневой кислоты в растворе;
B — константа адсорбции.
Адсорбция происходит лишь на поверхности, еще не покрытой молекулами Si (ОН) 4:
-±!L = (n0~nads)k-exp(-AR^T-i) (2)
Пн — количество молекул кремневой кислоты, освобождаемых в процессе гидролиза и приходящихся на единицу поверхности кремнезема; t — время;
K — константа кинетического уравнения для процесса гидролиза;
А — энергия активации процесса гидролиза;
R — газовая постоянная;
Т — температура, К.
Предполагается, что адсорбционное равновесие устанавливается относительно быстро по сравнению с другими рассматриваемыми этапами. Таким образом, уравнение (1) может быть включено в уравнение (2):
-^-т?*-*-» Р(-тг) <3>
Процесс конденсации на поверхности затрагивает лишь адсорбированные молекулы Si(OH)4:
-^Г - = - tladsk' ■ ехр (------------- (4)
Лс — количество сконденсированных молекул кремневой кислоты в расчете на единицу поверхности кремнезема; k'—константа кинетического уравнения для процесса конденсации;
А' — энергия активации процесса конденсации.
Так как принимается, что температура остается постоянной и величины k, k', А я А' также не изменяются, то можно ввести новые константы:
К = k • ехр (------ К' = k' • ехр (—
Комбинирование уравнений позволяет записать
■{К-К'Be)
Dt dt 1 dt 1 + be
Где n — концентрация адсорбированных молекул мономера к моменту времени t.
Концентрация кремневой кислоты с может быть выражена через объем растворителя V и общую поверхность твердого образца кремнезема F:
T
С = с_________ njЈl±______ L. JL [JiLdt
0 Са К (1 + be) V 2 dt Ul
Где са — начальная концентрация мономера Si(OH)4 в растворе.
|
Dn _ dnff і dnc _ щ |
Дифференцирование уравнения дает возможность установить взаимосвязь между временными изменениями величин концентраций, происходящими соответственно на поверхности твердого кремнезема и в объеме раствора:
Dn Г V. nob 1 dc
Dt IF' (1 - f be)2 j dt
|
J ___ Ce К |
Замена величины dnldt и последующее интегрирование дают 6 In (1+6с) Vbc bn0F - j-V (1 - bce)2 jn ^ — —J
1 + bce n0F n0F(\+bce)
где се — концентрация кремневой кислоты в растворе в состоянии равновесной растворимости для двухфазной системы, т. е. растворимого кремнезема в растворе и твердого аморфного кремнезема. Эта концентрация определяется как се = К! ЬК'.
Фаза твердого аморфного кремнезема, по-видимому, могла появиться в растворе в виде коллоидных частиц или же> как осажденный слой аморфного кремнезема в некоторых областях поверхности кристаллического образца.' Штобер использовал экспериментальное значение величины се, равное 0,011 % (110 мкг SiC>2 в 1 мл). На основании известной величины поверхностной концентрации, равной 10 микромоль Si(OH)4 на 1 м2, или 6 молекулам Si(OH)4 на 1 нм2, подсчитано [145], что величина щ равна 600 мкг Si(OH)4/M2. Экспериментальные данные были получены при растворении кремнезема в 500 мл раствора Рингера при рН 8,2 в течение 3—4 недель при 25°С с общей поверхности кристаллического образца кремнезема 10 м2. Используя в своих экспериментах частицы различных размеров, Штобер нашел относительную константу скорости растворения, отнесенную к единице поверхности.
Для кварца тот же автор использовал 6 групп частиц различных размеров в интервале 0,007—1,3 мкм с удельными поверхностями от 33,6 до 1,7 м2/г соответственно. Из концентрационной кривой растворимости кремнезема как функции времени были определены константы для приведенного выше уравнения:
B = 0,7 мл/мкг 1,7 сут"1
Конечные концентрации растворимого кремнезема изменялись в диапазоне от 0,0011 до 0,0013 % в превосходном согласии со значением 0,0011 % для растворимости кварца [115].
Для кварцевого стекла Ь = 0,7 мл/мкг (как и для кварца), но значение константы гидролиза К оказалось много большим, чем для кварца, что указывает на гораздо большую скорость гидролиза кварцевого стекла по сравнению с кварцем.
Допуская, что во всех случаях Ь = 0,7 мл/мкг, были определены следующие значения К и К' для различных модификаций кремнезема:
|
К', сут^1 (конденсация) |
|
К, сут—' (гидролиз) |
Кварц
Кварцевое стекло
Кристобалит
Стишовит
Тридимит
Коэсит
Когда фазы кремнезема, отличающиеся от кварца и от аморфного кремнезема, суспендированы в воде, конечная концентрация растворимого кремнезема не является концентрацией насыщения, а представляет результат конкуренции между кремнеземом, попадающим в раствор в виде молекул Si (ОН) 4, и молекулами Si (ОН) 4, повторно адсорбирующимися во всевозрастающей степени на поверхности твердого образца и блокирующими дальнейший процесс растворения. Таким образом, получаемая предельная концентрация зависит от величины поверхности твердого образца, подвергаемой действию раствора, и отнесена к единице объема раствора.
В том случае, когда один и тот же образец кремнезема с фиксированной общей поверхностью, равной 1 м2, каждые сутки помещается в 50 мл свежеприготовленного раствора Рингера (рН 8,4) с длительностью пребывания в растворе 24 ч, то количество кремнезема в растворе, ежесуточно поступающего за счет процесса растворения, достигает некоторого стабильного значения, которое является характеристическим для данной выбранной модификации кремнезема:
Удельная поверх - Предельная кон - ность, ы"/г центрация крем
Незема, масс. %
Кварцевое стекло 8,8 0,0039
Стишовит 21,6 0,0011
Кристобалит 8,5 0,0006
Тридимит 12,0 0,00045
Кварц 10,4 0,00029
Коэсит 10,6 0,00007
Если точка зрения Штобера правильна и кристобалит не имеет истинной равновесной растворимости, то расчеты, выполненные на основании опубликованных в литературе данных по растворимости, не могут быть обоснованными. Необходимость более точного определения понятия растворимости отмечалась и другими авторами [146]. Данные, представляемые в литературе как «растворимость» - различных форм кремнезема, часто указывают только лишь на скорость растворения или на предельную концентрацию, получаемую при частных условиях. Так, например, сообщение о том, что при рН 12,8 опал в 15— 18 раз более растворим по сравнению с безводным кремнеземом, просто указывает на относительную скорость растворения [147].
Подобным образом данные по растворимости, полученные Копейкиным и Михайловым [148] для кварца (0,0007 %), кри - стобалита (0,0012%), тридимита (0,0016%), кварцевого стекла (0,0088 %) и аморфного кремнезема (0,012%), завышены в случаях тридимита и кристобалита по сравнению с предельными концентрациями, наблюдаемыми ранее Штобе - ром. Нет сомнения, что подобные расхождения возникают из-за различий применяемых методов исследования. Из рассматриваемых данных только значения для кварца и аморфного кремнезема представляют собой истинную растворимость.
Взаимосвязь между «быстрорастворимым кремнеземом» на поверхности частиц кварца в области микронных размеров и «нарушенным слоем» в дальнейшем была исследована Бергманом, Картрайтом и Бентли [149], которые пришли к заключению, что частицы размером менее 1 мкм содержали слишком много быстрорастворимого кремнезема и это невозможно объяснить только лишь за счет присутствия его мономолекулярного слоя. Так, например, на частицах размером 0,3 мкм 8 % поверхности составлял быстрорастворимый кремнезем. Несомненно, что такой «нарушенный» материал должен быть удален с поверхности кварцевых частиц прежде, чем можно будет приступить к изучению поведения адсорбированного мономера Si (ОН) 4.
В работе [150] исследовалось растворение и осаждение кремнезема на кварце. Было установлено, что для предварительно очищенного действием HF образца кварца, погруженного в 0,1 н. раствор ацетата натрия при рН 7,7, наблюдалась кажущаяся равновесная растворимость 0,0018—0,0020 %. Осаждение монокремневой кислоты при рН~7 протекало гораздо быстрее, чем в более кислом растворе.
Необъяснимое до сих пор явление наблюдалось Бауманом [151]. Если очищенный порошок кварца многократно суспендировался в буферном растворе при рН 8,5 с концентрацией растворимого кремнезема 0,0088 %, то кремнезем адсорбировался на поверхности кварца до тех пор, пока не образовывалось несколько монослоев (рис. 1.5а и 1.56). Скорость адсорбции возрастала с повышением рН от 3 до 9 и была пропорциональна второй или третьей степени от значения исходной концентрации; с увеличением степени покрытия поверхности она уменьшалась. Изучение кинетики процесса показывает, что растворимый кремнезем удерживается на поверхности не физическими, а химическими связями. В процессе семи повторных 40-суточных экспериментов по выдерживанию порошка кварца с исходной концентрацией растворенного кремнезема 0,0088 % в растворе (при условии замены каждый раз раствора на свежий) адсорбция на порошке кварца продолжалась вплоть до осаждения четырех монослоев. Адсорбированный кремнезем не являлся обычным кристаллическим кварцем, поскольку был способен растворяться быстрее, чем кварц. Тем не менее такой кремнезем имел гораздо меньшую растворимость по сравнению с аморфным кремнеземом, так как продолжал осаждаться из раствора с концентрацией растворимого кремнезема менее
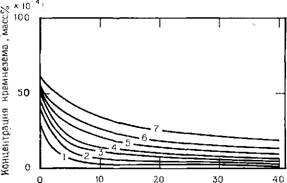
Нумерация кривых соответствует числу замен раствора иа новый. Во всех случаях начальная концентрация раствора составляла 0,0080 %.
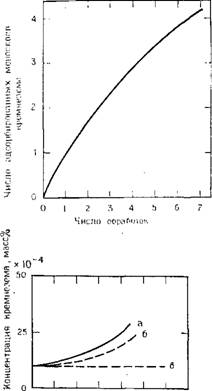
Рис. 1.56. Зависимость числа слоев адсорбированного на поверхности кварца мономерного кремнезема от числа 40-суточных обработок при 25 °С. Первоначальная концентрация кремнезема 0,0080 %. (Данные Баумана [151]).
Рис. 1.5в. Концентрация растворимого кремнезема, находящегося в растворе в равновесии с монослоями адсорбированного кремнезема при 25 °С. (Данные Баумана [151]).
|
0 12 3 4 5 6 Число адсорбированных монослоев |
|
Рис. 1.5а. Концентрация растворимого кремнезема в растворе после контактирования раствора с поверхностью кварца в течение указанного на рисунке времени при 25 °С. (Данные Баумана [151]). |
|
Сутли |
A — после 40 сут, б — экстраполирование к 100 сут, в — растворимость кварца
0,0030 % (растворимость обычного аморфного кремнезема 0,011—0,012 %).
Бауман предположил, что истинная растворимость кварца может быть даже меньшей чем 0,0011 %. По его мнению, растворение кварца прекращается при достижении концентрации растворимого кремнезема 0,0011 % в результате того, что при этой концентрации на поверхности кварца достаточно адсорбированных молекул Si (ОН) 4, чтобы прекратить процесс растворения при 25°С. С другой стороны, величина 0,0011 % представляет собой значение растворимости, экстраполированное из данных, полученных при более высоких температурах, когда, как известно, достигается истинная равновесная растворимость, а кристаллы кварца растут в пересыщенном растворе.
Это подтверждает тот факт, что адсорбированные слои кремнезема при 25°С очень медленно принимают упорядоченную структуру лежащей ниже кристаллической решетки. Кристаллизация, оставаясь действительно медленно протекающим процессом, тем не менее ускоряется с повышением температуры.
Возможное объяснение для вышеприведенных наблюдений заключается в следующем. Первый адсорбированный слой Si (ОН) 4 удерживается вначале водородными связями. Затем путем образования силоксановых связей происходит конденсация слоя с довольно правильным расположением, почти повторяющим регулярное построение нижележащих атомов кремния. Наличие на поверхности кварца регулярно расположенных силанольных групп позволяет осуществлять как почти совершенное совмещение адсорбированных молекул Si(OH)4, так и их очень сильную адсорбцию. Каждый последующий слой менее регулярен, что приводит к понижению величины адсорбционной константы и к повышению кажущейся растворимости такого слоя. Однако в четвертом слое регулярность расположения еще остается настолько заметной, что растворимость составляет только примерно 0,0025 %.
Из графической зависимости концентрации кремнезема в растворе после 40 сут от числа адсорбированных молекулярных слоев Si02 (данные Баумана, рис. 1.5 в) видно, что, вероятно, уже после второго слоя растворимость повышается, тогда как с увеличением числа слоев регулярное расположение атомов становится более разупорядоченным.
Из рис. 1.5а, показывающего зависимость концентрации кремнезема в растворе от времени контакта раствора с поверхностью кварца, видно, что наиболее близкие к линейным участки кривых позволяют выполнить приемлемую экстраполяцию к моменту времени контакта в 100 сут. Как показано на рис. 1.5в, величина концентрации кремнезема в растворе непрерывно падает; тем самым обосновано предположение, что во всех случаях кон - дентрадия кремнезема в растворе приближается к растворимости кварца. Следовательно, вполне вероятно, что если подобный кварцевый порошок с несколькими слоями адсорбированного кремнезема на поверхности подвергать процессу старения в течение примерно года или же нагревать суспензию кварца в растворе до 100°С, то адсорбированный кремнезем стал бы превращаться в кварц, а его растворимость понизилась бы до растворимости последнего.