Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
СВОЙСТВА ХЛОРИСТОГО ВОДОРОДА и соляной кислоты
|
Ю 30 50 70 90 Температура, 'С |
|
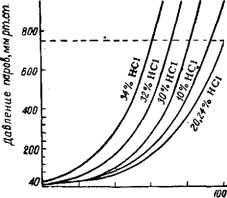
Рис. 111. Общее давление паров над соляной кислотой разных концентраций (в вес. %); (пунктирная линия —изобара 760 мм рт. ст.). |
Хлористый водород НС1 — бесцветный газ. 1 л при 0° весит 1,639 г; плавится он при —114,2°, кипит при —85,1°. Критические температура и давление равны 51,5° и 81,6 ат. Плотность жидкого хлористого водорода 0,831 г/см3 при 20° и 1,194 г/см3 при —85,8°.
Давление пара над жидким хлористым водородом:
Температура, °С. Давление, ат. .
|
0 25,46 |
|
20 41, £ |
|
40 64,52 |
|
51.5 81.6 |
-85,0 -20 1,0 14,53
При 30° жидкий хлористый водород растворяет меньше 0,1% воды. Молярная теплоемкость газообразного хлористого водорода при постоянном давлении вычисляется по формуле Ср = 6,5 + 0,001 Т.
Во влажном воздухе хлористый водород образует густой туман — мельчайшие капли соляной кислоты. Вредно действует на организм, раздражая и разрушая слизистые оболочки и дыхательные пути. Предельно допустимая концентрация НС1 в воздухе рабочей зоны производственных помещений 0,01 мг/л (С12—0,001 мг/л).

|
20 30 40 50 60 70 90 90Ю01Ю Температура, °С |
|
Рис. 112. Давление НС1 над соляиой кислотой в зависимости от температуры И еодержания HCl (в вес. %) в раСтворе. |
|
Температура, °С.... Число литров НС1, погло 1даемых 1 л воды. . |
Безводный хлористый водород почти не действует на металлы, соляная же кислота растворяет большинство металлов. В соляной кислоте устойчивы платина, золото, тантал, ниобий, некоторые силикатные минералы (андезит, диабаз, кварц) и изделия (стекло, керамика, фарфор), а также эбонит, резина, некоторые пластические массы, например, фао - лит, винипласт, тефлон и др. Углеродистая сталь, нагретая до 300—400°, и нержавеющие стали 1Х18Н9Т и ЭИ-496, нагретые до 500°, удовлетворительно устойчивы к соляной кислоте2'3. Окислы металлов превращаются газообразным хлористым водородом в хлориды; реакции ускоряются в присутствии водяного пара 4. Растворимость хлористого водорода в воде очень велика и Вильно зависит от температуры; при общем давлении 760 мм рт. ст.:
0 10 20 30 40 50 60
506,5 473,9 442,0 411,5 385,7 361,6 338,7
При парциальном давлении НС1 в газе 760 мм рт. ст. 1 л воды при 0° растворяет 525,2 л НС1 (в растворе 46,15 вес.% НС1), при 18° —451,2 л НС1 (в растворе 42,34 вес. % НС1). Общее давление паров и давление НС1 над соляной кислотой приведены на рис. 111 и 112. Теплоты растворения НС1 в воде могут быть вычислены с Помощью рис. 113.
Равновесное давление НС1 над соляной кислотой понижается при внесении в раствор CuCl, NH4CI и повышается в присутствии TiCU, SnCl2, SnCl4. Предполагают, что в системах CuCl — HCl - Н20, CuCl — NH4CI — - HCl — Н20, NH4C1 —HCl — —Н20 образуются соединения соответственно: 2СиС1 • НС1, CuCl • 2NH4C1, NH4CI • «НС1 (и—зависит от температуры) 6. В системе CuCl2—НС1—Н20 при неизменной температуре давление пара Н20 уменьшается с возрастанием содержания в растворе как НС1, так и СиС12. Это указывает на то, что в системе происходит высаливание CuCI2 и HCI. В системе ZnCl2—HCl—Н20 взаимодействие компонентов более сложное—в области одних концентраций происходит высаливание, в области других — всали - вание отдельных компонентов6.
|
450 |
|
400 |
|
350 |
|
300 |
|
250 |
|
200 |
|
1} 16 20 24 28 32 36 40 Содержание НС1, бес. % |
|
Рис. 113. Интегральнаи S и дифференциальная Ф теплоты растворения газообразного НС1 в соляной кислоте. |
Для давления паров в системе НС1—Н20 характерен минимум, соответствующий азеотропной смеси, состав которой зависит от температуры кипения (давления). Азеотропная смесь, кипящая при
|
ТАБЛИЦА 29 Концентрации азеотропных растворов в системе НС1—Н20
|
110° (под давлением 760 мм рт. ст.), содержит 20,24 вес. % НС1, при 75,9—22,15%, при 56,2—23,2%, при 19,9—24,6% 7 (см. также табл. 26).
Температуры кипения соляной кислоты при давлении 760 мм рт. ст. приведены в табл. 27.
|
ТАБЛИЦА 27 Температуры кипения соляной кислоты при 760 мм Ptn. cm.
|
Коэффициенты активности соляной кислоты приведены в Табл. 28 (см. также®).
ТАБЛИЦА 28
|
Средние коэффициенты активности НС1 в водных растворах
|
В системе НС1—Н20 установлено существование двух эвтектик: при —74,7° с 23,0% НС1 и при —73,0° с 26,5% НС!. Между эвтек- тиками находится ветвь кристаллизации конгруэнтно плавящегося при —70° гексагидрата НС1 • 6Н20. Метастабильная эвтектика лед —НС1-4Н20 находится при —87,5° и содержит 24,8% НС19.
В системе НС1—Н20 существуют кристаллогидраты10'11: НС1 • 8Н20, НС1 • 4Н20, НСЬЗНаО" (*пл -24,4°), НС1 • 2Н20 ,{*пл —17,7°), НС1 • Н20 (/пл —15,35°). Лед кристаллизуется из .10%-ной кислоты при —20°, из 15%-ной при —30°, из 20%-ной при —60°, из 24%-ной при —80°.
Плотность соляной кислэты при 16°:
Концентрация HCl, % . . 10,17 20,01 30,56 39,11 Плотность, г/см3 1,050 1,100 1,165 1,200
Удельная теплоемкость с соляной кислоты, содержащей п молей воды на 1 моль НС1 п:
П ... ........... 5,2 10 ?0 50 100 290
С.............................. 0,660 0,749 0,885 0,932 0,964 0,970
Вязкость 2 н. соляной кислоты в 1,12 раза, а 12 и. кислоты в 2,14 раза больше вязкости воды.
Растворимость хлора в солянвй кислоте при 21е и парциальном
Давлении хлора 760 мм рт. ст.:
Концентрация кислоты, г-экв НС1/л. . 0 0,1 1,0 3,0 6,0 9,0 ббъем хлора (0°, 7б0 мм рт. ст.), раот-
Воряющийся в 1 объеме кислоты. . 2,117 1,48 1,61 2,16 2,90 3 85
Давление хлора над его раствором в 36,3%-ной соляной кислоте При 20° и при концентрации хлора 1,55 г/л составляет 141 мм рт. ст., А при 7,82 г/л— 551,8 мм рт. ст., н в этих пределах изменяется пропорционально концентрации хлора 12.
Отношение равновесной концентрации хлора в газовой фаэе к концентрации его в 1 н. соляной кислоте (коэффициент распределения) при 20° является величиной постоянной, равной 5,3- 105 мм рт. ст./мольные доли 13.
Число объемов (0°, 760 мм рт. ст.) водорода, кислорода и двуокиси углерода, растворяющихся в 1 объеме соляной кислоты при 25°, при парциальном давлении этих газов 760 мм рт. ст.:
Концентрация кислоты, г-экв НС1 /л 0 0,5 12 3
Растворяется Н2 . . ..................................... 0,01754 0,0170 Q.0164 0,0154 0,0146
» 02 ............................................... 0,02831 0,0271 0,0263 0,0345
» С02 ............................................. 0,759 0,738 0,732 0,728
О растворимости НС1 в серной кислоте можно судить по данным'4 равновесия в системе HCl—H2SO4—Н2О (табл. 29).
В водной системе Ma2S04 + 2HCl-=2NaCH-H2S04 при 25° установлено наличие поля насыщения у газообразного компонента —НС1. В растворе с максимальной концентрацией серной кислоты, находящейся в равновесии с NaCl и соляной кислотой при парциальном давлении НС1, равном 1 ат, содержится (в вес. %): H2S04 — 53,8, NaCl — 5,5, HCl —0,8. При взаимодействии газообразного хлористого водорода с декагидратом сульфата натрия выделяется поваренная соль и в растворе образуется серная кислота, содержащая 28% H2S04,18% HCl и 2,3% NaCl. Выход H2S04 Достигает 90—97% 1В.
|
369 |
|
Применение |
|
363 |
Г+ XL Соляная кислота
|
Равновесные концентрации в системе НС1—H2S04—Н20 (в вес. %; рНС1 — в мм рт. ст.) ТАБЛИЦА 59
|
Газообразный НС1 при парциальном давлении НС1, меньшем 0,1 мм рт. ст., быстро сорбируется смесью Na2S04+Na2S04 • ЮН20, по-видимому, с образованием твердого раствора Na2S04 + NaCl. Безводный Na2S04 не взаимодействует с газообразным НС1 при низких давлениях и начинает медленно реагировать лишь при давлении НС1, превышающем 2 ат 16.
Соляную кислоту применяют в химической промышленности для выработки хлористых солей цинка, кальция, бария, аммония и других и органических продуктов — анилина, дифениламина и прочих, для выработки синтетического каучука (хлоропрена), красителей, для омыления жиров и масел. Соляную кислоту применяют йри получении гидролизного спирта и глюкозы из крахмала, в производстве сахара, желатина и клея, при дублении и окраске кож, в производстве активированного угля, при крашении тканей, для травления металлов (снятия окислов с их поверхности) при металлообработке, в различных гидрометаллургических процессах, в гальванопластике, в нефтедобыче для увеличения дебита скважин, для консервирования кормов (в Японии) и т. д. Жидкий и газообразный хлористый водород применяют для гидрохлорирования раз - Личных органических соединений с целью получения хлористого этила C2HsCl, хлорвинила СН2СНС1 из ацетилена, этиленхлоргид- рина, синтетической камфоры и др.
В США производят более 1,8 мли. т в год соляной кислоты (100% НС1)17.
Выпускают несколько сортов твхничвекой соляной кислоты.(табл. 30).
ТАБЛИЦА 30
Требования к качеству соляной кислоты
|
Содержание НС1,не менее Максимальное содержание примесей: Серной кислоты (S03) серной кислоты (S04) Железа (Fe)....................... Мышьяка (As) .... свободного хлора (С12) остаток после прокаливания...................................... Ртути (Hg)........................ |
(содержание компонентов в °/о)
|
Техническая Синтетическая техническая
|
Очистка разбавленных растворов соляной кислоты (до 5 М) от
|
19 |
Соединений железа может быть произведена с помощью анионооб - менной смолы, которую регенерируют промывкой водой 18. Очистку концентрированной технической соляной кислоты (с концентрацией больше 32% НС1) от ионов Fe3+, Fe2+ и S04~ — предложено производить катионообменной смолой, приготовленной на основе фе
Нола
Показана возможность очищать соляную кислоту от железа экстракцией бутилацетатом — при содержании Fe (III) 10—25 г/л Степень извлечения его превышает 99,9% 20. Летучие примеси можно выдувать из соляной кислоты воздухом.
Соляную кислоту транспортируют в стальных гуммированных цистернах и бочках и в фаолитовых контейнерах, а также в стеклянных бутылях емкостью не более 40 л. Бутыли помещают в плетеные из прутьев корзины или деревянные обрешетки, выложенные соломой или древесной стружкой. Хранят соляную кислоту в стальных гуммированных резервуарах, а также в резервуарах, защищенных' фаолитом и винипластом21. Использование гуммированных цистерн и резервуаров сильно упрощается при осуществлении вулканизации обкладки без давления при низкой температуре22.
В отдельных случаях для транспортировки и хранения НС1, а также для санитарных целей может представить интерес поглощение хлористого водорода сульфатом меди или свинца, из которых он потом выделяется при нагревании23.
L
К техническому сульфату натрия, получаемому в соляно-суль- фатном производстве, по ГОСТ 1363—47 предъявляются следующие требования (в %):
I сорт II сорт
TOC o "1-3" h z Na2S04, не менее................................................................ 95 91
H2S04, не более................................................................. 1,5 3,5
NaCl » » . . ,.................................................................... 1,2 3,5
Fe » » ............................................................................. 0,2 0,25
Не растворимый в воде остаток, не более... 0,3 0,8