Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
КАРБАМИД
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
Карбамид CO(NH2)2 — диамид угольной кислоты (мочевина) В чистом виде представляет собой бесцветные кристаллы, не имеющие запаха, с плотностью 1,335 г/см3 и температурой плавления 132,4°. Технический карбамид — белые или желтоватые кристаллы, имеющие форму иглообразных ромбических призм; его насыпной вес колеблется в пределах 0,52—0,64 тм3 (в зависимости от влажности). В чистом карбамиде содержится 46,6% азота или, в пересчете на аммиак, 56,7%.
Сухой карбамид при нагревании под атмосферным давлением выше температуры плавления разлагается. Механизм его разложения предполагается следующий. Вначале карбамид изомеризуется в цианат аммония, который диссоциирует на циановую кислоту и аммиак:
CO(NH2)2 —* NH4NCO —У HNCO + NH3
Циановая кислота, "взаимодействуя с карбамидом, образует биурет:
HNCO + СО (NH2)2 = NH2CONHCONH2
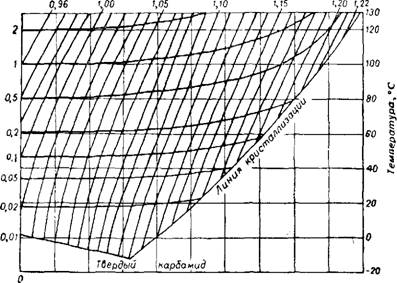
При более сильном нагревании биурет разлагается на аммиак и циановую кислоту, полимеризующуюся в циануровую кислоту (HNCO)3, которая образует с выделившимся аммиаком амиды й имиды циануровой кислоты1_8. В присутствии избытка аммиака разложение карбамида приостанавливается 9. Добавление NH4NO3 к карбамиду приводит к весьма существенной стабилизации последнего, тем большей, чем больше содержится нитрата в смеси |0. Насыщенный раствор карбамида в воде при 20° содержит 51,83%, при 60° — 71,88%, при 120° —95% CO(NH2)2. Выше 130° в водном растворе карбамид разлагается на аммиак и двуокись углерода. Температуры кипения водных растворов карбамида различной концен-
грации при различных давлениях могут быть определены по номограмме на рис. 373. Линия, ограничивающая на номограмме сетку кривых, — кривая растворимости. Эвтектика соответствует температуре —12° и концентрации 32% CO(NH2)2. Косые линии, идущие сверху вниз, — величины плотности растворов, а кривые, идущие слева направо, — давления насыщенного пара над растворами.
|
Плотность раствора, 3/C«J |
|
T 6 S <* О W |
|
Ю 20 30 40 50 ео 70 80 90 Концентрация карбамида, г/100г раствора |
|
Рис. 373. Свойства водных растворов карбамида (номограмма Фрежака), |
|
I |
Карбамид хорошо растворяется в спирте и в аммиаке. С аммиаком образует соединение (ИНгЬСО • NH3, содержащее 77,9% карбамида и 22,1% аммиака. С повышением температуры растворимость карбамида в аммиаке значительно повышается; выше 30° растворимость карбамида в жидком аммиаке больше, чем в воде.
Давление паров аммиака над растворами карбамида в аммиаке значительно ниже, чем над жидким аммиаком.
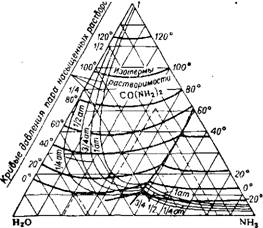
На рис. 374 приведена диаграмма состояния системы карбамид—аммиак—вода и кривые давления пара насыщенных растворов 1!.
Карбамид вступает в реакцию с кислотами, давая солеобраз - ные соединения. Например, малорастворимый в воде нитрат карбамида NH2C0NH2-HN03 кристаллизуется в виде моноклинных призм, плавящихся при 163° (при нагревании разлагается со
взрывом), фосфат карбамида NH2CONH2-H3PO.j образует ромбические кристаллы с температурой плавления 117,5°. Фосфат карбамида хорошо растворяется в воде 12, но при этом полностью диссоциирует.
С солями карбамид образует комплексные соединения. Большой интерес представляют, в частности, те из них, в которых оба компонента являются удобрениями, например Са (N03)2-4C0(NH2)2 и
NH4C1-C0(NH2)213.14.
|
^ СО(КНг)г
Рнс. 374. Диаграмма состояния системы карбамид — аммнак — вода (в мол. %) с кривыми давления пара насыщенных растворов (тонкие линии). |
При взаимодействии карбамида с монокальцийфосфатом образуются фосфат карбамида и дикальцийфосфат 15>16
Са (Н2Р04)2 • Н20 + СО (NH2)2 = СО (NH2)2 • Н3Р04 + СаНР04 + Н20
При нагревании водных растворов карбамида под атмосферным давлением выше 80° в результате гидратации карбамид переходит в карбамат аммония:
СО (NH2)2 + Н20 = NH2COONH4
Карбамат аммония (соль карбаминовой кислоты NH2COOH) плавится при 145—150°. В присутствии карбамида, воды и аммонийных солей температура плавления карбамата аммония снижается.
При растворении в воде карбамат аммония частично гидратируется с образованием карбоната
NH2COONH4+HJO ^rt (NH4)2COS
Который в последующем превращается в бикарбонат аммония, распадающийся в свою очередь на аммиак и двуокись углерода: (NH4)2 СОЗ = NH4HCO3 + NH3 NH4HCO3 = С02 + н20 + NH3
В разбавленных растворах карбамат аммония почти полностью переходит в карбонат. Степень гидролиза карбамата аммония значительно понижается в присутствии аммиака.
На рис. 375 показана, растворимость в системе NH2COONH4—Н20 17> 18. Ниже 60° растворы карбамата аммония содержат примеси других аммонийных солей. От —13 до +5° карбамат аммония находится в растворе совместно с карбонатом, а от +5 до +60° с комплексной солью (NH4) 2С03 • 2NH4HC03 — сескви - карбонатом аммония.
В интервале температур от 0 до 118° растворимость карбамата аммония в жидком аммиаке незначительна. В присутствии карбамида его растворимость в аммиаке повышается.