Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ОСАЖДЕНИЯ ДИКАЛЬЦИЙФОСФАТА(ПРЕЦИПИТИРОВАНИЯ)
Суммарные реакции осаждения дикальцийфосфата из раствора фосфорной кислоты известью или известняком при температуре ниже 50°:
Н3РО4 +Са(ОН)2 = СаНР04 • 2Н20
Или
Н3РО4 + СаСОз + Н20 = СаНР04 • 2Н20 + С02
Не отражают химизма процесса.
Вначале известь или известняк полностью растворяются, образуя монокальцийфосфат, например:
Са(ОН)2 + 2Н3Р04 = Са(Н2Р04)2 + 2Н20
В дальнейшем, по мере нейтрализации фосфорной кислоты, монокальцийфосфат инконгруэнтно разлагается в растворе с выделением в осадок дикальцийфосфата:
Са(Н2Р04)2 + 2Н20 = СаНР04 • 2Н20 + Н3Р04
Помимо этого монокальцийфосфат также реагирует с новыми порциями извести или известняка:
Са(ОН)2 + Са(Н2Р04)2 + 2Н20 = 2[СаНР04 • 2Н20]
Избыток извести сверх теоретического весового отношения СаО : Р205 в дикальцийфосфате (равного 0,79 и соответствующего рН раствора 6,3) приводит к разложению дикальцийфосфата:
4СаНР04 = Са(Н2Р04)2+ Са3(Р04)2
При этом Рг05 наполовину переходит в трикальцийфосфат, т е. в плохо усвояемую растениями форму. В присутствии избытка известняка ретроградации преципитата не происходит.
|
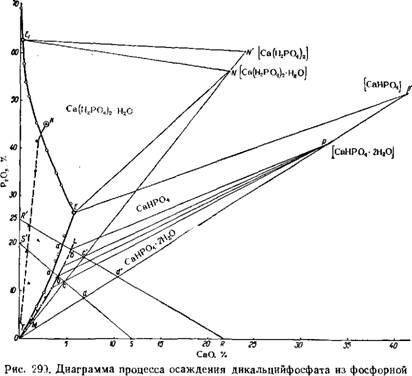
Кислоты: ОЕ- стабильная и ML — метастабильная ветви изотермы системы СаО—Р2О5 — НгО при 40°; кг-ветвь растворимости СаНР04 в системе Ca0-P205-H2SIF6-H20 при 60°. |
Примеси, содержащиеся в фосфорной кислоте, также реагируют с известью или известняком:
H2S04 + Ca(0H)2 = CaS04-2H20 H2SiF6 + ЗСа(ОН)2 = 3CaF2 + Si02 + 4Н20
И др.
В результате этого уменьшается содержание усвояемой Р2О5 в продукте и затрудняется отфильтровывание преципитата из-за выделяющихся илистых осадков кремневой кислоты и др.
На диаграмме системы СаО—Р205—Н20 при 40° (рис. 299) показаны условия преципитирования фосфорной кислоты концентрацией 20% Р2О5 (точка S') известковым молоком, содержащим 12% СаО (точка S), и кислоты концентрацией 25% Р205 точка R') суспензией известняка с отношением Ж: Т, равным,5 : 1, и концентрацией СаО около 22% (точка R). При преципи - тировании состав системы изменяется вдоль соединительных прямых SS' и RR'.
В равновесных условиях, при нейтрализации кислоты до образования насыщенного раствора в точках а и а', жидкая фаза, состоящая из свободной Н3Р04 и Са(Н2Р04)2, должна стать насыщенной по отношению к дикальцийфосфату СаНР04. Практически насыщение наступает позже, в точках b и Ь' на метаста- бильной ветви ML растворимости твердой фазы СаНР04*2Н20. Для ее кристаллизации необходимо образование растворов, пересыщенных метастабильной фазой. Интенсивное образование ди - кальцийфосфата, по-видимому, начинается в момент полной нейтрализации первого иона водорода фосфорной кислоты (точки с и с'), т. е. при растворении половинного количества окиси кальция, затрачиваемой на осаждение преципитата.
Как указывалось выше, кристаллизация дикальцийфосфата происходит, по-видимому, в результате разложения монокальцийфосфата из-за инконгруэнтности состава равновесных его растворов по отношению к составу твердых фаз * (луч растворения монокальцийфосфата ONN' проходит вне поля кристаллизации этой соли):
Са(Н2Р04)2 + 2Н20 = СаНР04 • 2Н20 + Н3Р04
В указанных точках степень разложения монокальцийфосфата70-72 составляет соответственно 32,6 и 36,1%. Образование свободной фосфорной кислоты в момент спонтанной кристаллизации дикальцийфосфата и вызывает интенсивное разложение оставшегося карбоната, не прореагировавшего к этому моменту.
Изучение системы СаО—Р205—H2SiF6—Н20 при 60° показало73, что растворимость дикальцийфосфата резко снижается под влиянием образующегося CaF2 (см. изотерму КТ на рис. 299). В связи с этим преципитирование экстракционной необесфторенной фосфорной кислоты протекает, вероятно, в условиях более высоких пересыщений.
Фосфорная кислота, получаемая сернокислотным методом из необогащенных фосфоритов Каратау, содержит до 15% MgO по отношению к Р205. Осаждение дикальцийфосфата в данном случае должно быть рассмотрено с помощью диаграммы системы MgO—СаО—Р205—Н20 74. При норме СаО 0,71 вес. ч. на 1 вес. ч. Р205 (90% от стехиометрической®6) фосфаты магния остаются в жидкой фазе. Только применение избытка СаО в виде известкового молока позволяет почти полностью осадить Р205 (частично, в виде димагнийфосфата).
Реакция нейтрализации фосфорной кислоты известью (в виде известкового молока) протекает с очень высокой скоростью. При смешении фосфорной кислоты с известковым молоком создается пересыщение раствора в тонком слое вокруг частиц извести, что вызывает осаждение фосфатов кальция в виде корок, замедляющих дальнейший процесс. Медленное введение известкового молока, высокая дисперсность частиц извести и интенсивное перемешивание уменьшает опасность таких «местных» пересыщений.
Скорость осаждения преципитата карбонатами определяется скоростью разложения последних фосфорной кислотой. Природные известняки, начиная от меловидных до мрамороподобных пород, обладают различной плотностью. Более плотные разновидности требуют для своего разложения наиболее тонкого измельчения (до 0,075—0,060 мм), менее плотные породы измельчают до величины частиц 0,10—0,075 мм. Осажденный мел и мел-рухляк реагируют с наибольшей скоростью. Фосфорная кислота концентрации KV-45% Р2О5 разлагает тонко измельченный известняк соответственно на 80—90% в течение 10—15 мин. После нейтрализации фосфорной кислоты до рН = 3,8—4,0, разложение карбоната резко замедляется. Частичная нейтрализация катионами фосфорной кислоты, полученной сернокислотной экстракцией низкокачественных фосфоритов, значительно уменьшает скорость разложения известняка. Фосфорнокислые растворы, полученные взаимодействием соляной кислоты и фосфоритов, разлагают известняк с большей скоростью чем фосфорная кислота той же концентрации, полученная сернокислотным способом.
Нейтрализация фосфорной кислоты известняком осложняется обильным выделением двуокиси углерода с образованием в слое пены очень мелких кристаллов дикальцийфосфата. Найдены75-77 способы, предотвращающие бурное вспенивание пульпы. При периодическом преципитировании суспензия известняка должна вводиться медленно, синхронно с разложением карбоната. Для уменьшения степени пересыщения раствора целесообразно после введения около 70% известняка в течение некоторого времени прекратить его подачу и затем продолжать осаждение. При непрерывном процессе следует вводить в первый реактор всю фосфорную кислоту и не больше 70% известняка, во втором реакторе производить только перемешивание пульпы и заканчивать осаждение в третьем реакторе, вводя в него остальное количество суспензии известняка. Такой же режим необходим и при осаждении преципитата известковым молоком. Несоблюдение этого приводит к осаждению мелких (5—50 т) кристаллов дикальцийфосфата. При раздельном введении суспензии известняка выделяются крупные кристаллы дикальцийфосфата длиной до 100—150 мк и до 50 мк Шириной, большей частью собранные в конгломераты. При раздельном введении известкового молока образуются кристаллы примерно таких же размеров, но более тонкие. Очень мелкие кристалллы образуются под влиянием примесей экстракционной фосфорной кислоты 78.
В конце преципитирования процесс затормаживается образованием на частицах карбоната и, особенно, извести непроницаемой корки кристаллов дикальцийфосфата. По условиям равновесия в системе СаО—Р205—Н20 фосфорная кислота должна осаждаться почти полностью. Практически же с помощью известняка нейтрализовать всю фосфорную кислоту оказывается невозмож -
|
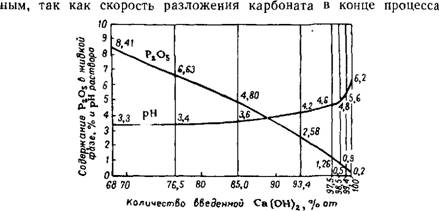
Стехиометрической нормы Рис. 300. Изменение рН раствора в процессе преципитирования фосфорной кислоты. |
Крайне мала. Причиной этого, помимо образования экранирующей корки с большим диффузионным сопротивлением, является и почти 100%-ная нейтрализация первого иона водорода в жидкой фазе. Остаточное содержание Р2О5 в растворе может быть доведено обычно до 0,2—0,3%. Большая степень осаждения Р205 известковым молоком достигается только при условии высокой дисперсности частиц извести (не крупнее 0,15 мм). Более крупные частицы извести покрываются непроницаемой коркой, вследствие этого жидкая фаза может содержать до 3% Р205, несмотря на присутствие в твердой фазе свободной извести. Для получения высокодисперсного известкового молока требуется производить гашение извести трехкратным количеством горячей воды79. Помимо этого необходима классификация известкового молока для выделения частиц размером свыше 0,15 мм. Избыток свободной извести в твердой фазе может привести к образованию более основных фосфатов кальция (трикальцийфосфата и гидроксилапатита), плохо усвояемых растениями.
Изменение рН раствора и концентрации в нем Р2О5 в зависимости от количества введенной извести показано на рис. 300.
Кристаллизация дикальцийфосфата начинается после прибавления 50% извести от стехиометрического количества (см. выше), когда рН раствора становится равным 3—3,2. При последующем введении извести величина рН постепенно возрастает примерно до 4,8, а затем даже при добавке незначительного количества извести величина рН резко увеличивается, что вызывает образование трикальцийфосфата.
При рН около 4,8 первый ион водорода фосфорной кислоты полностью нейтрализуется. В этой точке происходит резкий перелом кривой рН, поэтому именно в данной области осаждение нужно вести очень осторожно, чтобы не ввести избыток извести. Резкий перелом кривой изменения рН позволяет контролировать конец преципитирования, который определяют по индикатору метиловому красному, изменяющему окраску до желто-оранжевой; более удобен смешанный индикатор (метиловый красный и метиловый синий) окраска которого изменяется от фиолетовой до светло-зеленой 80.